Діючі речовини: Цефтибутен
Ізоцеф 200 мг тверді капсули
Ізоцеф 400 мг тверді капсули
Вставки для упаковки Isocef доступні для розмірів упаковки: - Ізоцеф 200 мг тверді капсули, Ізоцеф 400 мг тверді капсули
- Ізоцеф 36 мг / мл гранули для пероральної суспензії
- Isocef 400 мг гранули для пероральної суспензії, Isocef 200 mg гранули для пероральної суспензії
Показання Для чого використовується Ізоцеф? Для чого це?
Ізоцеф містить діючу речовину цефтибутен.
Цефтибутен-це антибіотик, що належить до класу бета-лактамів та до сімейства ліків, які називаються цефалоспоринами.
Ізоцеф використовується проти бактерій, чутливих до ліків.
Ізоцеф показаний при лікуванні:
- інфекції верхніх дихальних шляхів: горла (фарингіт, тонзиліт), порожнин біля носа (гайморит) та вух (отит)
- інфекції нижніх дихальних шляхів: бронхів (бронхіт), легенів (первинна позалікарняна пневмонія) та бронхів і легенів одночасно (бронхопневмонія)
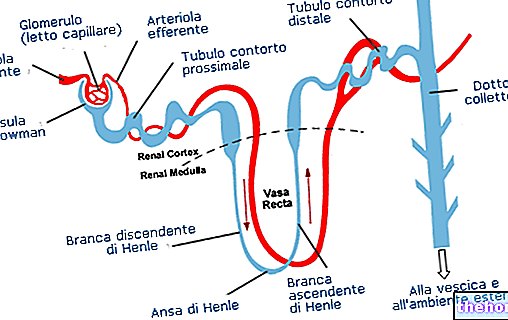
- інфекції сечовивідних шляхів: нирок, сечового міхура та протоки, що переносить сечу з сечового міхура назовні (гострий та хронічний пієліт, цистопієліт, цистит, уретрит) та як лікарський засіб вибору при гострому неускладненому гонококовому уретриті.
Протипоказання Коли Ізоцеф не слід застосовувати
Не використовуйте Isocef
- якщо у вас алергія на діючу речовину, будь -який інший цефалоспорин або будь -який інший інгредієнт цього препарату (перерахований у розділі 6)
- якщо у вас виникли важкі та раптові алергічні реакції (анафілаксія) на інші антибіотики, які називаються пеніцилінами або іншими антибіотиками сімейства бета-лактамних
- якщо ви вагітні або підозрюєте, що вагітні (див. Вагітність та годування груддю)
- якщо це для дитини віком до шести місяців (див. "Попередження та запобіжні заходи").
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Ізоцеф
Поговоріть зі своїм лікарем або фармацевтом перед використанням Isocef, якщо:
- мають тяжкі пошкодження нирок (ниркова недостатність) або перебувають на діалізі, і в цьому випадку ваш лікар вирішить, яку дозу Ізоцефу використати. Якщо ви перебуваєте на діалізі, ваш лікар уважно стежитиме за вашим здоров’ям і призначить введення Isocef одразу після діалізу.
- у вас проблеми зі шлунком і кишечником, особливо якщо у вас хронічне запалення товстої кишки (хронічний коліт), ваш лікар буде обережно призначати цей препарат
- Під час терапії Ізоцефом може виникнути «зміна кишкової флори (бактерії, наявні в« кишечнику ») з настанням помірної та важкої діареї (включаючи псевдомембранозний коліт, спричинений токсинами Clostridium difficile)
- маєте в анамнезі алергію або підозрюєте алергію на клас антибіотиків під назвою пеніциліни. Якщо у вас алергія на пеніциліни, у вас також може бути алергія на цефалоспозрин (перехресна реактивність), а також можуть виникнути важкі та раптові алергічні реакції (анафілаксія). У цих випадках ваш лікар припинить терапію Ізоцефом і призначить вам відповідну терапію. судоми або алергічний шок під час застосування Ізоцефу, Ваш лікар негайно припинить введення ліків і негайно розпочне відповідне лікування, якщо Ви приймаєте ліки, що затримують згортання крові, оскільки Ізоцеф може зменшити здатність зупиняти кровотечу. специфічні аналізи крові (час тромбопластину або Міжнародний нормалізований коефіцієнт - МНВ).
Діти
Ізоцеф не показаний дітям до шести місяців.
Взаємодії Які ліки або продукти харчування можуть змінити дію Ізоцефу
Повідомте свого лікаря або фармацевта, якщо ви використовуєте, нещодавно використовували або могли б використовувати інші ліки.
Ізоцеф не взаємодіє з лікарськими засобами, що знижують кислотність шлунка на основі алюмінію-магнію та ранітидину, та ліками від астми на основі теофіліну (разова доза, що вводиться внутрішньовенно).
Цефалоспорини, включаючи ізоцеф, можуть у рідкісних випадках взаємодіяти з лікарськими засобами, які затримують згортання крові та можуть зменшувати здатність зупиняти кровотечу. У цих випадках лікар призначить конкретні аналізи крові (протромбіновий час).
Isocef з продуктами харчування
Одночасний прийом їжі не впливає на ефективність капсул Isocef.
Попередження Важливо знати, що:
Вагітність та годування груддю
Якщо ви вагітні або годуєте грудьми, думаєте, що можете бути вагітними або плануєте народження дитини, перед застосуванням цього препарату зверніться за порадою до лікаря або фармацевта.
Введення Ізоцефу під час вагітності та годування груддю необхідно оцінити з точки зору потенційного ризику та користі як для матері, так і для плоду.
Час годування
Цефтибутен проникає у грудне молоко, тому у немовлят може виникнути діарея, яка вимагає можливого припинення грудного вигодовування.
Через розвиток можливої алергії Ізоцеф слід призначати під час годування груддю лише тоді, коли користь від нього перевищує ризик.
Водіння автомобіля та роботу з машинами
Ізоцеф не впливає на здатність керувати автомобілем та працювати з механізмами.
Дозування та спосіб застосування Як використовувати Ізоцеф: Дозування
Завжди використовуйте цей препарат точно так, як вам сказав ваш лікар або фармацевт. Якщо є сумніви, зверніться до лікаря або фармацевта.
Рекомендована доза для дорослих становить:
- інфекції нижніх дихальних шляхів
- пневмонія: 200 мг 2 рази на день
- бронхіт: 400 мг 1 раз на добу
- інфекції верхніх дихальних шляхів
- 400 мг 1 раз на добу
- інфекції сечовивідних шляхів
- 400 мг 1 раз на добу
Капсули Isocef можна приймати незалежно від часу прийому їжі. Капсули слід ковтати з невеликою кількістю води.
Якщо ви забули використовувати Ізоцеф
Не використовуйте подвійну дозу, щоб компенсувати пропущену дозу.
Якщо Ви припините прийом Ізоцефу
Якщо у вас виникнуть додаткові запитання щодо застосування цього препарату, зверніться до лікаря або фармацевта.
Передозування Що робити, якщо ви прийняли занадто багато Isocef
Токсичних проявів після випадкового передозування Ізоцефу не виявлено.
У разі випадкового проковтування / прийому надмірної дози Isocef негайно повідомте про це свого лікаря або зверніться до найближчої лікарні.
Побічні ефекти Які побічні ефекти ізоцефу
Як і всі ліки, цей препарат може викликати побічні ефекти, хоча вони виникають не у всіх.
У клінічних дослідженнях, проведених приблизно у 3000 пацієнтів, найчастіше повідомлялося про побічні ефекти:
- нудота (3%)
- діарея (3%)
- головний біль (головний біль) (2%).
У ході клінічних випробувань та постмаркетингового спостереження спостерігалися такі небажані ефекти:
Поширені (можуть виникнути до 1 з 10 осіб)
- головний біль (головний біль)
- нудота
- діарея
Нечасті (можуть виникнути у 1 з 100 осіб)
- грибкова інфекція (кандидоз ротової порожнини)
- вагінальна інфекція - збільшення еозинофілів (тип клітин крові) (еозинофілія)
- позитивний прямий тест Кумбса * (лабораторне дослідження)
- зниження гемоглобіну (білка, який переносить кисень у крові)
- Тривалий протромбіновий час (який вказує, як довго згортається кров)
- збільшення INR (значення, яке вказує на час згортання крові)
- втрата апетиту (анорексія)
- зниження смаку (дисгевзія)
- закладений ніс (закладеність носа)
- утруднене дихання (задишка)
- запалення шлунка (гастрит)
- Він смикався
- біль у животі
- запор
- сухість у роті, труднощі переварювання (диспепсія)
- викиди повітря з заднього проходу (метеоризм)
- нетримання калу
- збільшення деяких параметрів функції печінки: білірубіну та трансаміназ (гіпербілірубінемія *, збільшення АСТ та АЛТ)
- утруднення сечовипускання (дизурія)
- ниркова недостатність *
- ураження нирок (токсична нефропатія *)
- наявність цукру та інших речовин, що називаються кетоновими тілами, в сечі (ниркова глікозурія * та кетонурія *)
* спостерігається з іншими цефалоспоринами і може виникнути при застосуванні Ізоцефу.
Рідкісні (можуть виникнути до 1 з 1000 осіб)
- запалення частини кишечника, що називається товстою кишкою, викликане бактеріальною інфекцією (коліт Clostridium difficile)
- зменшення кількості типів клітин крові, які називаються лейкоцитами (лейкопенія)
- зменшення кількості тромбоцитів (тромбоцитемія)
- зменшення кількості еритроцитів (апластична анемія, гемолітична анемія)
- порушення кровотечі
- зменшення кількості всіх типів клітин крові (панцитопенія)
- зменшення кількості типів лейкоцитів, які називаються нейтрофілами (нейтропенія)
- різке зменшення кількості лейкоцитів (агранулоцитоз)
- судоми
- збільшення показників крові деяких параметрів функції печінки (лактатдегідрогеназа - ЛДГ)
Дуже рідко (може виникнути до 1 з 10 000 осіб)
- порушення чутливості (парестезія)
- сонливість
- запаморочення
- втома
Невідомо (частоту неможливо оцінити за наявними даними)
- інфекції, що перекриваються (суперінфекція)
- сироваткова хвороба (характеризується шкірним висипом, болем у суглобах, лихоманкою, збільшенням лімфатичних вузлів, зниженням артеріального тиску та збільшенням селезінки)
- реакції гіперчутливості, включаючи важкі та раптові реакції (анафілактична реакція)
- скорочення м’язів бронхів (бронхоспазм)
- висип
- кропив’янка
- чутливість до світла (фоточутливість)
- свербіж
- важкі шкірні реакції (ангіоневротичний набряк, синдром Стівенса-Джонсона, мультиформна еритема та токсичний епідермальний некроліз)
- психічні (психотичні) розлади
- порушення мови (афазія)
- темний стілець (мелена)
- печінкові (гепатобіліарні) порушення та пожовтіння шкіри та очей (жовтяниця).
Додаткові побічні ефекти у дітей
Нечасті (можуть виникнути до 1 на 100 дітей)
- запалення шкіри (пелюшковий висип)
- кров у сечі (гематурія)
Дуже рідко (може виникнути до 1 на 10000 дітей)
- агітація
- безсоння
- надмірне рух (гіперкінез)
- дратівливість
- охолодження
Повідомлення про побічні ефекти
Якщо у Вас виникли будь -які побічні ефекти, зверніться до лікаря або фармацевта, що включає будь -які можливі побічні ефекти, не зазначені у цій інструкції. Ви також можете повідомляти про побічні ефекти безпосередньо через національну систему звітності на веб -сторінці "www.agenziafarmaco.it/it/responsabili". Повідомляючи про побічні ефекти, ви можете допомогти надати більше інформації про безпеку застосування цього препарату.
Термін придатності та утримання
Не зберігати при температурі вище 25 ° C.
Зберігайте цей препарат подалі від очей та недоступного для дітей місця.
Не використовуйте цей препарат після закінчення терміну придатності, зазначеного на картонній упаковці після напису "Термін дії".
Термін придатності відноситься до останнього дня цього місяця.
Не викидайте ліки через стічні води або побутові відходи. Попросіть свого фармацевта, як викинути ліки, які ви більше не використовуєте. Це допоможе захистити навколишнє середовище.
Інша інформація
Що містить Ізоцеф
- Діюча речовина - цефтибутен. Кожна капсула містить 200 мг або 400 мг цефтибутену
- Допоміжні інгредієнти: целюлоза мікрокристалічна, амідогліколят натрію, стеарат магнію. Компоненти капсули: желатин, діоксид титану, лаурилсульфат натрію. Компоненти ущільнювальної стрічки: желатин, полісорбат 80
Як виглядає Isocef та вміст упаковки
Isocef випускається у формі твердих капсул для перорального застосування.
Він доступний у наступних упаковках:
- 200 мг: 6 і 12 твердих капсул у блістері.
- 400 мг: 4 і 6 твердих капсул у блістері.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
ISOCEF
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
ISOCEF 200 мг тверді капсули
Діючий принцип:
Кожна тверда капсула містить 200 мг цефтибутену.
ISOCEF 200 мг гранули для пероральної суспензії
Діючий принцип:
Кожен пакетик містить 200 мг цефтибутену.
Допоміжні речовини з відомими ефектами
Кожен пакетик містить 1,11 г сахарози і 5,56 мг бензоату натрію.
ISOCEF 400 мг тверді капсули
Діючий принцип:
Кожна тверда капсула містить 400 мг цефтибутену.
ISOCEF 400 мг гранули для пероральної суспензії
Діючий принцип:
Кожен пакетик містить 400 мг цефтибутену.
Допоміжні речовини з відомими ефектами
Кожен пакетик містить 2,23 г сахарози і 11,12 мг бензоату натрію.
ISOCEF 36 мг / мл гранули для пероральної суспензії
Діючий принцип:
У 100 г гранул міститься 14,40 г цефтибутену.
Допоміжні речовини з відомими ефектами
Кожен флакон містить 80,31 г сахарози і 0,40 г бензоату натрію.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Тверді капсули.
Гранули для пероральної суспензії.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Ізоцеф показаний для лікування інфекцій, спричинених чутливими збудниками, зокрема:
• Інфекції верхніх дихальних шляхів: фарингіт, тонзиліт, синусит, середній отит.
• Інфекції нижніх дихальних шляхів: бронхіт, первинна позалікарняна пневмонія, бронхопневмонія.
• Інфекції сечовивідних шляхів: гострий та хронічний пієліт, цистопієліт, цистит, уретрит. Як препарат другої лінії при неускладненому гострому гонококовому уретриті.
04.2 Дозування та спосіб введення
Дозування
Дорослі
Інфекції нижніх дихальних шляхів
Пневмонія: 200 мг двічі на день;
бронхіт: 400 мг 1 раз на добу.
Інфекції верхніх дихальних шляхів: 400 мг один раз на день.
Інфекції сечовивідних шляхів: 400 мг один раз на день.
Педіатричне населення
Діти старше 6 місяців
Неускладнені інфекції нижніх дихальних шляхів: 9,0 мг / кг один раз на день.
Інфекції верхніх дихальних шляхів (наприклад, середній отит): 9,0 мг / кг один раз на день.
Інфекції сечовивідних шляхів: 9,0 мг / кг один раз на день.
Максимальна добова доза для дітей не повинна перевищувати 400 мг / добу.
Безпека та ефективність у дітей віком до 6 місяців ще не встановлені.
Спосіб введення
Гранули Ізоцефу для пероральної суспензії можна приймати за одну -дві години до або після їжі.
Капсули Isocef можна приймати незалежно від часу прийому їжі.
04.3 Протипоказання
Підвищена чутливість до активної речовини, до будь -якого іншого цефалоспорину або до будь -якої з допоміжних речовин, перерахованих у розділі 6.1.
Ізоцеф не можна застосовувати пацієнтам, у яких були відомі серйозні або гострі реакції гіперчутливості (анафілаксія) до пеніцилінів або інших бета-лактамних антибіотиків.
Досвід застосування у дітей віком до шести місяців недостатній для встановлення безпеки застосування цефтибутену у цій популяції пацієнтів.
Вагітність (див. Розділ 4.6)
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
Порушення функції нирок
Пацієнтам з вираженою нирковою недостатністю або пацієнтам, які проходять діаліз, може знадобитися коригування дози Ізоцефу. Ізоцеф легко піддається діалізу. Пацієнти, які перебувають на діалізі, повинні перебувати під ретельним наглядом, при цьому Ізоцеф слід вводити одразу після діалізу.
На фармакокінетику та дозування цефтибутену не впливає помірне порушення функції нирок (кліренс креатиніну між 50-79 мл / хв). Пацієнтам з кліренсом креатиніну між 30-49 мл / хв добову дозу слід зменшити вдвічі. При більш низьких значеннях кліренсу креатиніну потрібна подальша корекція дози. У пацієнтів з нирковою недостатністю, які проходять діаліз, може знадобитися коригування дози. Пацієнтам, які перебувають на діалізі 2/3 рази на тиждень, рекомендується вводити разову дозу ізоцефу 400 мг в кінці кожного діалізного лікування.
Шлунково -кишковий тракт
Ізоцеф слід з обережністю призначати особам, які мають в анамнезі складні шлунково -кишкові захворювання, особливо хронічний коліт.
Clostridium difficile
Під час терапії Ізоцефом та іншими антибіотиками широкого спектру дії може виникнути «зміна кишкової флори з настанням антибіотико-асоційованої діареї», включаючи псевдомембранозний коліт через токсини. Clostridium difficile. Пацієнти можуть мати діарею помірного або тяжкого ступеня або смертельну, з зневодненням або без нього, як під час, так і після лікування супутнім антибіотиком. Важливо пам’ятати цей діагноз для будь -якого пацієнта, у якого спостерігається стійка діарея протягом або до двох місяців після застосування Ізоцефу або іншого антибіотика широкого спектру дії.
Легкі форми псевдомембранозного коліту зазвичай сприятливо реагують на просте припинення прийому препарату. При середніх або важких формах лікування повинно включати сигмоїдоскопію, відповідне бактеріологічне дослідження та введення рідин, електролітів та білків. У випадках, коли коліт не поліпшується після припинення прийому препарату, а у важких випадках - застосування перорального ванкоміцину є методом вибору при псевдомембранозному коліті. Clostridium difficile викликається антибіотиками. Необхідно виключити інші причини коліту.
Гіперчутливість
Цефалоспоринові антибіотики слід призначати з особливою обережністю пацієнтам з відомою або підозрюваною алергією на пеніциліни. Приблизно 5% пацієнтів з підтвердженою алергією на пеніцилін перехресно реагують на антибіотики цефалоспоринового ряду. Важкі гострі реакції гіперчутливості (анафілаксія) також спостерігалися у осіб, які отримували пеніциліни або цефалоспорини, і може спостерігатися перехресна реакція з анафілаксією. Важка анафілаксія вимагає відповідного невідкладного лікування за клінічними показаннями (адреналін, внутрішньовенна інфузія рідини, введення кисню, антигістамінні препарати, кортикостероїди, інші пресорні аміни).
Також слід бути гранично обережним при призначенні Ізоцефу пацієнтам з будь -якими алергічними реакціями (наприклад, сінною лихоманкою або бронхіальною астмою), оскільки ці пацієнти мають підвищений ризик розвитку тяжких реакцій гіперчутливості.
Якщо під час застосування Ізоцефу виникають судоми або алергічний шок, застосування Ізоцефу слід негайно припинити та негайно розпочати відповідне лікування.
Гематологія
Цефалоспорини, включаючи цефтибутен, можуть у рідкісних випадках знижувати активність протромбіну, що призводить до подовження тромбопластинового часу, особливо у пацієнтів, які раніше стабілізувалися на пероральній антикоагулянтній терапії. Цим пацієнтам слід вводити вітамін К.
Важлива інформація про деякі інгредієнти
Гранули Isocef містять сахарозу Пацієнтам з рідкісними спадковими проблемами непереносимості фруктози, мальабсорбції глюкози-галактози або недостатністю сахарази-ізомальтази не слід приймати цей препарат
Гранули Ізоцефу для пероральної суспензії містять бензоат натрію. У новонароджених це може збільшити ризик жовтяниці.
Після відкриття пляшки або пакетиків може бути виявлений сірчаний запах, який не погіршує якість продукту. Після розчинення сірчистий запах зникає.
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Були проведені дослідження взаємодії між Ізоцефом та кожною з наступних речовин: антациди з високим вмістом гідроксиду алюмінію-магнію, ранітидин та теофілін в одній дозі, що вводиться внутрішньовенно. Суттєвих взаємодій не відбулося. Вплив ізоцефу на рівні плазми та фармакокінетику перорально введеного теофіліну невідомий.
Цефалоспорини, включаючи цефтибутен, можуть у рідкісних випадках знижувати активність протромбіну, що призводить до подовження протромбінового часу, особливо у пацієнтів, які раніше стабілізувалися на пероральній антикоагулянтній терапії. У пацієнтів групи ризику слід контролювати протромбіновий час, при необхідності призначаючи вітамін.
На сьогоднішній день не повідомляється про значні взаємодії з іншими препаратами. Вони не спостерігалися при хімічних ізоцефальних взаємодіях або при лабораторних дослідженнях. Помилковий позитивний результат прямого тесту Кумбса був зареєстрований при застосуванні інших цефалоспоринів. Прямий Кумбс не виявив позитивних реакцій навіть до концентрацій 40 мкг / мл.
Одночасний прийом їжі не впливає на ефективність капсул Isocef, хоча може затримувати та зменшувати всмоктування суспензії Isocef.
04.6 Вагітність та період лактації
Вагітність
Не існує адекватних та контрольованих досліджень щодо застосування лікарського засобу вагітним жінкам, під час пологів або пологів. Оскільки на даний час немає клінічного досвіду застосування цефтибутену під час вагітності, препарат слід вводити лише тоді, коли це дійсно необхідно, безпосередньо Оскільки дослідження репродукції на тваринах не завжди є передбачувальними для людини, введення Isocef під час вагітності та лактації слід оцінювати з точки зору потенційного ризику та користі як для матері, так і для плоду.
Час годування
Цефтибутен виділяється з грудним молоком, тому у немовлят можуть виникнути зміни у кишковій флорі з діареєю та колонізацією дріжджів, що вимагатиме припинення грудного вигодовування.
Через розвиток можливої сенсибілізації Ізоцеф слід призначати лише під час лактації, коли користь явно перевищує ризик.
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Ізоцеф не впливає на здатність керувати автомобілем або працювати з механізмами.
04.8 Побічні ефекти
Короткий опис профілю безпеки
У клінічних дослідженнях, які були проведені приблизно у 3000 пацієнтів, найчастіше повідомлялося про побічні ефекти: нудоту (3%), діарею (3%) (див. Розділ 4.4) та головний біль (2%).
У класифікації системних систем побічні ефекти перераховані за такими категоріями частоти: поширені (≥ 1/100,
Таблиця побічних реакцій
У кожній групі частот небажані ефекти представлені у порядку їх зменшення.
* спостерігається з іншими цефалоспоринами і може виникнути при застосуванні Ізоцефу.
Повідомлення про підозрювані побічні реакції.
Повідомлення про підозрювані побічні реакції, що виникають після реєстрації лікарського засобу, є важливими, оскільки вони дозволяють здійснювати постійний моніторинг співвідношення користь / ризик лікарського засобу. Медичних працівників просять повідомляти про будь -які підозрювані побічні реакції через національну систему звітності. "Адреса www. agenziafarmaco.gov.it/it/responsabili.
04.9 Передозування
Токсичних проявів після випадкового передозування Ізоцефу не виявлено.
Може бути показано промивання шлунка, специфічного антидоту немає. Велика кількість ізоцефу може бути виведена з крові за допомогою гемодіалізу. Фактичне видалення за допомогою перитонеального діалізу не встановлено.
У дорослих здорових добровольців, які отримували разові дози до двох грамів ізоцефу, серйозних побічних реакцій не спостерігалося, і всі лабораторні та клінічні дослідження показали нормальні значення.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: Бета-лактамні антибактеріальні засоби. Цефалоспорини. Код ATC: J01DD14
ISOCEF-це напівсинтетичний антибіотик цефалоспоринового ряду.
Цефтибутен має широкий спектр бактерицидної активності щодо грамнегативних та грампозитивних бактерій.
Показано, що цефтибутен має високу активність (низький МІК) проти E. Coli, Klebsiella sp., Proteus, Salmonella spp., Haemophilus influenzae та Streptococcus pyogenes.
Він також активний проти Citrobacter sp., Moraxella (Branhamella) catarrhalis, Morganella morganii, Enterobacter spp., Serratia spp. та Streptococcus pneumoniae.
Сприйнятливі мікроорганізми включають види, які часто беруть участь у інфекціях верхніх і нижніх дихальних шляхів та гострих та ускладнених інфекціях сечовивідних шляхів.
Він не активний проти стафілококів, ентерококів або Pseudomonas spp.
Однак ці організми зазвичай не залучені до запропонованих показань до застосування цефтибутену.
Антибактеріальна активність та механізм дії
Як і у більшості бета-лактамних антибіотиків, бактерицидна активність цефтибутену обумовлена пригніченням синтезу клітинної стінки.
Завдяки своїй хімічній структурі цефтибутен дуже стійкий до дії бета-лактамаз.
Багато мікроорганізмів, що продукують бета-лактамази, стійкі до пеніцилінів або інших цефалоспоринів, можуть бути пригнічені цефтибутеном.
Цефтибутен має високу стійкість до хромосомних цефалоспориназ та опосередкованих плазмідами пеніциліназ, за винятком бета-лактамаз, що продукуються B. fragilis.
Цефтибутен по суті зв'язується з PBP-3 E. Coli, викликаючи дози, що дорівнюють ¼-½ мінімальної інгібуючої концентрації (MIC), до утворення ниткоподібних форм, тоді як лізис спостерігається у дозах, що в 2 рази перевищують MIC .
Мінімальна бактерицидна концентрація (CMB) для Е. Колі чутливий і стійкий до ампіциліну майже дорівнює МІК.
Висока біодоступність у позаклітинних рідинах дозволяє цефтибутен діяти лише на помірно чутливі патогени "in vitro" (див. Фармакокінетику).
Тест на чутливість
Техніка дифузії: лабораторні результати, отримані за допомогою одиночних дисків, що містять 30 мкг цефтибутену, слід інтерпретувати за такими критеріями: діаметр зони ≥21 мм вказує на чутливість; 18-20 мм помірна чутливість; Опір ≤17 мм. Для "Гемофіл зона> 28 мм вказує на чутливість. Ізоляти пневмококу з зоною оксациліну більше 20 мм чутливі до цефтибутену.
Стандартні процедури вимагають використання лабораторних контрольних організмів. Диск 30 мкг повинен давати зону діаметром 29-35 мм для Е.Колі ATCC 25922 і 29-35 мм для "H.influenzae ATCC 9247.
Для всіх тестів слід використовувати диски Цефтибутен 30 мкг в пробірці блоків. Клас дисків (цефалотин), які використовуються для перевірки чутливості до цефалоспорину, не підходить через відмінності в спектрі з цефтибутеном.
Техніка розведення: Мікроорганізми можна вважати чутливими до цефтибутену, якщо МІК ≤ 18 мкг / мл і стійкими, якщо МІК ≥ 32 мкг / мл. Організми з МІК 16 мкг / мл є помірно чутливими.
Як і стандартні методи дифузії, процедури розведення вимагають використання лабораторних контрольних організмів.Стандартний порошок цефтибутену дає значення МІК від 0,125 до 0,5 мкг / мл на літр.Е.Колі ATCC 25922, ≥ 32 мкг / мл для С. Авреус ATCC 29213 і 0,25-1,0 мкг / мл на л "H.influenzae ATCC 49247.
"In vitro" антибактеріальна активність
Цефтибутен проявляє виражену бактерицидну активність; кількість живих бактеріальних клітин різко зменшується при концентраціях, що дорівнюють 50% і більше МІК; при концентраціях, що в 2 рази перевищують смертність від МІК, становить 99,9% без повторного зростання за 24 години.
У здорових добровольців, які отримували дози до 2 г ISOCEF, серйозних побічних ефектів не спостерігалося, і всі лабораторні показники залишалися в межах норми.
05.2 Фармакокінетичні властивості
Пероральні дози добре всмоктуються, досягаючи максимальної концентрації у плазмі крові через 2-3 години.
Середній пік плазми після перорального прийому разової дози 200 мг становить 9,9 мкг / мл (діапазон: 7,7-11,9 мкг / мл); тоді як після введення одноразової пероральної дози 400 мг середній пік плазми становить приблизно 17,0 мкг / мл (діапазон: 9,5-29,9).
При введенні за відсутності їжі абсорбція становить близько 90% дози, що оцінюється на основі відновлення сечі.
Одночасне введення 400 мг капсул ISOCEF з висококалорійною (800 калорій) та багатою на ліпіди їжею уповільнює, але не зменшує всмоктування цефтибутену, тоді як, як показали деякі дослідження, уповільнює та зменшує всмоктування ISOCEF. Підвіска.
Цефтибутен легко проникає в інтерстиціальні рідини, досягаючи концентрацій, подібних до таких у сироватці крові, які зберігаються довше.
Основний метаболіт, транс-цефтибутен, який має антибіотичну активність у 8 разів нижчий, ніж цефтибутен, становить 7,2-9,2% від загальної кількості виведеного препарату.
Цефтибутен виводиться нирками, а 62-68% введеної дози виводиться із сечею у незміненому вигляді.
Нирковий кліренс майже ідентичний загальному кліренсу, що свідчить про те, що цефтибутен виводиться переважно нирками.
Період напіввиведення цефтибутену у здорових добровольців становить приблизно 2-2,3 години. У пацієнтів із помірною нирковою недостатністю (кліренс креатиніну від 30 до 49 мл / хв) середній період напіввиведення з плазми крові подовжується до 7,1 години.
Препарат можна діалізувати як гемодіалізом, так і перитонеальним діалізом у кількості, що дорівнює 65% дози.
05.3 Дані доклінічної безпеки
Цефтибутен проявляє дуже низьку токсичність при введенні лабораторним тваринам у дозах, що в 250–1000 разів перевищують дозу, що використовується у людей.
На відміну від інших цефалоспоринів, цефтибутен не виявляє нефротоксичності при внутрішньовенному введенні. у дозах 1000 мг / кг для кроликів. Цефтибутен має зв'язування з білками близько 80% у мавп, близько 30% у щурів, близько 17% у мишей і близько 65% у людей.
Цефтибутен не виявляє відповідного антигенного потенціалу.
Цефтибутен не виявляє ніякого "дисульфірамоподібного" ефекту у щурів, тоді як він показує дуже низьку гостру та хронічну токсичність у щурів та собак у досліджених дозах (гостра токсичність: щури 5000-10000 мг / кг; собаки 2500-5000 мг / кг ; хронічна токсичність: щур 100-1000 мг / кг; собака 150-600 мг / кг).
Цефтибутен не змінює статевий цикл та репродуктивну здатність як щурів, так і їх потомства.
Цефтибутен не виявляє тератогенного ефекту у щурів до 4000 мг / кг / добу та у кроликів до 40 мг / кг / день, а також не викликає мутагенних ефектів у всіх досліджуваних тестах.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
ISOCEF 200 мг тверді капсули
Мікрокристалічна целюлоза, амідогліколят натрію, стеарат магнію. Компоненти капсул: Желатин, діоксид титану, лаурилсульфат натрію. Компоненти ущільнювальної стрічки: Желатин, полісорбат 80.
ISOCEF 200 мг гранули для пероральної суспензії
Полісорбат 80, симетикон, ксантанова камедь, безводний колоїдний кремнезем, ароматизатор вишні, діоксид титану, бензоат натрію (Е211), сахароза.
ISOCEF 400 мг тверді капсули
Мікрокристалічна целюлоза, амідогліколят натрію, стеарат магнію. Компоненти капсул: Желатин, діоксид титану, лаурилсульфат натрію. Компоненти ущільнювальної стрічки: Желатин, полісорбат 80.
ISOCEF 400 мг гранули для пероральної суспензії
Полісорбат 80, симетикон, ксантанова камедь, безводний колоїдний кремнезем, ароматизатор вишні, діоксид титану, бензоат натрію (Е211), сахароза.
ISOCEF 36 мг / мл гранули для пероральної суспензії
Полісорбат 80, симетикон, ксантанова камедь, діоксид кремнію, аромат вишні, діоксид титану, бензоат натрію (Е211), сахароза.
06.2 Несумісність
Не актуально.
06.3 Строк дії
З неушкодженою упаковкою
Ізоцеф 200 мг тверді капсули 2 роки
Ізоцеф 200 мг гранули для пероральної суспензії 18 місяців
Ізоцеф 400 мг тверді капсули 2 роки
Ізоцеф 400 мг гранули для пероральної суспензії 18 місяців
Ізоцеф 36 мг / мл гранули для пероральної суспензії - флакон 18 місяців
Після розчинення
Відновлена суспензія: 14 днів.
06.4 Особливі умови зберігання
Не зберігати при температурі вище 25 ° C.
06.5 Характер безпосередньої упаковки та вміст упаковки
Ізоцеф 200 мг тверді капсули - 6 твердих капсул у блістері
Ізоцеф 200 мг тверді капсули - 12 твердих капсул у блістері
Ізоцеф 200 мг гранули для пероральної суспензії - 6 пакетиків
Ізоцеф 200 мг гранули для пероральної суспензії - 12 пакетиків
Ізоцеф 400 мг тверді капсули - 4 тверді капсули у блістері
Ізоцеф 400 мг тверді капсули - 6 твердих капсул у блістері
Ізоцеф 400 мг гранули для пероральної суспензії - 4 пакетика
Ізоцеф 400 мг гранули для пероральної суспензії - 6 пакетиків
Ізоцеф 36 мг / мл гранули для пероральної суспензії - 1 флакон
Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження
Капсули: капсули слід ковтати з невеликою кількістю води.
Пакетики: вміст пакетиків слід розвести у невеликій кількості води і негайно випити.
Приготування пероральної суспензії: Струсіть пляшку перед додаванням води, щоб полегшити розсіювання грануляту. Заповніть прикріплений лічильник водою до вигравіруваної на ньому позначки "рівень води". Додайте половину цієї води у пляшку, закрийте її, переверніть догори дном воду, залишену в лічильнику у пляшці, інтенсивно струсіть її, закрийте і енергійно струсіть до тих пір, поки не отримаєте повну дисперсію грануляту. Після розчинення суспензія стабільна протягом 14 днів. Перед кожним введенням суспензію струшують.
15 г гранул, диспергованих у очікуваній кількості води, дають 60 мл суспензії, що містить 36 мг / мл цефтибутену.
ВКАЗІВКИ З ВИКОРИСТАННЯ ДОЗЕРА
Після розчинення суспензії діяти наступним чином:
1) Зніміть кольоровий захисний ковпачок дозатора
2) Вставте дозатор до кінця у пляшку
3) Витягніть підвіску, потягнувши лише за градуйований поршень, до досягнення виїмки, що відповідає вазі дитини.
АДМІНІСТРАТОР 1 раз на день
07.0 ВЛАСНИК РОЗРОБНИЦТВА
RECORDATI Chemical and Pharmaceutical Industries S.p.A. - через Civitali, 1- 20148 Мілан
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
Ізоцеф 200 мг тверді капсули - 6 твердих капсул A.I.C. n. 027850066
Ізоцеф 200 мг тверді капсули - 12 твердих капсул A.I.C. n. 027850167
Ізоцеф 200 мг гранули для пероральної суспензії - 6 пакетиків A.I.C. n. 027850080
Isocef 200 мг гранули для пероральної суспензії-12 пакетиків A.I.C. n. 027850179
Ізоцеф 400 мг тверді капсули - 4 тверді капсули A.I.C. n. 027850078
Ізоцеф 400 мг тверді капсули - 6 твердих капсул A.I.C. n. 027850142
Isocef 400 мг гранули для пероральної суспензії - 4 пакетика A.I.C. n. 027850092
Isocef 400 мг гранули для пероральної суспензії - 6 пакетиків A.I.C. n. 027850155
Isocef36 мг / мл гранули для пероральної суспензії-1 флакон A.I.C. n. 027850104
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
Дата першого дозволу: 03 березня 1992 року
Дата останнього оновлення: 03 березня 2007 року
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
01/12/2015