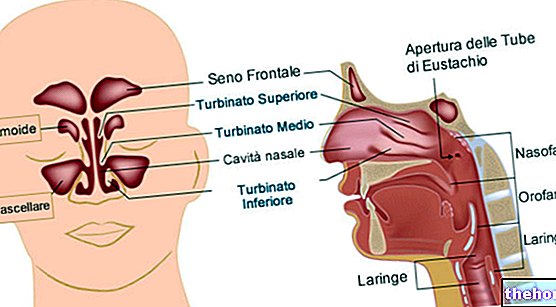
Амінокислоти та білки є проміжними продуктами переходу від світу мінералів до живої речовини.
Як вказує їх назва, амінокислоти є двофункціональними органічними речовинами: складаються з аміно-функції (-NH2) та карбоксильної функції (-COOH); вони можуть бути α, β, γ тощо залежно від положення, яке займає аміногрупа щодо карбоксильної групи:



Біологічно важливі амінокислоти-це всі α-амінокислоти.
Білкові структури складаються з двадцяти амінокислот.
Як видно з загальних структур, показаних вище, усі амінокислоти мають спільну частину та іншу частину, яка їх характеризує (представлені загалом з R).
З двадцяти амінокислот дев’ятнадцять є оптично активними (вони відхиляють площину поляризованого світла).
Більшість амінокислот мають лише одну аміногрупу та один карбоксил, тому їх називають нейтральні амінокислоти; ті, що мають додатковий карбоксил, називаються кислотні амінокислоти тоді як ті, у кого є додаткова аміногрупа, є основні амінокислоти.
Амінокислоти є кристалічними твердими речовинами і мають хорошу розчинність у воді.
Брак деяких амінокислот у раціоні викликає серйозні зміни в розвитку; насправді людський організм не здатний синтезувати деякі амінокислоти, які точно називаються незамінними (їх необхідно вводити разом з дієтою), тоді як він може виробляти сам по собі лише деякі амінокислоти (незамінні).
Однією з хвороб через брак незамінних амінокислот є хвороба, відома під назвою квашиоркор (слово, що походить з африканського діалекту, що в перекладі означає «перша і друга»); ця хвороба вражає первістка, але після народження другої дитини, оскільки у першої дитини не вистачає материнського молока, яке містить правильний запас білків. Тому ця хвороба широко поширена серед людей, які страждають від недоїдання, і включає діарею, відсутність апетиту, що призводить до поступового ослаблення організму.
Як уже згадувалося, природні амінокислоти, за винятком гліцину (це а-амінокислота з воднем замість групи R і є найменшою з двадцяти), мають оптичну активність через наявність принаймні однієї асиметричної вуглецю. У природних амінокислотах абсолютна конфігурація асиметричного вуглецю, на якому пов'язані тільки аміно- та карбоксильні групи, належить до серії L;
D-амінокислоти ніколи не стають частиною структури білка.
Ми пам’ятаємо, що:
ДНК ---- транскрипція → м-РНК ---- трансляція → білок
Транскрипція здатна кодуватися як L-амінокислоти; D-амінокислоти можуть міститися в небілкових структурах (наприклад, у стінці слизової оболонки бактерій: у бактерій немає "генетичної інформації про наявність D-амінокислот для захисної ролі, однак існує" генетична інформація для ферментів які мають справу зі стінкою бактеріальної оболонки).
Повернемося до амінокислот: різна структура групи R визначає індивідуальні особливості кожної амінокислоти і вносить особливий внесок у характеристики білків.
Тому вважалося, що амінокислоти поділяються залежно від природи групи R:
Полярні, але незаряджені амінокислоти:
Гліцин (R = H-)
Серин (R = HO-CH2-)
Треоніністотні
Треонін має два центри симетрії: у природі існує лише 2S, 3R треонін.
Треонін є незамінною амінокислотою (не плутати з незамінною: усі амінокислоти незамінні), тому її слід приймати під час дієти, тобто вживаючи продукти, які її містять, оскільки, як уже згадувалося, генетична спадщина відсутня у клітини людини, здатні виробляти цю амінокислоту (ця спадщина присутня у багатьох рослинах і кращих).
Гідроксильна група серину та треоніну може бути естерифікована фосфорильною групою (одержання фосфосерину та фосфотреоніну), цей процес називається фосфорилювання; фосфорилювання використовується в природі для трансляції сигналів між внутрішнім і зовнішнім елементом клітини.
Цистеїн (R = HS-CH2-)
Сульфгідрил цистеїну легше трансформувати, ніж гідроксил серину: сірка та кисень є шостою групою, але сірка легше окислюється, оскільки має більші розміри.
Тирозин [R = HO- (C6H4) -CH2-]
N.B.
(C6H4) = ді-заміщене бензольне кільце
Як і серин і треонін, гідроксил може бути естерифікований (фосфорильований).Аспарагін (R = NH2-CO-CH2-)
Глютамін (R = NH2-CO-CH2-CH2-)
Неполярні амінокислоти
мають гідрофобні бічні групи; у цьому класі ми виділяємо:
Аліфатика:
Аланін (R = CH3-)
Валін (R = (CH3) 2-CH-) незамінний
Лейцин (R = (CH3) 2-CH-CH2-) незамінний
Ізолейцин (R =
) істотний
Необхідний метіонін (R = CH3-S-CH2-CH2-)
Клітинні мембрани складаються з ліпідного двошару з білками, які закріплені завдяки їх гідрофобному характеру, тому вони містять аланін, валін, ізолейцин та лейцин. З іншого боку, метіонін є амінокислотою, яка майже завжди присутня в невеликій кількості (близько 1%).
Пролін
Ароматичні:
Фенілаланін (R = Ph-CH2-) Ph = феніл: незамінний монозаміщений бензол
Триптофан (R =
істотні
Ці дві амінокислоти, будучи ароматичними, поглинають майже ультрафіолетове випромінювання (близько 300 нм); тому можна використати методику УФ -спектрофотометрії для визначення концентрації відомого білка, що містить ці амінокислоти.
Заряджені амінокислоти
У свою чергу вони поділяються на:
Кислі амінокислоти (з полярними залишками з негативним зарядом при рН 7) є такими, оскільки вони здатні давати позитивний заряд Н +:
Аспарагінова кислота
Глутамінова кислота (R =
)
Ці амінокислоти походять відповідно з аспарагіну та глутаміну; всі чотири існують у природі, і це означає, що c " - це конкретна інформація для кожного з них, тобто c" - базовий триплет у ДНК, що кодує кожну з них.
Основні амінокислоти (з полярними залишками з позитивним зарядом при рН 7) є такими, оскільки вони здатні приймати позитивний заряд Н +:
Лізин (R =
) істотний
Аргінін (R =
)
Гістидин (R =
)
Існують білки, у яких у бічних ланцюгах є похідні амінокислот: наприклад, може бути присутнім фосфосерин (немає генетичної інформації, що кодує фосфосерин, лише серін); фосфосерин - це модифікація посттрансляційний: після того, як відбувся синтез білка
ДНК ---- транскрипція → м-РНК ---- трансляція → білок
такі посттрансляційні модифікації можуть відбуватися на бічних ланцюгах білка.
Дивіться також: Білки, погляд на хімію