Діючі речовини: гідроксикарбамід (гідроксимочевина)
ОНКО КАРБІД 500 мг тверді капсули
Чому використовується Onco Carbide? Для чого це?
ФАРМАКОТЕРАПЕВТИЧНА КАТЕГОРІЯ
Інші протипухлинні засоби
ТЕРАПЕВТИЧНІ ПОКАЗАННЯ
Значні терапевтичні реакції досягаються при застосуванні ОНКО -КАРБІДу при хронічному мієлоїдному лейкозі та інших хронічних мієлопроліферативних синдромах (есенціальна тромбоцитемія, поліцитемія вера та ідіопатичний мієлофіброз). ОНКО КАРБІД також показаний для лікування пацієнтів, які страждають на гомозиготну серповидноклітинну анемію.
Протипоказання, коли не слід застосовувати Онкокарбід
Відома гіперчутливість до активної речовини або до будь -якої з допоміжних речовин.
Важка депресія кісткового мозку: лейкопенія (з кількістю лейкоцитів менше 2500 / мм3), тромбоцитопенія (з кількістю тромбоцитів менше 100000 / мм3) або тяжка анемія. Вагітність та годування груддю. Вакцина проти жовтої лихоманки.
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Onco Carbide
ОНКО КАРБІД слід з обережністю застосовувати пацієнтам, які раніше опромінювалися або проходили антибластну терапію, тобто з протипухлинними препаратами, а також особам з тяжкою нирковою недостатністю. У осіб, які вже опромінені, може спостерігатися «загострення» опромінюючої еритеми.
ОНКО КАРБІД слід з обережністю призначати пацієнтам з важкими захворюваннями печінки. Перед початком терапії ОНКО КАРБІДу будь -яку важку анемію слід усунути шляхом переливання цільної крові.
Ретельне гематологічне спостереження під час лікування з контролем гемоглобіну, лейкоцитів та тромбоцитів. Лікування слід припинити, якщо лейкоцити падають нижче 2500 / мм3 або тромбоцити нижче 100000 / мм3, щоб відновити їх лише після того, як ці параметри повернуться до нормальних значень.
З обережністю застосовувати пацієнтам, які проходять курс лікування або вже проходили лікування протипухлинними препаратами або променевою терапією щодо можливого виникнення депресії кісткового мозку.
Пацієнти літнього віку більш чутливі до ONCO CARBIDE і вимагають менших доз.
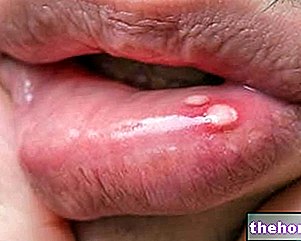
Тривале лікування гідроксимочевиною пов'язане з появою шкірних та ротових реакцій. Більшість з них, такі як пігментація нігтів, шкіри та ротової порожнини, ксероз шкіри, виразка у роті та іхтіоз, є прийнятними і не потребують припинення лікування. Виразки на шкірі є рідкісними проявами, але мають ефект. хронічні мієлопроліферативні синдроми, а в деяких випадках вимагають тимчасового або постійного припинення терапії. Виразки на шкірі часто розташовуються біля крижових кісток або на ногах, болючі і іноді переходять у некроз. Вони виникають частіше. у літніх людей або у жінок. в літературі спостерігалися у пацієнтів, які отримували дозу більше 1 г на добу протягом щонайменше 1 року.
Патогенез шкірних виразок ще належить визначити, навіть якщо вважається, що препарат пошкоджує базальний шар епідермісу. Відміна гідроксимочевини зазвичай призводить до повного загоєння та полегшення болю.
Взаємодії Які ліки або продукти харчування можуть змінити дію онкокарбіду
Повідомте свого лікаря або фармацевта, якщо ви нещодавно приймали інші ліки, навіть ті, що відпускаються без рецепта.
Немає даних про потенціал взаємодії гідроксисечовини з іншими препаратами.
Багаторічний клінічний досвід показує, що гідроксимочевина не має високого потенціалу взаємодії.
Одночасне застосування з іншими мієлосупресивними препаратами або променева терапія може збільшити ризик депресії кісткового мозку або інших побічних явищ.
Уникайте одночасного застосування ослаблених вірусних вакцин, імуносупресивної терапії. Уникайте одночасного застосування інгібіторів зворотної транскриптази, аналогів нуклеозидів. Ризик васкуліту при одночасному або попередньому застосуванні інтерферону. Уникайте одночасного застосування інактивованих вакцин (поліомієліт), застосування циклоспорину та такролімусу.
Попередження Важливо знати, що:
Продукт, як і більшість протипухлинних препаратів, виявив канцерогенні властивості у тварин за певних умов експерименту.
Фертильність, вагітність та годування груддю
Попросіть поради у свого лікаря або фармацевта, перш ніж приймати будь -які ліки.
Вагітність: Препарати, що впливають на синтез ДНК, такі як гідроксимочевина, потенційно мутагенні. Дослідження на тваринах показали репродуктивну токсичність. Гідроксимочевина проникає через плаценту. Застосування препарату під час вагітності протипоказане.Однак якщо цей препарат застосовується під час вагітності, пацієнтка повинна бути поінформована про потенційний ризик для плода.Жінки репродуктивного віку повинні використовувати методи контрацепції.
Грудне вигодовування: Гідроксисечовина виділяється з грудним молоком. Під час застосування ОНКО КАРБІДу годування груддю слід припинити.
Вплив на здатність керувати автомобілем та працювати з механізмами
Досліджень щодо здатності керувати автомобілем та працювати з механізмами не проводилося.
Важлива інформація про деякі інгредієнти
У разі виявлення непереносимості цукру перед застосуванням ліків зверніться до лікаря.
Доза, спосіб та час введення Як використовувати онкокарбід: дозування
При хронічному мієлоїдному лейкозі рекомендується безперервна терапія в дозі 20-30 мг / кг перорально в одноразовій добовій дозі. Шість тижнів лікування є достатнім періодом для визначення ефективності ONCO CARBIDE.
Якщо є клінічні ознаки сприятливого ефекту, терапію слід продовжувати невизначено довго. При серповидно-клітинній анемії рекомендується безперервна терапія в дозі 15-30 мг / кг / добу перорально за один або два щоденних введення. У цих пацієнтів для визначення ефективності ОНКО КАРБІДу потрібно щонайменше 6-8 місяців безперервного лікування.
У всіх випадках дозу ОНКО КАРБІДу лікар повинен відкоригувати на основі бажаного клінічного ефекту та виявлених гематологічних побічних ефектів. Лікування слід припинити, якщо лейкоцити знизяться до менш ніж 2500 / мм3 або тромбоцити до менше 100000 У цих випадках підрахунок повторюють через три дні, і якщо він має тенденцію до зростання до нормальних значень, терапію відновлюють, можливо, зменшуючи дозу.
При солідних пухлинах можна застосовувати пероральну терапію 80 мг / кг в одноразовій добовій дозі.
Схема періодичного дозування пропонує перевагу особливо низької токсичності; ця схема також використовується в поєднанні з променевою терапією.
Передозування Що робити, якщо ви прийняли занадто багато Onco Carbide
Гідроксимочевина є цитостатичним засобом.У разі, якщо небажані ефекти є клінічно значущими, тимчасово припиніть лікування, перевірте гематологічні показники та за необхідності відновіть нормальні показники за допомогою переливання крові.
У разі випадкового проковтування / прийому надмірної дози ONCO CARBIDE негайно повідомте про це свого лікаря або зверніться до найближчої лікарні. Якщо у вас є запитання щодо застосування ОНКО КАРБІДУ, зверніться до свого лікаря або фармацевта.
Побічні ефекти Які побічні ефекти від онкокарбіду
Як і всі ліки, ОНКО КАРБІД може викликати побічні ефекти, хоча вони виникають не у всіх.
Основним побічним ефектом у разі терапії ОНКО КАРБІДОМ є депресія кісткового мозку, яка проявляється лейкопенією, анемією, а іноді і тромбоцитопенією. Рідше зустрічаються такі симптоми шлунково -кишкового тракту, як стоматит, анорексія, нудота, блювота, діарея та запор.
Рідко можуть виникати дизурія, алопеція та олігоспермія; азооспермія (відсутність сперматозоїдів) та олігоспермія (наявність невеликої кількості сперматозоїдів) зазвичай оборотні. Як і при застосуванні інших антимітотичних препаратів, виключно повідомлялося про аменорею (зникнення менструації). Повідомлялося про лихоманку. Повідомлялося про рідкісні випадки гострого інтерстиціального захворювання легенів та фіброзу легенів. Вторинний лейкоз може розвинутися у пацієнтів, які проходять тривале лікування гідроксимочевиною для мієлопроліферативних захворювань, таких як поліцитемія вера та тромбоцитоз
Під час тривалого лікування високими дозами рідко повідомлялося про виразки шкіри на ногах, які можуть бути оборотними після припинення лікування. Дерматологічні реакції, такі як макулопапульозний висип та еритема обличчя, свербіж, гіперпігментація, меланоніхія (пошкодження, що зачіпають нігті чорного кольору), суха шкіра, атрофія шкірно-нігтьового покриву, лущення шкіри, ураження шкіри та симільдерматоміозит (еритематозні або еритематозні ураження) дотримуватися -десквамативна).
Повідомлялося про рідкісні випадки злоякісних пухлин шкіри: базально -клітинний і плоскоклітинний рак.
У неврологічній сфері рідко описувалися головний біль, запаморочення, дезорієнтація, галюцинації та судоми. Функція ниркових канальців може бути тимчасово порушена з послідовним збільшенням сечовини в крові, ККД та креатиніну. У деяких випадках спостерігалося «аномальне зміна показників печінки.
Тимчасове переривання ONCO CARBIDE зазвичай подолає вищезгадані порушення. Дотримання вказівок, що містяться в листівці, знижує ризик небажаних наслідків.
Повідомлення про побічні ефекти
Якщо у Вас виникли будь -які побічні ефекти, зверніться до лікаря або фармацевта, що включає будь -які можливі побічні ефекти, не зазначені у цій інструкції. Про побічні ефекти також можна повідомляти безпосередньо через національну систему звітності "www.agenziafarmaco.gov.it/it/responsabili". Повідомляючи про побічні ефекти, ви можете допомогти надати більше інформації про безпеку застосування цього ліки.
Термін придатності та утримання
Термін придатності: див. Термін придатності, зазначений на упаковці.
Термін придатності відноситься до продукту в недоторканій упаковці, правильно зберігається.
УВАГА: НЕ ВИКОРИСТОВУВАЙТЕ ЛІКАРСТВЕННИЙ ПРОДУКТ ПІСЛЯ ДАТИ ГОДНОСТІ, ВЗНАЧЕНОЇ НА УПАКОВКІ
Зберігати при температурі не вище 25 ° С
Ліки не слід утилізувати через стічні води або побутові відходи. Запитайте у фармацевта, як утилізувати ліки, які ви більше не використовуєте. Це допоможе захистити довкілля.
ЗБЕРЕЖІТЬ ЛЕКАРСТВЕННИЙ ПРОДУКТ ДОСТУПНО ДОСТУПУ ТА ПОГЛЯДУ ДІТЕЙ
Склад та лікарська форма
СКЛАД
Одна капсула містить: Діюча речовина: гідроксикарбамід (гідроксимочевина) 500 мг. Допоміжні речовини: лактоза; цитрат кальцію; двоосновний цитрат натрію; стеарат магнію.Компоненти капсули, що містить: желатин; діоксид титану (Е171); оксид заліза (Е172).
ФАРМАЦЕВТИЧНА ФОРМА І ЗМІСТ
Тверді капсули. Упаковка, що містить 20 капсул по 500 мг, упакована у блістери.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
ОНКО КАРБІД
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Одна капсула містить:
Діючий принцип: гідроксимочевина 500 мг.
Допоміжні речовини: лактози.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Тверда капсула для перорального застосування.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Значні терапевтичні реакції досягаються при застосуванні ОНКО -КАРБІДу при хронічному мієлоїдному лейкозі та інших хронічних мієлопроліферативних синдромах (есенціальна тромбоцитемія, поліцитемія вера та ідіопатичний мієлофіброз). ОНКО КАРБІД також показаний для лікування пацієнтів, які страждають на гомозиготну серповидноклітинну анемію.
04.2 Дозування та спосіб введення
При хронічному мієлоїдному лейкозі та інших хронічних мієлопроліферативних синдромах (есенціальна тромбоцитемія, поліцитемія вера та ідіопатичний мієлофіброз) рекомендується безперервна терапія у дозі 20-30 мг / кг / добу перорально за один або два щоденних введення. Шість тижнів лікування є достатнім періодом для визначення ефективності ONCO CARBIDE.
Якщо є клінічні ознаки сприятливого ефекту, терапію слід продовжувати невизначено довго.
При серповидно-клітинній анемії рекомендується безперервна терапія в дозі 15-30 мг / кг / добу перорально за один або два щоденних введення. У цих пацієнтів для визначення ефективності ОНКО КАРБІДу потрібно щонайменше 6-8 місяців безперервного лікування.
У всіх випадках дозу ОНКО КАРБІДу лікар повинен відкоригувати на основі бажаного клінічного ефекту та виявлених гематологічних побічних ефектів. Лікування слід припинити, якщо лейкоцити знизяться до менш ніж 2500 / мм3 або тромбоцити до менше 100000 У цих випадках підрахунок повторюють через три дні, і якщо він має тенденцію до зростання до нормальних значень, терапію відновлюють, можливо, зменшуючи дозу.
При солідних пухлинах можна застосовувати пероральну терапію 80 мг / кг в одноразовій добовій дозі.
Схема періодичного дозування пропонує перевагу особливо низької токсичності; ця схема також використовується в поєднанні з променевою терапією.
04.3 Протипоказання
Відома гіперчутливість до активної речовини або до будь -якої з допоміжних речовин.
Важка депресія кісткового мозку: лейкопенія (з кількістю лейкоцитів менше 2500 / мм3), тромбоцитопенія (з кількістю тромбоцитів менше 100000 / мм3) або тяжка анемія. Вагітність та годування груддю.
Вакцина проти жовтої лихоманки.
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
ОНКО КАРБІД слід з обережністю застосовувати пацієнтам, які раніше опромінювалися або проходили антибластну терапію, а також особам з тяжкою нирковою недостатністю. У осіб, які вже опромінені, може спостерігатися «загострення» опромінюючої еритеми.
ОНКО КАРБІД слід з обережністю призначати пацієнтам з важкими захворюваннями печінки.
Будьте обережні у пацієнтів, які проходять лікування або вже проходили лікування протипухлинними або променевою терапією щодо можливого виникнення депресії кісткового мозку.
Перед початком терапії ОНКО КАРБІДу будь -яку важку анемію слід усунути шляхом переливання цільної крові.
Ретельне гематологічне спостереження під час лікування з контролем гемоглобіну, лейкоцитів та тромбоцитів. Лікування слід припинити, якщо лейкоцити падають нижче 2500 / мм3 або тромбоцити нижче 100000 / мм3, щоб відновити їх лише після того, як ці параметри повернуться до нормальних значень.
Пацієнти літнього віку більш чутливі до ONCO CARBIDE і вимагають менших доз.
Продукт, як і більшість протипухлинних препаратів, виявив канцерогенні властивості у тварин за певних умов експерименту.
Тривале лікування гідроксимочевиною пов'язане з появою шкірних та ротових реакцій. Більшість з них, такі як пігментація нігтів, шкіри та ротової порожнини, ксероз шкіри, виразка у роті та іхтіоз, є прийнятними і не потребують припинення лікування. Виразки на шкірі є рідкісними проявами, але мають ефект. Значний побічний ефект препарату. Вони з’являються у пацієнтів із хронічні мієлопроліферативні синдроми і в деяких випадках вимагають тимчасового або постійного припинення терапії. Виразки на шкірі часто розташовуються біля щиколоток або на ногах, болючі і іноді переходять у некроз. Вони виникають частіше. у літніх людей або у жінок. Більшість випадків повідомлені в літературі, спостерігалися у пацієнтів, які отримували дозу, що перевищує 1 г на добу протягом щонайменше 1 року. Патогенез виразок на шкірі ще належить визначити, навіть якщо вважається, що препарат пошкоджує базальний шар епідермісу.
Виведення гідроксимочевини зазвичай призводить до повного загоєння та полегшення болю.
Важлива інформація про деякі інгредієнти
Цей препарат містить лактозу: Пацієнтам з рідкісними спадковими проблемами непереносимості галактози, дефіцитом лактази Лаппа або порушенням всмоктування глюкози-галактози не слід приймати цей препарат.
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Немає даних про потенціал взаємодії гідроксисечовини з іншими препаратами.
Багаторічний клінічний досвід показує, що гідроксимочевина не має високого потенціалу взаємодії.
Одночасне застосування з іншими мієлосупресивними препаратами або променева терапія може збільшити ризик депресії кісткового мозку або інших побічних явищ.
Уникайте одночасного застосування ослаблених вірусних вакцин, імуносупресивної терапії. Уникайте одночасного застосування інгібіторів зворотної транскриптази, аналогів нуклеозидів. Ризик васкуліту при одночасному або попередньому застосуванні інтерферону. Уникайте одночасного застосування інактивованих вакцин (поліомієліт), застосування циклоспорину та такролімусу.
04.6 Вагітність та лактація
Вагітність: препарати, що впливають на синтез ДНК, такі як гідроксимочевина, потенційно мутагенні. Дослідження на тваринах показали репродуктивну токсичність. Гідроксимочевина проникає через плаценту.
Застосування препарату під час вагітності, як правило, протипоказано. Однак якщо цей препарат застосовується під час вагітності, пацієнтка повинна бути поінформована про потенційний ризик для плода.
Жінки дітородного віку повинні користуватися методами контрацепції.
Час годування: Гідроксимочевина виводиться з грудним молоком. Грудне вигодовування слід припинити під час застосування ОНКО КАРБІДУ.
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Досліджень щодо здатності керувати автомобілем та працювати з механізмами не проводилося.
Не існує припущень або доказів того, що препарат може змінити увагу та час реакції.
04.8 Побічні ефекти
Основним побічним ефектом у разі терапії ОНКО КАРБІДОМ є депресія кісткового мозку, яка проявляється лейкопенією, анемією, а іноді і тромбоцитопенією. Рідше зустрічаються такі симптоми шлунково -кишкового тракту, як стоматит, анорексія, нудота, блювота, діарея та запор. Рідко можуть виникати дизурія, алопеція та олігоспермія; азооспермія та олігоспермія зазвичай оборотні. Як і при застосуванні інших антимітотичних препаратів, виключно повідомлялося про аменорею.
Повідомлялося про лихоманку.
Повідомлялося про рідкісні випадки гострого інтерстиціального захворювання легенів та фіброзу легенів.
Вторинний лейкоз може розвинутися у пацієнтів, які проходять тривале лікування гідроксимочевиною для мієлопроліферативних захворювань, таких як поліцитемія вера та тромбоцитоз
Під час тривалого лікування високими дозами рідко повідомлялося про виразки шкіри на ногах, які можуть бути оборотними після припинення лікування.
Також можуть спостерігатися дерматологічні реакції, такі як висип на плямі, еритема обличчя, свербіж, гіперпігментація, меланоніхія, сухість шкіри, атрофія шкірно-нігтьового покриву, лущення шкіри, ураження шкіри, подібні до дерматоміозиту.
Повідомлялося про рідкісні випадки злоякісних пухлин шкіри: базально -клітинний і плоскоклітинний рак
У неврологічній сфері рідко описувалися головний біль, запаморочення, дезорієнтація, галюцинації та судоми. Функція ниркових канальців може бути тимчасово порушена з послідовним збільшенням сечовини в крові, ККД та креатиніну. У деяких випадках спостерігалося «аномальне зміна показників печінки.
Тимчасове переривання ONCO CARBIDE зазвичай подолає вищезгадані порушення.
Повідомлення про підозрювані побічні реакції
Повідомлення про підозрювані побічні реакції, що виникають після реєстрації лікарського засобу, є важливим, оскільки воно дозволяє здійснювати постійний моніторинг співвідношення користь / ризик лікарського засобу. Медичних працівників просять повідомляти про будь -які підозрювані побічні реакції через національну систему звітності. "Адреса www. agenziafarmaco.gov.it/it/responsabili.
04.9 Передозування
Гідроксимочевина є цитостатичним засобом.У разі, якщо небажані ефекти є клінічно значущими, тимчасово припиніть лікування, перевірте гематологічні показники та за необхідності відновіть нормальні показники за допомогою переливання крові.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Категорія лікарського засобу: інші протипухлинні засоби.
ATC: L01XX05.
ONCO CARBIDE (Hydroxyurea) - препарат з протипухлинною дією, доступний для перорального застосування. Специфічний механізм дії гідроксисечовини до кінця не відомий. Однак вважається, що препарат викликає негайне пригнічення синтезу ДНК, діючи як інгібітор рибонуклеотидредуктази. без втручання в синтез РНК або білка.
При "серповидноклітинній анемії" гідроксимочевина викликає збільшення концентрації фетального гемоглобіну (HbF). " У клінічних дослідженнях із застосуванням гідроксимочевини відзначалося значне збільшення HbF від вихідного рівня.
05.2 Фармакокінетичні властивості
Гідроксимочевина добре всмоктується з шлунково-кишкового тракту. Пікові рівні в плазмі спостерігаються приблизно через 2 години після перорального прийому. Період напіввиведення з плазми становить близько 2 годин. Близько 80% препарату метаболізується до сечовини на рівні печінки та виводиться з організму в сечі протягом 12 годин.
Гідроксимочевина досягає помітних концентрацій у центральній нервовій системі.
05.3 Дані доклінічної безпеки
Одноразову пероральну токсичність досліджували на щурах та мишах. LD50 дорівнював 7330 мг / кг у миші та 5780 мг / кг у щура. Дослідження токсичності при повторних дозах (підгострий та хронічний) у щурів, собак та мавп виявили дозозалежну гіпоплазію кісткового мозку легкої та помірної інтенсивності; лише при більш високих дозах, що перевищують клінічну, спостерігалася атрофія яєчок з блокуванням сперматогенезу, втрата ваги, серцево -судинні ефекти та гематологічні зміни.
Гідроксимочевина є цитостатичним препаратом, і через її механізм дії, спільний з іншими протипухлинними препаратами, можна уявити, що вона може мати потенційний вплив на репродукцію, мутагенез, тератогенез та канцерогенез.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Лактоза; цитрат кальцію; двоосновний цитрат натрію; стеарат магнію.
06.2 Несумісність
Невідомо.
06.3 Строк дії
5 років, в цілій упаковці.
06.4 Особливі умови зберігання
Зберігати при температурі не вище 25 ° С.
06.5 Характер негайної упаковки та вміст упаковки
Блистерний термоізоляційний блистер з ПВХ / PVDC, запаяний алюмінієвою фольгою / PVDC.
Коробка з 20 твердих капсул по 500 мг.
06.6 Інструкції з використання та поводження
ОНКО КАРБІД - лікарський засіб, з яким потрібно поводитися обережно. Люди, які не приймають ОНКО КАРБІД, особливо вагітні жінки, не повинні контактувати з препаратом. Якщо вам потрібно поводитися з капсулами, слід надіти одноразові рукавички і вимити руки до і після роботи з капсулами. У разі відкриття капсули надлишок порошку необхідно видалити за допомогою абсорбуючого паперу, який буде закритий у закритий поліетиленовий пакет, щоб утилізувати відповідно до місцевих процедур утилізації ліків.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
TEOFARMA S.r.l. через F.lli Cervi, 8 - 27010 Valle Salimbene (PV)
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
A.I.C.: 021510019
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
1970 - 2010
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
Березень 2015 року