Діючі речовини: Толтеродіна
Детрузитол 1 мг і 2 мг таблетки, вкриті оболонкою
Доступні вставки для упаковки Детрузитол для розмірів упаковки:- Детрузитол 1 мг і 2 мг таблетки, вкриті оболонкою
- Детрузитол ретард 2 мг і 4 мг тверді капсули з пролонгованим вивільненням
Чому використовується Детрузитол? Для чого це?
Діючою речовиною Детрузитолу є толтеродин. Толтеродин належить до класу ліків, які називаються антимускаринами.
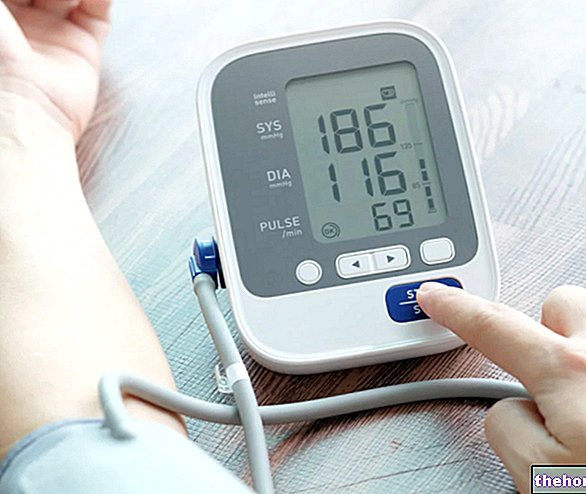
Детрузитол використовується для симптоматичного лікування синдрому гіперактивної сечового міхура. Якщо ви страждаєте від синдрому гіперактивного сечового міхура, ви помітите нездатність контролювати сечовипускання, необхідність часто поспішати в туалет без будь -яких попереджувальних знаків.
Протипоказання Коли не слід застосовувати Детрузитол
Не приймайте Детрузитол
- Якщо у вас алергія (гіперчутливість) на толтеродин або будь -який інший інгредієнт препарату
- Якщо вам важко виводити сечу з сечового міхура (затримка сечі)
- Якщо у вас неконтрольована вузькокутова глаукома (високий очний тиск із втратою зору, не лікується належним чином)
- Якщо ви страждаєте на міастенію (надмірна м’язова слабкість)
- Якщо у вас важкий виразковий коліт (виразка та запалення товстої кишки)
- Якщо у вас токсичний мегаколон (гостре розширення товстої кишки)
Заходи безпеки при застосуванні Що потрібно знати перед прийомом Детрузитолу
Будьте особливо обережні з Детрузитолом
- Якщо у вас утруднене сечовипускання та / або поганий відтік сечі
- Якщо у вас є шлунково -кишкові розлади, які впливають на проходження та / або перетравлення їжі.
- Якщо у вас проблеми з нирками (ниркова недостатність)
- Якщо у вас проблеми з печінкою
- Якщо у вас є нервові захворювання, які впливають на артеріальний тиск, кишечник або статеву функцію (будь -яка нейропатія вегетативної нервової системи).
- Якщо у вас є грижа діафрагми (грижа органу черевної порожнини)
- Якщо ви страждаєте від зниження перистальтики кишечника або страждаєте від сильного запору (зниження перистальтики шлунково-кишкового тракту)
- Якщо у вас є проблеми з серцем, такі як:
- Змінене відстеження серця (ЕКГ)
- Повільне серцебиття (брадикардія)
- Важливі попередні захворювання серця, такі як:
- кардіоміопатія (ослаблення серцевого м’яза)
- ішемія міокарда (зниження припливу крові до серця),
- аритмія (нерегулярне серцебиття)
- серцева недостатність
- Якщо у вас особливо низький рівень калію (гіпокаліємія), кальцію (гіпокальціємія) або магнію (гіпомагніємія) у крові.
Якщо що -небудь із зазначеного стосується вас, будь ласка, повідомте свого лікаря або фармацевта перед початком лікування.
Взаємодії Які препарати або продукти харчування можуть змінити дію Детрузитолу
Толтеродин, активний інгредієнт Детрузитолу, може взаємодіяти з іншими ліками.
Не рекомендується використовувати толтеродин з:
- деякі антибіотики (містять, наприклад, еритроміцин, кларитроміцин);
- ліки для лікування грибкових інфекцій (наприклад, кетоконазол, ітраконазол);
- ліки, що використовуються для лікування ВІЛ.
Детрузитол слід застосовувати з обережністю при одночасному застосуванні з:
- ліки, що впливають на проходження їжі (містять, наприклад, метоклопрамід та цизаприд)
- ліки для лікування нерегулярного серцебиття (містять, наприклад, аміодарон, соталол, хінідин, прокаїнамід)
- інші лікарські засоби з механізмом дії, подібним до Детрузитолу (антимускаринові властивості) або ліки з механізмом дії, протилежним Детрузитолу (холінергічні властивості). Якщо у вас виникнуть додаткові запитання, зверніться до лікаря.
Скажіть своєму лікарю, якщо ви приймаєте або нещодавно приймали інші ліки, навіть ті, для яких вам не потрібен рецепт лікаря.
Прийом Детрузитолу з їжею та напоями
Детрузитол можна приймати до, після або під час їжі.
Попередження Важливо знати, що:
Вагітність та годування груддю
Вагітність
Детрузитол не слід приймати під час вагітності. Негайно зверніться до лікаря, якщо ви вагітні, якщо ви думаєте, що вагітні або плануєте завагітніти.
Час годування
Немає даних про виведення толтеродину у жіноче молоко.
Грудне вигодовування не рекомендується під час введення Детрузитолу.
Порадьтеся з вашим лікарем або фармацевтом, перш ніж приймати будь -які ліки.
Водіння автомобіля та роботу з машинами
Детрузитол може викликати запаморочення, втому або погіршити зір. Здатність керувати автомобілем або працювати з механізмами може бути порушена.
Дозування та спосіб застосування Як застосовувати Детрузитол: Дозування
Дозування
Завжди приймайте Детрузитол точно так, як вам сказав ваш лікар. Якщо ви не впевнені, поговоріть зі своїм лікарем або фармацевтом.
Звичайна доза становить одну таблетку 2 мг двічі на день, за винятком пацієнтів, які мають проблеми з нирками та печінкою або мають побічні ефекти, для яких лікар може зменшити дозу до однієї таблетки 1 мг двічі на день.
Детрузитол не рекомендується дітям.
Таблетки призначені для перорального застосування і їх слід ковтати цілими.
Тривалість лікування
Ваш лікар скаже вам, як довго слід застосовувати Детрузитол. Не припиняйте лікування раніше, ніж очікувалося, оскільки ви не побачите негайного ефекту. Налагодження сечового міхура займе деякий час. Пройдіть курс лікування таблетками, призначеними лікарем. Якщо до цієї дати ви не помітили жодного ефекту, зверніться до лікаря.
Переваги лікування слід переоцінити через 2–3 місяці.
Завжди звертайтесь до лікаря, якщо ви думаєте про припинення лікування.
Якщо ви забули прийняти Детрузитол
Якщо ви забули прийняти дозу у звичайний час, ви можете прийняти її, як тільки згадаєте, якщо це не надто близько до часу для вашої наступної дози.
Не приймайте подвійну дозу, щоб компенсувати пропущену дозу.
Якщо у вас виникнуть додаткові запитання щодо застосування цього продукту, зверніться до лікаря або фармацевта.
Передозування Що робити, якщо ви прийняли занадто багато Детрузитолу
Якщо ви або хтось інший прийняв занадто багато таблеток, негайно зверніться до лікаря або фармацевта.
Побічні ефекти Які побічні ефекти у Детрузитолу
Як і всі ліки, Детрузитол може викликати побічні ефекти, хоча вони виникають не у всіх.
Негайно зверніться до лікаря або до відділення швидкої допомоги, якщо у вас виникнуть симптоми ангіоневротичного набряку, такі як:
- набряк обличчя, язика або глотки
- труднощі при ковтанні
- кропив’янка і утруднене дихання
Вам також слід звернутися до лікаря у разі реакцій гіперчутливості (наприклад, свербіж, висип, кропив’янка, утруднене дихання). Це трапляється нечасто (зустрічається менш ніж у 1 з 100 пацієнтів).
Зверніться до лікаря або негайно зверніться до відділення невідкладної допомоги, якщо ви помітили будь -який з таких симптомів:
- біль у грудях, утруднене дихання або схильність до легкого стомлення (навіть у стані спокою), утруднене дихання вночі, набряк ніг.
Це можуть бути симптоми серцевої недостатності. Це трапляється нечасто (зустрічається менш ніж у 1 з 100 пацієнтів).
Під час лікування Детрузитолом повідомлялося про такі побічні ефекти з такою частотою:
Дуже поширені побічні ефекти (виникають більш ніж у 1 з 10 пацієнтів):
- Сухість у роті
- Головний біль
Поширені побічні ефекти (виникають менш ніж у 1 з 10 пацієнтів):
- Бронхіт
- Запаморочення, сонливість, відчуття поколювання в руках і ногах
- Сухі очі, погіршення зору
- Запаморочення
- Серцебиття
- Утруднення травлення (диспепсія), запор, біль у животі, надмірна кількість повітря або газу в шлунку або кишечнику, блювота
- Сухість шкіри
- Хворобливе або утруднене сечовипускання, неможливість спорожнити сечовий міхур
- Втома, біль у грудях, надлишок рідини в організмі, що викликає набряк (наприклад, щиколотки)
- Збільшення ваги
- Діарея
Нечасті побічні ефекти (зустрічаються менше ніж у 1 пацієнта з 100):
- Алергічні реакції
- Нервозність
- Збільшення частоти серцевих скорочень, серцева недостатність, нерегулярне серцебиття
- Біль у животі
- Порушення пам’яті
Інші повідомлені реакції включають важкі алергічні реакції, сплутаність свідомості, галюцинації, почервоніння шкіри, ангіоневротичний набряк та дезорієнтацію. Повідомлялося також про погіршення симптомів деменції у пацієнтів, які проходять курс лікування деменції.
Якщо будь -який з побічних ефектів стає серйозним, або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта.
Повідомлення про побічні ефекти
Якщо у Вас виникли будь -які побічні ефекти, зверніться до лікаря або фармацевта, що включає будь -які можливі побічні ефекти, не зазначені у цій інструкції. Про побічні ефекти також можна повідомляти безпосередньо через національну систему звітності за адресою www.agenziafarmaco.gov.it/it/responsabili. Повідомляючи про побічні ефекти, ви можете допомогти надати більше інформації про безпеку застосування цього препарату.
Термін придатності та утримання
Зберігати в недоступному для дітей місці.
Не використовуйте Детрузитол після закінчення терміну придатності, зазначеного на упаковці. Термін придатності відноситься до останнього дня місяця.
Особливих запобіжних заходів щодо зберігання немає.
Ліки не слід утилізувати через стічні води або побутові відходи. Запитайте у фармацевта, як викидати ліки, якими ви більше не користуєтесь. Це допоможе захистити навколишнє середовище.
Дедлайн »> Інша інформація
Що містить Детрузитол
Діюча речовина - толтеродин тартрат.
Кожна таблетка Детрузитолу 1 мг містить 1 мг толтеродин тартрату, що відповідає 0,68 мг толтеродину
Кожна таблетка Детрузитолу 2 мг містить 2 мг толтеродин тартрату, що відповідає 1,37 мг толтеродину
Допоміжними речовинами є:
- Ядро: целюлоза мікрокристалічна, кальцій двоосновний фосфат дигідрат натрію крохмальгліколят (тип В) магнію стеарат кремнезем, безводний колоїдний
- Покривна плівка: Гіпромелоза Мікрокристалічна целюлоза Стеаринова кислота Діоксид титану (E171)
Як виглядає Детрузитол та вміст упаковки
Таблетки Детрузитолу 1 мг - білі, круглі, двоопуклі, з нанесеними позначками вище і нижче літер "TO".
Таблетки Детрузитолу 2 мг - білі, круглі, двоопуклі, з нанесеними позначками вище та нижче літер "DT".
Таблетки Детрузитол 1 мг та 2 мг випускаються в наступних розмірах упаковки:
Пухирі, що містять:
- 20 таблеток (2 х 10)
- 30 таблеток (3 х 10)
- 50 таблеток (5 х 10)
- 100 таблеток (10 х 10)
- 14 таблеток (1 х 14)
- 28 таблеток (2 х 14)
- 56 таблеток (4 х 14)
- 280 таблеток
- 560 таблеток
Пляшки, що містять 60 або 500 таблеток.
Не всі розміри упаковок можна продавати.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ -
ДЕТРУЗИТОЛЬНІ ПЛАСТИНИ, ПОВЕРХНІ ПЛЕНКОЮ
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД -
Кожна таблетка, вкрита плівковою оболонкою, містить: толтеродин тартрату 1 мг або 2 мг, що відповідає 0,68 мг і 1,37 мг толтеродину.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА -
Таблетки, вкриті плівковою оболонкою.
Таблетки, вкриті плівковою оболонкою, білого кольору, круглі та двоопуклі.
Таблетка 1 мг має надрізи вище і нижче літер TO, а таблетка 2 мг має виїмки вище і нижче літер DT.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ -
04.1 Терапевтичні показання -
Симптоматичне лікування термінового нетримання сечі та / або збільшення частоти сечовипускання та терміновості у пацієнтів із синдромом гіперактивного сечового міхура.
04.2 Дозування та спосіб введення -
Дорослі (включаючи літніх пацієнтів) :
Рекомендована доза становить 2 мг двічі на день, за винятком пацієнтів з печінковою недостатністю або тяжкою нирковою недостатністю [ШКФ (кліренс інуліну)
Через 2-3 місяці слід повторно оцінити ефект лікування (див. Розділ 5.1).
Педіатричні пацієнти :
Ефективність Детрузитолу у дітей не доведена (див. Розділ 5.1).
04.3 Протипоказання -
Толтеродин протипоказаний пацієнтам з:
- Затримка сечі
- неконтрольована вузькокутова глаукома
- Міастенія гравіс
- Відома гіперчутливість до толтеродину або допоміжних речовин
- Важкий виразковий коліт
- Токсичний мегаколон
04.4 Спеціальні попередження та відповідні запобіжні заходи при використанні -
Толтеродин слід з обережністю застосовувати пацієнтам з:
- Значна обструкція відтоку сечового міхура з ризиком затримки сечі
- Обструктивні розлади шлунково -кишкового тракту, наприклад. пілоричний стеноз
- Зміна функції нирок (див. Розділ 4.2)
- Захворювання печінки (див. Розділи 4.2 та 5.2)
- Нейропатія, що впливає на вегетативну нервову систему
- Грижа стравохідного отвору
- Ризик зниження моторики шлунково -кишкового тракту
Було виявлено, що введення багаторазових добових доз 4 мг (терапевтичне) та 8 мг (супратерапевтичне) толтеродину з негайним вивільненням подовжує інтервал QTc (див. Розділ 5.1). Клінічна значимість цих даних неясна і залежить від ризику для окремого пацієнта. фактори та чутливість Толтеродин слід з обережністю застосовувати пацієнтам з факторами ризику подовження інтервалу QT, включаючи:
- Подовження вродженого або набутого та задокументованого QT
- електролітні порушення, такі як гіпокаліємія, гіпомагніємія та гіпокальціємія
- брадикардія
- Існуюча важка ішемічна хвороба серця (кардіоміопатія, ішемія міокарда, аритмія, серцева недостатність)
- Одночасний прийом препаратів, що подовжують інтервал QT, включаючи препарати класу 1А (наприклад, хінідин, прокаїнамід) та клас III (наприклад, аміодарон, соталол), антиаритмічні засоби.
Зокрема, при застосуванні потужного інгібітора CYP3A4 введення толтеродину слід проводити з обережністю (див. Розділ 5.1). Слід уникати одночасного лікування потужними інгібіторами CYP3A4 (див. Розділ 4.5 Взаємодія).
Як і при будь -якому іншому лікуванні симптомів невідкладної сечі або невідкладного нетримання сечі до початку лікування, слід враховувати можливі органічні причини терміновості та частоти.
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії -
У разі слабкого метаболізму CYP2D6 одночасне системне лікування потужними інгібіторами CYP3A4, такими як макролідні антибіотики (наприклад, еритроміцин та кларитроміцин), протигрибкові засоби (наприклад, кетоконазол та ітраконазол) та інгібітори протеаз не рекомендується у зв’язку із збільшенням сироваткової концентрації. ) ризик передозування (див. розділ 4.4.).
Одночасне лікування іншими препаратами, що володіють антимускариновими властивостями, може призвести до більш вираженого терапевтичного ефекту та побічних реакцій. І навпаки, терапевтичний ефект толтеродину може бути зменшений після одночасного лікування агоністами холінергічних мускаринових рецепторів.
Дія прокінетичних препаратів, таких як метоклопрамід та цизаприд, може бути зменшена за допомогою толтеродину .
Одночасне лікування флуоксетином (потужним інгібітором CYP2D6) не призводить до клінічно значущої взаємодії, оскільки толтеродин та його CYP2D6-залежний метаболіт 5-гідроксиметилтолтеродин є еквівалентними.
Дослідження взаємодії з лікарськими засобами не показали взаємодії з варфарином або комбінованими оральними контрацептивами (етинілестрадіол / левоноргестрел).
Клінічне дослідження показало, що толтеродин не є метаболічним інгібітором CYP2D6, 2C19, 2C9, 3A4 або 1A2. Тому при одночасному застосуванні з толтеродином не очікується збільшення концентрації препаратів у плазмі крові, що метаболізуються за допомогою цих ізоферментів.
04.6 Вагітність та годування груддю -
Вагітність
Немає належних даних про застосування толтеродину вагітним жінкам.
Дослідження на тваринах показали ефекти репродуктивної токсичності (див. Розділ 5.3). Потенційний ризик для людини невідомий.
Тому ДЕТРУЗИТОЛ не рекомендується під час вагітності.
Час годування
Немає даних про виділення толтеродину у грудне молоко. У період лактації слід уникати застосування толтеродину.
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами -
Оскільки цей препарат може спричинити порушення акомодації або вплинути на час реакції, здатність керувати автомобілем та працювати з механізмами може негативно вплинути.
04.8 Побічні ефекти -
З огляду на його фармакологічний ефект, толтеродин може викликати легкі та помірні антимускаринові ефекти, такі як сухість у роті, диспепсія та сухість очей.
У наведеній нижче таблиці наведені дані, отримані за допомогою ДЕТРУЗИТОЛУ в ході клінічних досліджень та дані з постмаркетингового досвіду. Найчастіше повідомлялося про побічну реакцію-сухість у роті, яка виникала у 35% пацієнтів, які отримували таблетки ДЕТРУЗИТОЛ, і у 10% пацієнтів, які отримували плацебо. повідомлялося також дуже часто, що траплялося у 10,1% пацієнтів, які отримували таблетки ДЕТРУЗИТОЛ, і у 7,4% пацієнтів, які отримували плацебо.
Після початку терапії толтеродином у пацієнтів, які приймали інгібітори холінестерази для лікування деменції, були повідомлення про погіршення симптомів деменції (наприклад, сплутаність свідомості, дезорієнтація, марення).
Педіатричні пацієнти
У двох рандомізованих подвійних сліпих плацебо-контрольованих педіатричних дослідженнях ІІІ фази у 710 педіатричних пацієнтів протягом 12 тижнів частка пацієнтів з інфекцією сечовивідних шляхів, діареєю та аномальною поведінкою була вищою у пацієнтів, які отримували толтеродин, ніж у тих, хто отримував плацебо. (інфекція сечовивідних шляхів: толтеродин 6,8%, плацебо 3,6%; діарея: толтеродин 3,3%, плацебо 0,9%; ненормальна поведінка: толтеродин 1,6%, плацебо 0,4%(див. параграф 5.1).
Повідомлення про підозрювані побічні реакції
Повідомлення про підозрювані побічні реакції, що виникають після реєстрації лікарського засобу, є важливими, оскільки вони дозволяють здійснювати постійний моніторинг співвідношення користь / ризик лікарського засобу. Медичних працівників просять повідомляти про будь -які підозрювані побічні реакції через національну систему звітності. "Адреса: www .agenziafarmaco.gov.it/it/responsabili.
04.9 Передозування -
Найвища доза толтеродин-L-тартрату, що вводилася одноразово здоровим добровольцям, становила 12,8 мг. Найбільш серйозними побічними ефектами, що спостерігалися, були порушення акомодації та утруднення сечовипускання.
У разі передозування слід промити шлунок і ввести активоване вугілля.
Лікуйте симптоми наступним чином:
* важкі центральні антихолінергічні ефекти (наприклад, галюцинації, сильне збудження): ввести фізостигмін.
* Судоми або виражене збудження: ввести бензодіазепіни.
* Дихальна недостатність: зробити штучне дихання.
* Тахікардія: вводити β-адреноблокатори.
* Затримка сечі: використання катетера.
* Мідріаз: введення очних крапель пілокарпіну та / або утримання пацієнта в темряві.
Збільшення інтервалу QT спостерігалося при одноразовій добовій дозі 8 мг толтеродину з негайним вивільненням (удвічі більшій від рекомендованої добової дози стандартної лікарської форми та втричі більшій від максимальної експозиції препарату з пролонгованим вивільненням) протягом 4 днів У разі передозування толтеродину слід застосовувати стандартні підтримуючі заходи для регулювання подовження інтервалу QT.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ -
05.1 "Фармакодинамічні властивості -
Фармакотерапевтична група: спазмолітики сечі.
Код ATC: G04BD07.
Толтеродин - це специфічний конкурентний антагоніст мускаринових рецепторів, який демонструє вибірковість сечового міхура над слинними залозами in vivo. Один з метаболітів толтеродину (похідне 5-гідроксиметилу) має аналогічний фармакологічний профіль, як і у вихідної сполуки. У великих метаболізаторів цей метаболіт значно сприяє терапевтичному ефекту толтеродину (див. Розділ 5.2).
Ефекти від лікування можна очікувати протягом 4 тижнів.
Ефекти лікування Детрузитолом 2 мг двічі на день через 4 та 12 тижнів відповідно порівняно з плацебо (сукупні дані). Абсолютні та відсоткові зміни від вихідного рівня.
н.с. = не значний; * = стор
Вплив толтеродину оцінювали у пацієнтів, які піддавались обстеженню для базової уродинамічної оцінки, які після результатів уродинамічних тестів були віднесені до позитивних уродинамічних (моторні терміни) або негативних уродинамічних (сенсорні термінові) груп. У кожній групі пацієнти були рандомізовані для одержання як толтеродину, так і плацебо.
Клінічні ефекти толтеродину на інтервал QT i базуються на ЕКГ, отриманих у понад 600 пролікованих пацієнтів, включаючи пацієнтів літнього віку та пацієнтів з наявними серцево-судинними захворюваннями.
Вплив толтеродину на подовження інтервалу QT було додатково досліджено у 48 здорових добровольців (чоловіків та жінок) у віці 18-55 років. Пацієнтам давали 2 мг ставка і 4 мг ставка толтеродину у складі з негайним вивільненням. Результати (виправлені за формулою Фрідрісії) при максимальних концентраціях толтеродину (1 година) показали середнє збільшення інтервалу QTc на 5,0 та 11,8 мсек для доз 2 мг толтеродину відповідно. ставка і 4 мг ставка та 19,3 мсек для мофлоксацину (400 мг), що використовується як контрольний препарат. Фармакокінетична / фармакодинамічна модель показала, що інтервал QTc збільшується у пацієнтів з поганим метаболізмом (без CYP2D6), які отримують 2 мг толтеродину ставка порівнянний з тим, що спостерігається у швидких метаболізаторів, які отримували 4 мг ставка. При застосуванні обох доз толтеродину жоден суб’єкт, незалежно від метаболічного профілю, не перевищував 500 мсек абсолютного значення QTcF або не показував змін від вихідного рівня на 60 мсек. Ці зміни вважаються особливо значними пороговими значеннями. Доза 4 мг ставка відповідає максимальній експозиції (Cmax), що в три рази перевищує максимальну терапевтичну дозу капсул з пролонгованим вивільненням Детрузитолу.
Педіатричні пацієнти
Ефективність у педіатричній популяції не була продемонстрована. Було проведено два 12-тижневих рандомізованих, подвійно сліпих, плацебо-контрольованих дослідження фази III з капсулами толтеродину з пролонгованим вивільненням. 710 педіатричних пацієнтів (486 отримували тольтеродин та 224 отримували плацебо) у віці Від 5 до 10 років із збільшенням частоти сечовипускання та сечовипускання.
В обох дослідженнях між двома групами не спостерігалося істотних змін щодо вихідної загальної кількості епізодів нетримання сечі на тиждень (див. Розділ 4.8).
05.2 "Фармакокінетичні властивості -
Фармакокінетичні характеристики, характерні для цієї композиції: Толтеродин швидко всмоктується. І толтеродин, і 5-гідроксиметиловий метаболіт досягають максимальних концентрацій у сироватці крові через 1-3 години після введення.
Період напіввиведення толтеродину у вигляді таблеток становить 2-3 години у великих метаболізаторів та приблизно 10 годин у погано метаболізуючих (без CYP2D6). Після прийому таблеток концентрація у рівноважному стані досягається протягом 2 днів.
У великих метаболізаторів їжа не впливає на вплив незв’язаного толтеродину та активного метаболіту 5-гідроксиметилу, хоча рівень толтеродину збільшується під час прийому з їжею.
Так само не очікується ніяких клінічно значущих змін у поганих метаболізаторів.
Поглинання: Після перорального прийому толтеродин піддається метаболізму першого проходження, каталізованому CYP2D6, у печінці, що призводить до утворення 5-гідроксиметилового метаболіту, основного фармакологічно еквіпотентного метаболіту.
Абсолютна біодоступність толтеродину становить 17% у великих метаболізаторів та 65% у слабких метаболітів (дефіцит CYP2D6).
Розповсюдження: Толтеродин та 5-гідроксиметиловий метаболіт зв’язуються переважно з оросомукоїдом. Незв’язані фракції становлять відповідно 3,7% та 36%. Об’єм розподілу толтеродину становить 113 літрів.
Усунення: Толтеродин інтенсивно метаболізується в печінці після перорального застосування.
Первинний метаболічний шлях опосередковується поліморфним ферментом CYP2D6 і призводить до утворення метаболіту 5-гідроксиметилу. Подальша метаболізація призводить до утворення метаболітів 5-карбонової кислоти та N-деалкільованої 5-карбонової кислоти, які складають 51% та 29% метаболітів виявляється в сечі. Частина (близько 7%) населення має дефіцит активності CYP2D6. Профіль метаболізму, виявлений у цих пацієнтів (з поганою метаболічною здатністю), є деалкілуванням через ферменти CYP3A4 до деалкільованого N-толтеродину, що не викликає клінічних ефектів.
Решту населення складають швидкі метаболізатори. У великих метаболізаторів системний кліренс толтеродину в сироватці крові становить приблизно 30 л / годину. У поганих метаболізаторів зниження кліренсу призводить до значного збільшення сироваткової концентрації толтеродину (приблизно в 7 разів) та виявлення концентрацій 5-гідроксиметилового метаболіту, що не піддаються виявленню.
Метаболіт 5-гідроксиметилу є фармакологічно активним та еквіпотенційним щодо толтеродину. Через відмінності в характеристиках зв’язування білків толтеродину та 5-гідроксиметилового метаболіту експозиція (AUC) вільного толтеродину у пацієнтів із поганою метаболічною здатністю подібна до такої у поєднанні вільного толтеродину та похідного 5-гідроксиметилу у пацієнтів із активністю CYP2D6, коли вводяться в одній дозі. Безпека, переносимість та клінічна відповідь однакові незалежно від фенотипу.
Виведення радіоактивності після введення [14С] -толтеродину становить приблизно 77% із сечею та 17% з калом. Менше 1% дози виводиться у незміненому вигляді та приблизно 4% у вигляді 5-гідроксиметилового метаболіту.
У діапазоні терапевтичних доз фармакокінетика є лінійною.
Окремі групи пацієнтів
Порушення функції печінки: У пацієнтів з цирозом печінки виявлено приблизно у 2 рази вищу експозицію вільного толтеродину та його метаболіту 5-гідроксиметилу (див. Розділи 4.2 та 4.4).
Порушення функції нирок: середня експозиція вільного толтеродину та його метаболіту 5-гідроксиметилу подвоюється у пацієнтів з тяжкою нирковою недостатністю [кліренс інуліну (ШКФ)
У цих пацієнтів рівень інших метаболітів у плазмі крові помітно підвищився (до 12 разів). Клінічна значимість збільшення експозиції цих метаболітів невідома. Дані щодо випадків порушення функції нирок легкого та помірного ступеня відсутні (див. Розділи 4.2 та 4.4).
Педіатричні пацієнти
Експозиція активної речовини на дозу / мг є подібною у дорослих та підлітків. Середня експозиція активної речовини на дозу / мг приблизно у два рази вища у дітей віком від 5 до 10 років, ніж у дорослих (див. Розділи 4.2 та 5.1)
05.3 Доклінічні дані про безпеку -
У дослідженнях токсикології, мутагенезу, канцерогенезу та фармакології безпеки не було виявлено клінічно значущих ефектів, крім тих, що стосуються фармакологічних ефектів препарату.
Дослідження розмноження проводили на мишах і кроликах.
У мишей не спостерігалося впливу толтеродину на фертильність або репродуктивну функцію.
Толтеродин призвів до ембріональної смертності та вад розвитку плода після впливу плазми (Cmax або AUC) у 20 або 7 разів вище, ніж у чоловіків, які отримували лікування. Ніякого впливу на вади розвитку у кроликів не спостерігалося, але дослідження проводилися при значеннях експозиції у плазмі крові (Cmax або AUC), які були у 20 або 3 рази вищими, ніж очікувані у людей після терапевтичних доз.
Толтеродин, як і його активні метаболіти у людини, подовжує тривалість потенціалу дії (90% реполяризації) у волокнах пуркіньє собаки (у 14-75 разів більше терапевтичного рівня) та блокує потік K + у каналах hERG (клонований ефір людини ген, пов'язаний з a-go-go) (у 0,5-26,1 рази більше терапевтичного рівня).
У дослідженнях, проведених на собаках після введення толтеродину та його активних метаболітів людям (дози в 3,1–61,0 рази вище терапевтичних рівнів), спостерігалося подовження інтервалу QT. Клінічна значимість цього ефекту невідома.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ -
06.1 допоміжні речовини -
Ядро :
Мікрокристалічна целюлоза
Двоосновний кальцій фосфат дигідрат
Гліколят натрію крохмалю (тип В)
Стеарат магнію
Безводний колоїдний кремнезем
Покривна плівка :
Гранули для покриття, що містять:
Гіпромелоза
Мікрокристалічна целюлоза
Стеаринова кислота
Діоксид титану (E171)
06.2 Несумісність "-
Не актуально.
06.3 Строк дії "-
3 роки.
06.4 Особливі умови зберігання -
Особливих застережень щодо зберігання немає.
06.5 Характер безпосередньої упаковки та вміст упаковки -
Таблетки упаковуються в блістери з ПВХ / ПВХД та алюмінієвої фольги з термозапечатанним покриттям з ПВДК або у пляшки з ПНД з кришками з ПНД.
Упаковка: Таблетки Детрузитол випускаються у блістерах по 2х10, 3х10, 5х10 та 10х10 таблеток, 1х14, 2х14 та 4х14 таблеток, по 280 і 560 таблеток та у флаконах по 60 та 500 таблеток.
Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження -
Невикористаний продукт або відходи слід утилізувати відповідно до місцевих норм.
07.0 ВЛАСНИК "РОЗРОБНИЦТВА"
Pfizer Italia S.r.l.
Via Isonzo, 71 - 04100 Латина
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
ДЕТРУЗИТОЛ 1 мг таблетки, вкриті оболонкою - 28 таблеток, AIC n. 034168017
ДЕТРУЗИТОЛ 2 мг таблетки, вкриті оболонкою - 28 таблеток, AIC n. 034168029
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛА -
12 січня 1999/23 березня 2006