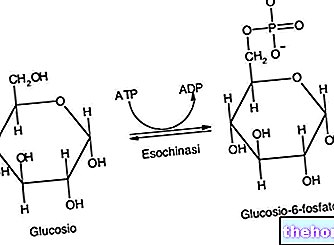
Якщо клітина працює в анаеробних умовах, вона виробляє енергію, перетворюючи глюкозу в лактат і, за циклом Кори, позбувається останнього; якщо є кисень (отже, в умовах спокою), більше 90% глюкози споживається аеробно і лише 10%, що залишилися, анаеробно. Коли виникає потреба у більшій кількості АТФ, ніж те, що здатний забезпечити аеробний шлях (наприклад, коли м’язи перебувають у стані стресу), тоді додатковий запас забезпечується анаеробним метаболізмом (ми перебуваємо в умовах нестачі кисню: задишка, втома при диханні тощо): необхідно прискорити цей метаболізм шляхом перетворення лактату (який одержують при гліколізі) в глюкозу шляхом глюконеогенезу.
У мітохондріях розвивається аеробний метаболізм.
Першим ферментом, що зустрічається в аеробному метаболізмі, є піруватдегідрогеназа; Точніше сказати, що піруватдегідрогеназа-це ферментний комплекс, а не фермент, оскільки він являє собою сукупність 48–60 одиниць білка з трьома послідовно діючими каталітичними центрами.
Піруватдегідрогеназа каталізує таку реакцію (окислювально -відновну):
Піруват + NAD + + CoA-SH → Ацетил CoA + NADH + H + + CO2
CoA-SH є коферментом А: він є похідним пантотенової кислоти; ацетил-кофермент А є тіоефіром. Це окисно -відновний процес, оскільки перший вуглець пірувату переходить від окислення номер три до окислення номер чотири (він окислюється), а другий вуглець пірувату переходить від окислення номер два до окислення номер три (він окислюється). Потім піруват окислюється (він втрачає в цілому два електрони) і НАД відновлюється.
Як згадувалося, піруватдегідрогеназа має три типи ферментативної активності, кожен з яких підтримується своїм каталітичним кофактором:
- тіамінпірофосфат (це похідне вітаміну В1); він активний у депротонованій формі: утворюється карбаніон.
- ліпоамід (це похідне ліпоєвої кислоти); він містить дуже реакційноздатний дисульфідний місток.
- флавін -адениндинуклеотид (це похідне вітаміну В2); це нуклеотид з окисно -відновними властивостями: його окисно -відновний центр складається з флавіну.
В еукаріотичних клітинах аеробний метаболізм відбувається в спеціалізованих органелах клітини, які є мітохондріями; у бактерій метаболізм глюкози та інших видів відбувається в клітині, але немає спеціалізованих органел.
Коли піруват потрапляє в мітохондрію, він піддається "дії піруваткарбоксилази", якщо є необхідність провести глюконеогенез (для реконструкції вихідного матеріалу), або він може бути підданий піруватдегідрогеназі, якщо це необхідно для виробництва енергії: "Ацетилкоензим А, який утворюється при аеробному метаболізмі, стимулює дію піруваткарбоксилази, отже, він сприяє глюкоконеогенезу та зменшує дію піруватдегідрогенази.
Давайте тепер подивимося, як діє піруватдегідрогеназа; перш за все, відбувається декарбоксилювання пірувату під дією тіамінпірофосфату.
Кисле середовище може гальмувати аеробний метаболізм, оскільки активна аніонна форма тіамінпірофосфату, яка протонується при кислому рН і не відбувається декарбоксилювання.
Декарбоксилювання-це складна реакція, оскільки зв'язок вуглець-вуглець доводиться розривати; в цьому випадку реакції термодинамічно сприяє той факт, що проміжний продукт реакції (гідроксиетилтіамінпірофосфат) дає резонанс (p-електрони молекули делокалізовані): гідроксиетилтіамінпірофосфат існує у трьох можливих формах (резонансу) та це робить його досить стабільним. Крім того, гідроксиетилтіамінпірофосфат в аніонній формі виживає досить довго, щоб мати можливість взаємодіяти з дисульфідним містком ліпоаміду (другий каталітичний кофактор піруватдегідрогенази); дисульфідний міст-це коливальний рукав (він розташований у кінець довгого гнучкого ланцюга) і може переміщатися від одного каталітичного центру до іншого в комплексі ферментів.
Потім ліпоамід через дисульфідний місток зв’язує гідроксиетилтіамінпірофосфат: отримують ацетилліпоамід.Щойно описана є першою стадією реакції трансацетилювання, каталізованої першим ферментом комплексу піруватдегідрогенази; в цій фазі між гідроксильною групою і тіамінпірофосфатом розривався зв’язок, який повернувся до початкової форми: відбулася окисно -відновна реакція, в якій дисульфідний міст діяв як окислювач (два атоми сірки відновились) у порівняннях у гідроксильній групі, яка окислюється до ацетилу.
Після цієї фази коливальна рука ліпоаміду рухається і наближається до другого ферменту піруватдегідрогенази, який здійснює справжню трансацетилазну активність, несучи з собою ацетильну групу: відбувається друга фаза реакції трансацетилювання, каталізована другим ферментом; таким чином ми отримали ацетил -кофермент А. Тепер необхідно відновити ліпоамід, що знаходиться у відновлюваній формі: втручається третій фермент піруватдегідрогенази, який окислює ліпоамід і переносить його електроди до FAD, який відновлюється до FADH2. FAD / FADH2 може функціонувати як окислювально -відновна пара в двох різних моноелектронних стадіях або в одній бієлектронній стадії.
FADH2 негайно передає свої електрони NAD +, отримуючи FAD і NADH + H +.
Ацетилкоензим А, отриманий, як описано, є вихідним продуктом циклу Кребса (або циклу трикарбонових кислот).

.jpg)

.jpg)