Загальність
Лікування хронічного мієлоїдного лейкозу (ХМЛ) включає декілька терапевтичних варіантів, які можуть тримати хворобу під контролем протягом тривалого періоду часу. Регулярні аналізи крові та кісткового мозку та часте оцінювання гематологом або онкологом можуть контролювати прогресування раку.

З результатів медичних досліджень (аналіз крові, цитогенетичні та молекулярні тести) можна зрозуміти:
- Ступінь ефективності лікування з плином часу та еволюція реакції на терапію;
- Якщо хвороба більше не реагує на ліки (стійкість до терапії).
Моніторинг та відповідь на терапію
Правильний моніторинг перебігу захворювання має важливе значення для перевірки ефективності терапії, а отже, для можливості оперативного втручання у разі невдачі лікування.
Цитогенетичний аналіз та дослідження молекулярної біології, а також у діагностичних цілях використовуються також для оцінки ступеня відповіді на терапевтичний протокол та для виявлення будь -якої стійкості захворювання після лікування (дослідження мінімальної залишкової хвороби):
- Повна гематологічна відповідь: Коли терапія починає давати ефект, кількість клітин лейкемії зменшується. Гематологічні тести більше не можуть виявити анормальні клони, але це можливо за допомогою цитогенетичного аналізу.
- Повна цитогенетична відповідь: отримується, коли наявність філадельфійської хромосоми (Ph) більше не підкреслюється звичайним цитогенетичним аналізом (стандартний підхід для моніторингу відповіді на лікування) або флуоресцентною гібридизацією in situ (FISH), методикою, яка оцінює відсоток Ph + клітини кісткового мозку. Цитогенетичний аналіз, виконаний на тонкоголковому аспірованому зразку кісткового мозку, також є єдиним методом визначення наявності будь-яких хромосомних змін, крім Філадельфійської хромосоми, з прогностичною роллю.
- Повна молекулярна відповідь: вона досягається, коли молекулярний аналіз не може виявити експресію гібридного гена BCR / ABL. Терапія виявилася ефективною, а молекулярні сигнали, які сприяють виробленню білків bcr-abl, настільки низькі, що їх неможливо виявити навіть за допомогою високочутливих тестів, таких як молекулярні. Підвищений рівень стенограми, який контролюється, може свідчити про втрату відповіді на лікування.
Досягнення цих результатів є дуже важливим результатом: багато досліджень показують, що пацієнти з повною цитогенетичною та молекулярною реакцією мають дуже високу ймовірність вижити протягом тривалого часу без прогресування хвороби до прискореної та / або бластної фази .
На ефективність терапії може вплинути багато факторів, і тому на початкових етапах рекомендується продовжувати обстеження через 3, 6, 12 і 18 місяців.
Інформація, отримана на сьогоднішній день з клінічних досліджень, які визначають оптимальну відповідь та неефективність у різні періоди терапії, призвела до розробки схеми моніторингу, якої необхідно дотримуватися для правильного ведення пацієнта (показання, запропоновані Європейська лейкемія-мережа):
Гематолог (або онколог) зможе встановити деякі цілі та перевірити ефективність терапії у конкретному клінічному випадку, оскільки пацієнти по -різному реагують на терапію, і не всі можуть досягти оптимальних етапів терапії протягом передбаченого періоду часу ...
Терапевтичні варіанти
Основною метою лікування ХМЛ є "досягнення повної молекулярної ремісії: хвороба контролюється за допомогою лікування (навіть якщо вона не зникає повністю)", а кількість вироблених патологічних клонів достатньо обмежена, щоб не викликати жодних симптомів. Більшість людей не можуть повністю позбутися від клітин лейкемії, лікування може допомогти досягти тривалої ремісії хвороби.
Терапевтичні цілі можуть включати:
- Обмежити прояв симптомів хронічного мієлоїдного лейкозу;
- Відновлення нормальних параметрів, пов'язаних з кількістю клітин крові;
- Зменшити кількість клітин лейкозу позитивної хромосоми Філадельфії (Ph +) та молекулярних сигналів (транскрипти BCR / ABL);
- Прагніть до зникнення Філадельфійських + хромосом (повна цитогенетична відповідь).
Звичайні антибластні препарати
Деякі антибластні препарати, наприклад бусульфан (алкілування) і l "гідроксимочевина (специфічний інгібітор синтезу ДНК), використовувалися, особливо в минулому, для досягнення циторедукції та контролю захворювання у хронічній фазі. Звичайне лікування призвело до поліпшення якості життя, але не змогло суттєво змінити природну історію захворювання або запобігти прогресуванню до фази прискорення / вибуху.
Рекомбінантний інтерферон-альфа
З початку 1980 -х років запровадження інтерферони дозволило спостерігати, на додаток до зменшення та нормалізації частки гранулоцитів, досягнення негативізації цитогенетичних та молекулярних тестів, що викликає більш тривалий період хронічної фази, з подальшим зменшенням еволюції у прискореній та / або бластній фазах. Інтерферон -альфа знизив роль традиційної терапії ХМЛ: цей препарат здатний викликати повну цитогенетичну відповідь у 20-30% пацієнтів, особливо перешкоджаючи трансляції проліферативних сигналів у клітинах Ph + та інгібуючи клітинні розмноження пухлинних попередників. Інтерферон-альфа також діє з непрямим механізмом на виживання клітин лейкемії, зменшуючи їх адгезію до клітин і посилюючи активність клітин імунної системи.
Обмеженням застосування цього препарату є його незначна токсичність.Побічні ефекти інтерферону включають втому, лихоманку та втрату ваги. З метою поліпшення досягнутих результатів, інтерферон комбінували з іншими цитотоксичними агентами. Було показано, що лише асоціація інтерферону з цитозин арабінозидом (ARA-C) дає кращі результати, ніж інтерферон, однак без очевидної переваги виживання.
Алогенна трансплантація кісткового мозку
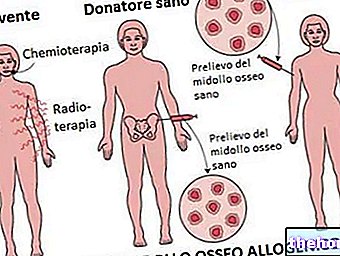
Трансплантація стовбурових клітин від здорового донора, сумісного з реципієнтом (алогенна трансплантація), протягом багатьох років є найчастішим терапевтичним показанням і досі є єдиним методом лікування, здатним остаточно викорінити новоутворення.
Ця процедура, якщо вона проводиться у хронічній фазі, може призвести до п’ятирічної виживання без захворювання приблизно у 50% випадків.
Алогенна трансплантація кісткового мозку передбачає першу фазу руйнування всіх (або майже всіх) клітин Ph + шляхом кондиціонування (хіміотерапія в поєднанні з загальним опроміненням тіла), після чого відбувається відновлення гемопоетичного мозку інфузованими стовбуровими клітинами -донорами. Крім того, донорські лімфоцити кісткового мозку сприяють контролю та / або усуненню будь-яких клітин Ph + з імуноопосередкованим ефектом, званим ефектом "трансплантат проти лейкемії" (трансплантат проти лейкемії). Відповідь на терапію можна контролювати, оцінюючи, чи зникли молекулярні зміни, характерні для хронічного мієлоїдного лейкозу. Алогенна трансплантація кісткового мозку являє собою терапевтичне лікування, здатне "вилікувати" ХМЛ, але, на жаль, включає швидкість неефективності через смертельну токсичність та / або рецидив. Ця процедура, насправді, дуже вимоглива і на неї може вплинути вік пацієнт, пацієнт і передчасність трансплантації (місяці або роки з моменту діагностики хронічної фази): через потенційну небезпеку це можливо практично лише у пацієнтів віком до 55 років без подальших супутніх патологій. Тому алогенна трансплантація становить реальну терапевтичну можливість лише для меншості пацієнтів з ХМЛ (також враховуючи труднощі з пошуком сумісного донора стовбурових клітин).
Зовсім недавно у пацієнтів з хронічним мієлоїдним лейкозом, непридатним для алотрансплантації (вік, відсутність донора, відмова тощо), була запропонована аутотрансплантація. Кістковий мозок пацієнта, повторно інфузований після "навмисно адекватної цитоцидної терапії для Ph + -клітин (з антибластичним + інтерфероном), відновлюється із переважним повторним розширенням Ph-клітин.
Іматініб мезилат (Glivec ®)
Історія лікування хронічного мієлоїдного лейкозу була революційно змінена впровадженням першого інгібітора тирозинкінази (Іматиніб мезилат), який значно сприяв покращенню якості життя пацієнтів.
Іматиніб є специфічним інгібітором BCR / ABL, розробленим після розуміння молекулярної біології захворювання та використаним при лікуванні Ph + хронічного мієлоїдного лейкозу.
Препарат здатний викликати повну молекулярну цитогенетичну ремісію у 80-90% пацієнтів, а також активний при мієлоїдних новоутвореннях з еозинофілією та залученням PDGRF (фактор росту, що походить від тромбоцитів, мітоген сироватки, що бере участь у багатьох патологічних станах, що сприяє хемотаксису та проліферації ємність).
Іматиніб вибірково блокує активність тирозинкінази BCR / ABL через механізм інгібування АТФ: препарат зв’язує молекулу високої енергії (АТФ), наявну у певному домені кінази BCR / ABL, запобігаючи фосфорилювання інших субстратів та блокуючи каскад реакцій, які відповідають за процес генерації Ph + лейкозних клонів. Доза, що використовується для цієї молекули (іматиніб метизилат), варіюється від 400 мг / добу до 800 мг / день у залежності від фази захворювання та відповіді. В даний час це препарат вибору для лікування ХМЛ через його чудову ефективність. Побічні ефекти, які можуть бути оборотними при суспензії та / або зменшенні дози, можуть бути різними (збільшення трансаміназ, нудота, висипання на шкірі, затримка рідини тощо).
Спостережувались випадки стійкості до препарату з плином часу (наприклад, пацієнти з прогресуючим захворюванням) та ідентифіковані біологічні клінічні критерії для визначення типу відповіді на лікування. Механізми, відповідальні за цю резистентність, виявляються множинними (мутації кіназного домену, ампліфікація / надмірна експресія BCR / ABL, клональна еволюція ...). У цих випадках продовження терапії іматинібом більше не є доцільним.
Для пацієнтів з цими станами можливі наступні варіанти:
- Алогенна трансплантація;
- Звичайна терапія (гідроксимочевина, бусульфан та ін.);
- L "інтерферон;
- Експериментальна терапія (з інгібіторами тирозинкінази 2 покоління).
Інгібітори тирозинкінази другого покоління
Невдача терапії іматинібом пов’язана з прогресуванням хронічного мієлоїдного лейкозу з прискореною та / або бластною фазою та має особливо поганий прогноз. В останні роки фармакологічні дослідження дозволили використовувати в клінічній практиці інгібітори тирозинкінази другого покоління, активні у пацієнтів, у яких розвинулася резистентність до іматинібу: Дазатиніб (Sprycel ®) та Нілотініб (Tasigna ®) використовуються у пацієнтів з хронічною фазою та / або прогресування ХМЛ, стійкої до дії Glivec ® і здатної повторно індукувати повну та стійку гематологічну, цитогенетичну та молекулярну реакції. Проте численні дослідження показали, що клон Ph + - через його генетичну нестабільність - може викликати мутації домену кінази BCR / ABL і виявляються стійкими до різних інгібуючих препаратів. Інші молекули на експериментальній фазі (інгібітори 3 -го покоління) спрямовані на специфічні мішені хронічного мієлоїдного лейкозу; зокрема, вони здатні сенсибілізувати лейкозні клітини Ph + зі специфічними мутаціями (приклад: Mk-0457 для стійкої ХМЛ та з мутацією T315I, яка безпосередньо впливає t місце зв'язування іматинібу).
Інші статті на тему "Терапія хронічного мієлоїдного лейкозу"
- Хронічний мієлоїдний лейкоз: Хронічний мієлоїдний лейкоз: діагностика
- Хронічний мієлоїдний лейкоз: визначення, причини, симптоми













-cos-cause-e-disturbi-associati.jpg)










.jpg)