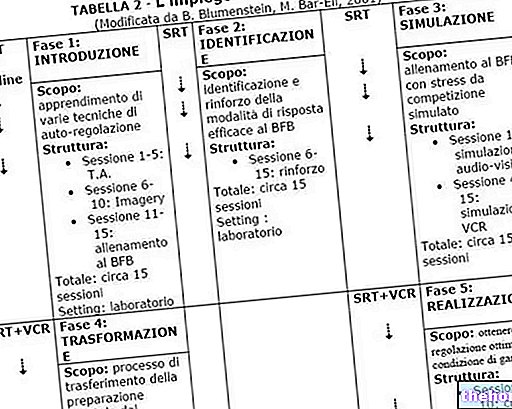
Діючі речовини: Адалімумаб
Humira 40 мг / 0,8 мл розчин для ін’єкцій для педіатричного застосування
Пакети Humira доступні для розмірів упаковки:- Humira 40 мг / 0,8 мл розчин для ін’єкцій для педіатричного застосування
- Humira 40 мг розчин для ін’єкцій у попередньо заповненому шприці
- Humira 40 мг розчин для ін’єкцій у попередньо заповненому шприці з захисним пристроєм для голки
- Humira 40 мг розчин для ін’єкцій у попередньо заповненій ручці
Чому використовується Humira? Для чого це?
Humira містить діючу речовину адалімумаб, селективний імуносупресивний засіб. Humira призначений для лікування поліартикулярного ювенільного ідіопатичного артриту у дітей у віці 2-17 років, ентезитоартриту у дітей у віці 6-17 років, хвороби Крона у дітей у віці 6-17 років. 17 років та бляшкового псоріазу у дітей у віці від 4 до 17 років. Це препарат, що зменшує запальний процес цих захворювань. Діюча речовина, адалімумаб, є людським моноклональним антитілом, виробленим культурами клітин. Моноклональні антитіла - це білки, які розпізнають та зв'язуються з іншими білками. Адалімумаб зв’язується зі специфічним білком (фактором некрозу пухлини або TNFα), який у високих концентраціях присутній при таких запальних захворюваннях, як поліартикулярний ювенільний ідіопатичний артрит, артрит, пов’язаний з ентезитом, хвороба Крона та бляшковий псоріаз.
Поліартикулярний ювенільний ідіопатичний артрит та артрит, асоційований з ентезитом
Поліартикулярний ювенільний ідіопатичний артрит та ентезит-асоційований артрит є запальними захворюваннями. Humira використовується для лікування поліартикулярного ювенільного ідіопатичного артриту та ентезитоартриту. При діагностиці можуть бути призначені лікарські засоби, що модифікують захворювання, такі як метотрексат. Якщо відповідь на ці препарати недостатня, дитині буде призначено Хуміру для лікування поліартикулярного ювенільного ідіопатичного артриту або артриту, асоційованого з ентезитом.
Хвороба Крона у дітей
Хвороба Крона - це запальне захворювання травного тракту. Humira призначений для лікування хвороби Крона у дітей віком від 6 до 17 років. Дитині спочатку дадуть інші ліки. Якщо ваша дитина не реагує достатньо добре на ці ліки, йому або їй буде призначено Humira для зменшення ознак та симптомів хвороби Крона.
Дитячий бляшковий псоріаз
Бляшковий псоріаз - це стан шкіри, який викликає почервонілі, лускаті, затверділі ділянки шкіри, покриті сріблястими лусочками. Вважається, що псоріаз викликаний проблемою з імунною системою організму, що призводить до збільшення виробництва клітин шкіри. Humira використовується для лікування важкого бляшкового псоріазу у дітей та підлітків у віці від 4 до 17 років, у яких місцева терапія та фототерапія не працювали оптимально або не показані.
Протипоказання Коли Хуміра не слід застосовувати
Не використовуйте Humira
- Якщо у вашої дитини алергія на адалімумаб або будь -який інший інгредієнт цього препарату (перерахований у розділі 6).
- Якщо у вас "важка інфекція, включаючи активний туберкульоз (див." Попередження та запобіжні заходи "). Важливо повідомити лікаря, якщо у вашої дитини є симптоми інфекції, такі як лихоманка, рани, втома, проблеми зі зубами.
- При наявності помірної або важкої серцевої недостатності. Важливо повідомити лікаря, якщо було або є серйозне серцеве захворювання (див. "Попередження та запобіжні заходи").
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Хуміру
Порадьтеся з лікарем або фармацевтом вашої дитини перед використанням препарату Хуміра
- Якщо у вас виникли будь -які алергічні реакції з такими симптомами, як стиснення в грудях, хрипи, запаморочення, набряк або висип, припиніть давати Хуміру та негайно зверніться до лікаря.
- Якщо у вас є інфекція, включаючи тривалі або локалізовані інфекції (наприклад, виразки ніг), перед початком лікування препаратом Хуміра проконсультуйтеся з лікарем. Якщо ви не впевнені, зверніться до лікаря.
- Ви можете легше заразитися інфекціями під час лікування Humira. Цей ризик може збільшитися, якщо у дитини порушена функція легенів. Ці інфекції можуть бути серйозними і включати туберкульоз, інфекції, викликані вірусами, грибками, паразитами чи бактеріями, або інші умовно-патогенні інфекції та сепсис, які в рідкісних випадках можуть бути небезпечними для життя. Важливо повідомити лікаря про такі симптоми, як лихоманка, рани, втома або проблеми зі зубами. Ваш лікар може порекомендувати тимчасово припинити Хуміру.
- Оскільки у пацієнтів, які отримували Humira, були випадки туберкульозу, перед початком терапії Humira лікарю потрібно буде перевірити, чи є у дитини типові ознаки або симптоми туберкульозу. Це включатиме збирання детальної медичної оцінки, включаючи історію хвороби дитини та відповідні клінічні тести (наприклад, рентген грудної клітки та туберкулінову пробу). Результати та результати таких тестів повинні бути записані в картку оповіщення для пацієнта. Дуже важливо повідомити лікаря, якщо дитина коли -небудь хворіла на туберкульоз, чи мала вона тісний контакт з хворими на туберкульоз. Під час терапії може виникнути туберкульоз, навіть якщо дитина пройшла профілактичне лікування туберкульозу. Негайно зверніться до лікаря, якщо під час або після терапії з’являються симптоми туберкульозу (постійний кашель, втрата ваги, млявість, помірна температура) або інші інфекції.
- Скажіть своєму лікарю, якщо ваша дитина проживає або подорожує в регіони, де грибкові інфекції, такі як гістоплазмоз, кокцидіоїдомікоз або бластомікоз, є ендемічними.
- Скажіть своєму лікарю, якщо у вашої дитини були повторювані інфекції або якщо у них є умови, які підвищують ризик зараження.
- Скажіть своєму лікарю, якщо ваша дитина є носієм вірусу гепатиту В (HBV), якщо у нього активна інфекція вірусу гепатиту В або якщо ви думаєте, що він може бути ризикований зараження вірусом гепатиту В. Лікар повинен перевірити дитину на гепатит Вірусна інфекція B. Прийом препарату Хуміра може спричинити реактивацію вірусу гепатиту В у людей, які є носіями цього вірусу. У деяких рідкісних випадках, особливо якщо пацієнт проходить терапію іншими препаратами, що пригнічують імунну систему, реактивація вірусу гепатиту В може бути небезпечною для життя.
- Важливо повідомити лікаря вашої дитини, якщо з’являться такі симптоми інфекції, як лихоманка, рани, втома або проблеми з зубами.
- Перед операцією або стоматологічними процедурами повідомте свого лікаря, що ваша дитина приймає Хуміру. Ваш лікар може порекомендувати тимчасове призупинення.
- Якщо у вашої дитини такі демієлінізуючі захворювання, як розсіяний склероз, лікар вирішить, чи слід починати прийом препарату Хуміра.
- Деякі вакцини можуть викликати інфекції, тому їх не слід вводити під час лікування препаратом Хуміра. Проконсультуйтеся з лікарем, перш ніж робити щеплення дитині. Дітям рекомендується, по можливості, виконувати запланований графік щеплень відповідно до чинних вказівок щодо вакцинації перед початком терапії Хумірою. Якщо ви приймали Humira під час вагітності, у вашої дитини може бути підвищений ризик зараження цією інфекцією приблизно через 5 місяців після останньої дози, яку ви прийняли під час вагітності. Важливо повідомити свого педіатра або іншого медичного працівника про використання Humira. під час вагітності, щоб вони могли вирішувати, коли Вашій дитині робити щеплення будь -якого типу.
- У разі легкої серцевої недостатності та супутнього лікування препаратом Хуміра лікарю необхідно буде ретельно оцінити стан серця дитини та контролювати його стан. Важливо повідомити лікаря про будь -які проблеми з серцем, як минулі, так і теперішні. Якщо з’являються нові симптоми серцевої недостатності або погіршуються наявні симптоми (наприклад, задишка або набряк ніг), негайно зверніться до лікаря. Лікар вирішить, чи може дитина приймати Хуміру.
- У деяких пацієнтів організм не може виробляти достатню кількість клітин крові, щоб допомогти боротися з інфекцією або зупинити кровотечу. Якщо у вашої дитини стійка температура, синці або кровотеча або блідість, негайно зверніться до лікаря. Останні можуть прийняти рішення про припинення терапії.
- Деякі типи пухлин зустрічалися дуже рідко у пацієнтів, як дітей, так і дорослих, які отримували лікування препаратом Хуміра або іншими препаратами проти ФНО.У пацієнтів з тривалим важким ревматоїдним артритом ризик розвитку лімфоми (типу раку, що вражає лімфатичну систему) та лейкемії (типу раку, що вражає кров та кістковий мозок) може бути вищим за середній. Якщо ваша дитина приймає Хуміру, ризик захворіти на лімфому, лейкемію чи інші види раку може зрости. У рідкісних випадках у пацієнтів, які отримували Humira, спостерігався специфічний та важкий тип лімфом. Деякі з цих пацієнтів також отримували азатіоприн або 6-меркаптопурин. Скажіть своєму лікарю, якщо ви приймаєте азатіоприн або 6-меркаптопурин разом з Humira. Крім того, у пацієнтів, які приймали Хуміру, спостерігалися випадки немеланотичного раку шкіри. Якщо під час або після терапії з’являються нові ураження шкіри, або якщо зовнішній вигляд наявних ушкоджень змінюється, повідомте про це свого лікаря.
- Були випадки злоякісних пухлин, крім лімфоми, у пацієнтів із специфічним типом легеневої хвороби, що називається хронічною обструктивною легеневою хворобою (ХОЗЛ), які лікувалися іншим анти-ФНП. Якщо ваша дитина хворіє на ХОЗЛ або багато курить, вам слід обговорити з лікарем, чи доцільне лікування анти-ФНО.
Діти та підлітки
- Вакцинація: Якщо можливо, Ваша дитина повинна була вже зробити всі щеплення перед застосуванням препарату Хуміра.
- Не давайте Хуміру дітям з поліартикулярним ювенільним ідіопатичним артритом віком до 2 років.
Взаємодії Які препарати або продукти харчування можуть змінити дію препарату Хуміра
Інші ліки та Humira
Повідомте лікаря або фармацевта Вашої дитини, якщо Ваша дитина приймає, нещодавно приймала або може приймати будь -які інші ліки.
Humira можна приймати разом з метотрексатом або іншими протиревматичними препаратами, що модифікують хворобу (сульфасалазин, гідроксихлорохін, лефлуномід та парентеральні солі золота), стероїдами або анальгетиками, включаючи нестероїдні протизапальні препарати (НПЗЗ).
Humira не слід приймати одночасно з лікарськими засобами, що містять анакінру або абатацепт як активну речовину. Якщо ви не впевнені, зверніться до лікаря.
Humira з їжею та напоями
Оскільки Humira вводиться під шкіру (підшкірно), їжа та напої не впливають на Humira.
Попередження Важливо знати, що:
Вагітність та годування груддю
Вплив препарату Хуміра на вагітних невідомий, тому застосування препарату Хуміра вагітним жінкам не рекомендується. Рекомендується уникати вагітності, застосовуючи адекватну контрацепцію під час лікування препаратом Хуміра та принаймні 5 місяців після лікування. "Остання медикаментозна терапія Якщо ваша дитина завагітніє, вам слід звернутися до лікаря.
Невідомо, чи проникає адалімумаб у грудне молоко.
Якщо особа, яка приймає Хуміру, - це молода жінка, яка годує грудьми, вона повинна припинити грудне вигодовування під час терапії Хумірою та принаймні через 5 місяців після останнього лікування препаратом Хуміра. Якщо ви приймали Humira під час вагітності, у вашої дитини може бути підвищений ризик зараження. Важливо, щоб ви розповіли своєму педіатру або іншому медичному працівнику про ваше застосування Humira під час вагітності, перш ніж ваша дитина отримає будь -які ліки. (див. розділ про вакцинацію для отримання додаткової інформації).
Якщо ви підозрюєте, що ваша дочка почала вагітність або планує завагітніти, зверніться за порадою до лікаря або фармацевта перед використанням цього препарату.
Водіння автомобіля та роботу з машинами
Humira може впливати на здатність керувати автомобілем, їздити на велосипеді або працювати з механізмами, хоча і незначно. Після прийому Humira у вас можуть виникнути порушення зору та відчуття, що ваше оточення крутиться.
Дозування та спосіб застосування Як застосовувати Humira: Дозування
Завжди використовуйте цей препарат точно так, як вам сказав лікар або фармацевт вашої дитини. Якщо ви сумніваєтесь, зверніться до лікаря або фармацевта вашої дитини.
Діти з поліартикулярним ювенільним ідіопатичним артритом
Рекомендована доза Humira для пацієнтів з поліартикулярним ювенільним ідіопатичним артритом у віці від 2 до 12 років залежить від зросту та ваги дитини. Лікар вашої дитини порадить вам правильну дозу для використання. Рекомендована доза Humira для пацієнтів з поліартикулярним ювенільним ідіопатичним артритом у віці 13-17 років-40 мг через тиждень.
Діти з артритом, асоційованим з ентезитом
Рекомендована доза Humira для пацієнтів з ентезит-асоційованим артритом у віці від 6 до 17 років залежить від зросту та ваги дитини.
Діти або підлітки з хворобою Крона
Діти або підлітки вагою менше 40 кг:
Звичайна схема прийому становить 40 мг на початку, потім 20 мг через два тижні.Якщо потрібна більш швидка відповідь, лікар може призначити початкову дозу 80 мг (у вигляді двох ін’єкцій за один день), а потім - 40 мг через два тижні Після цього звичайна доза становить 20 мг через тиждень. Залежно від реакції дитини лікар може збільшити частоту прийому дози до 20 мг щотижня.
Діти або підлітки вагою 40 кг і більше:
Звичайна схема прийому становить 80 мг на початку, потім 40 мг через два тижні.Якщо потрібна більш швидка відповідь, лікар може призначити початкову дозу 160 мг (у вигляді 4 ін’єкцій на день або 2 ін’єкції на день протягом 2 днів поспіль), потім через 2 тижні - 80 мг. Після цього звичайна доза становить 40 мг через тиждень. Залежно від реакції дитини лікар може збільшити частоту доз до 40 мг. Також доступні ручки по 40 мг та наповнені шприци по 40 мг.
Діти або підлітки з псоріазом
Рекомендована доза Humira для пацієнтів віком від 4 до 17 років з бляшковим псоріазом залежить від ваги вашої дитини. Лікар вашої дитини порадить вам правильну дозу для застосування.
Спосіб і шлях введення
Humira вводиться шляхом ін’єкції під шкіру (шляхом підшкірної ін’єкції).
Інструкції з приготування та ін'єкції Хуміри:
Наступна інструкція пояснює, як вводити Хуміру. Уважно прочитайте інструкції та виконуйте їх крок за кроком. Ваш лікар або його асистент дасть вам вказівки щодо техніки самовведення та кількості, яку потрібно дати своїй дитині. Не вводьте ін’єкції, доки ви не впевнені, що розумієте, як приготувати та розпочати введення. Після належного вказівки ін’єкцію можна зробити вам або іншим, таким як член сім’ї чи друг.
Недотримання наведених нижче інструкцій, як описано, може призвести до зараження, яке, в свою чергу, може викликати інфекцію у дитини. Вміст шприца не можна змішувати з іншими лікарськими засобами в одному шприці або флаконі.
1) Підготовка
- Переконайтеся, що ви знаєте відповідну кількість (обсяг), необхідну для вашої дози. Якщо ви не знаєте суму, припиніть та зверніться до лікаря для отримання подальших інструкцій.
- Вам знадобиться спеціальний контейнер для відходів, такий як контейнер для гострих предметів або за вказівкою вашої медсестри, лікаря або фармацевта. Поставте контейнер на робочу поверхню.
- Ретельно вимийте руки.
- Вийміть з картону коробку, що містить шприц, адаптер для флакона, флакон, 2 тампони зі спиртом та голку. Якщо у картонній коробці є друга коробка для наступного введення, негайно поверніть її до холодильника.
- Перевірте термін придатності на картонній упаковці. НЕ використовуйте будь -які елементи з коробки після закінчення терміну придатності.
- Розмістіть наведені нижче предмети на чистій поверхні, БЕЗ виймання предметів з упаковки. Один шприц об'ємом 1 мл Один адаптер для флакона Один педіатричний флакон з ін'єкційним розчином Humira Дві спиртові прокладки або одна голка
- Humira - прозора, безбарвна рідина. НЕ використовуйте його, якщо рідина непрозора, знебарвлена, або всередині є флокуляції або частинки.
2) Підготовка дози Humira до ін’єкцій
Загальні вказівки: НЕ викидайте предмети, поки ін'єкція не буде завершена.
- Підготуйте голку, частково відкривши упаковку з кінця, найближчого до жовтого роз'єму шприца. Відкрийте упаковку настільки, щоб відкрити жовтий роз'єм шприца. Розмістіть упаковку світлою стороною вгору.
- Зніміть пластикову кришку з флакона, поки не побачите верхню частину пробки флакона.
- Очистіть ковпачок флакона одним із тампонів зі спиртом. НЕ торкайтеся кришки флакона після очищення її тампоном.
- Зніміть кришку з упаковки адаптера флакона, не виймаючи її з упаковки.
- Тримайте флакон кришкою догори дном.
- Коли серповидний адаптер все ще знаходиться у прозорій упаковці, прикріпіть його до пробки флакона, натискаючи на нього, доки адаптер не клацне.
- Коли ви переконаєтесь, що адаптер прикріплений до флакону, витягніть упаковку з флакона.
- Обережно покладіть флакон та адаптер на чисту робочу поверхню, обережно, щоб не впасти. НЕ торкайтеся адаптера.
- Приготуйте шприц, частково відкривши упаковку з кінця, найближчого до білого поршня.
- Відкрийте прозору упаковку настільки, щоб відкрити білий поршень, не виймаючи шприц із упаковки.
- Утримуючи пакет шприца, ПОВІЛЬНО витягніть поршень на 0,1 мл вище встановленої дози (наприклад, якщо встановлена доза становить 0,5 мл, посуньте поршень до 0,6 мл). НІКОЛИ не перевищуйте положення, що відповідає 0,9 мл, незалежно від призначеної дози.
- На наступному етапі обсяг буде відрегульовано до встановленої дози.
- НЕ виштовхуйте білий поршень до кінця зі шприца.
ПРИМІТКА: Якщо білий поршень виштовхнути до кінця зі шприца, викиньте шприц і зверніться до свого постачальника Humira для заміни. НЕ намагайтесь знову вставити білий поршень.
- НЕ використовуйте білий поршень, щоб вийняти шприц з упаковки. Тримайте шприц на градуйованій стороні і виймайте його з упаковки. НІ в якому разі не кладіть шприц.
- Утримуючи перехідник, вставте кінчик шприца в адаптер і поверніть шприц однією рукою за годинниковою стрілкою до упору. НЕ затягуйте занадто сильно.
- Утримуючи флакон, натисніть білий поршень до упору. Цей крок важливий для отримання правильної дози. Утримуйте білий шток поршня і переверніть флакон і шприц догори дном.
- Повільно потягніть білий поршень на 0,1 мл вище встановленої дози. Важливо відмінити відповідну дозу. Обсяг, еквівалентний призначеній дозі, буде встановлено на кроці 4, Підготовка дози. Якщо призначена доза становить 0,5 мл, потягніть білий поршень до об’єму 0,6 мл. Рідина пройде з флакона в шприц.
- Натисніть білий поршень до кінця, щоб виштовхнути рідину назад у флакон. Знову повільно потягніть за білий поршень, поки він не досягне 0,1 мл вище встановленої дози; важливо відмінити відповідну дозу та запобігти утворенню бульбашок повітря у рідині або порожніх просторах.Об’єм, еквівалентний призначеній дозі, буде встановлено на кроці 4, Підготовка дози.
- Якщо у шприці залишилися бульбашки повітря або прогалини, ви можете повторити це до трьох разів. НЕ струшуйте шприц.
ПРИМІТКА: Якщо білий поршень виштовхнути до кінця зі шприца, викиньте шприц і зверніться до свого постачальника Humira для заміни. НЕ намагайтеся знову вставляти білий поршень.
- Утримуючи шприц у вертикальному положенні на градуйованій стороні, вийміть перехідник з флакона, відкрутивши перехідник іншою рукою. НЕ торкайтесь кінчика шприца.
- Якщо ви помітили велику бульбашку повітря або порожній простір біля кінчика шприца, ПОВІЛЬНО вставте білий поршень у шприц, поки рідина не почне надходити у наконечник шприца. НЕ натискайте на білий поршень один раз за положення дози.
- Наприклад, якщо встановлена доза становить 0,5 мл, НЕ проштовхуйте білий поршень за положення 0,5 мл.
- Переконайтеся, що рідина, що залишилася у шприці, принаймні еквівалентна дозі, яку витягують. Якщо він нижчий, НЕ використовуйте шприц і зверніться до свого лікаря.
- Вільною рукою візьміть пакет з голками з жовтим роз’ємом шприца вниз.
- Тримаючи шприц вгору, вставте наконечник шприца в жовтий роз'єм і поверніть шприц, як зазначено стрілкою на малюнку, до упору. Голка тепер прикріплена до шприца.
- Вийміть голку з упаковки, але НЕ знімайте прозору кришку голки.
- Помістіть шприц на чисту робочу поверхню. Негайно перейдіть до етапу введення та етапів підготовки дози.
3) Вибір та підготовка місця ін’єкції
- Виберіть місце на стегні або животі: НЕ використовуйте ту саму ділянку, яка була використана для останньої ін’єкції.
- Нова ін'єкція повинна бути зроблена щонайменше на 3 см від місця останньої ін'єкції.
- НЕ вводьте ін'єкції в ділянки, де шкіра почервоніла, отримала синці або тверда. Це може свідчити про інфекцію; тому слід звернутися до лікаря.
- Щоб зменшити ймовірність зараження, протріть місце ін’єкції іншим спиртовим тампоном. НЕ торкайтесь області знову перед ін’єкцією.
4) Приготування дози
- Візьміть шприц голкою вгору.
- Другою рукою поверніть рожеву кришку голки до шприца
- Зніміть прозорий ковпачок з голки, потягнувши його іншою рукою вгору.
- Голка чиста.
- НЕ торкайтесь голки.
- НЕ направляйте шприц вниз після зняття прозорого ковпачка з голки.
- НЕ намагайтеся знову надіти прозорий ковпачок на голку.
- Тримайте шприц на рівні очей голкою вгору, щоб чітко бачити кількість рідини. Будьте обережні, щоб ліки не потрапили в очі.
- Перевірте кількість ліків, які ви прийняли ще раз.
- Обережно втисніть білий поршень у шприц, доки у шприці не буде вказано необхідну кількість ліків. Надлишок рідини може витікати з голки під час натискання на поршень. НЕ виймайте голку або шприц.
Ін'єкція Humira
- Вільною рукою обережно візьміть вже протерту спиртом ділянку і тримайте її нерухомо.
- Другою рукою тримайте шприц під кутом 45 ° до місця ін’єкції.
- Одним твердим, швидким рухом втисніть всю голку в шкіру.
- Відпустіть шкіру рукою.
- Натисніть на білий поршень, щоб ввести ліки, поки шприц не буде порожнім.
- Коли шприц порожній, вийміть голку зі шкіри, відтягнувши її під тим самим кутом, що і при її введенні.
- Вільною рукою обережно візьміть вже протерту спиртом ділянку і тримайте її нерухомо.
- Другою рукою тримайте шприц під кутом 45 ° до місця ін’єкції.
- Одним твердим, швидким рухом втисніть всю голку в шкіру.
- Відпустіть шкіру рукою.
- Натисніть на білий поршень, щоб ввести ліки, поки шприц не буде порожнім.
- Коли шприц порожній, вийміть голку зі шкіри, витягнувши її під тим самим кутом, що і при її введенні.
- Обережно потягніть рожеву кришку голки вгору, над голкою, і відкрийте її, а потім покладіть шприц з голкою на робочу поверхню. НЕ надягайте прозорий ковпачок на голку.
- За допомогою шматочка марлі прикладіть тиск до місця ін’єкції протягом 10 секунд. Можлива невелика кровотеча. НЕ масажуйте місце ін'єкції. При бажанні нанесіть патч.
Утилізація матеріалів
- Вам знадобиться спеціальний контейнер для відходів, такий як контейнер для гострих предметів, або за вказівкою вашої медсестри, лікаря або фармацевта.
- Помістіть шприц з голкою, флакон та адаптер у спеціальний контейнер для гострих предметів. НЕ кладіть ці предмети у контейнер для домашнього сміття.
- Шприц, голку, флакон та адаптер НІКОЛИ не можна використовувати повторно.
- Завжди зберігайте цей контейнер подалі від очей та недоступного для дітей місця.
- Викиньте всі інші використані матеріали у контейнер для побутового сміття.
Передозування Що робити, якщо ви прийняли занадто багато Хуміри
Якщо ви використовуєте більше, ніж слід:
Якщо ви випадково вводите більшу кількість препарату Хуміра або вводите його частіше, ніж призначив лікар, зверніться до лікаря та повідомте йому, що ваша дитина вжила більше ліків. Завжди зберігайте коробку або флакон із ліками, навіть якщо вони порожні.
Якщо ви використовуєте менше Хуміри, ніж слід:
Якщо ви випадково вводите меншу кількість препарату Хуміра або вводите його рідше, ніж призначено лікарем чи фармацевтом вашої дитини, зверніться до лікаря або провізора вашої дитини та повідомте їм, що ваша дитина випила менше ліків. Завжди зберігайте коробку або флакон із ліками, навіть якщо вони порожні.
Якщо ви забули використовувати Хуміру:
Якщо ви забули зробити дитині ін’єкцію Хуміри, вона повинна ввести дозу Хуміри, як тільки вона пам’ятає, а потім регулярно давати дитині наступну дозу відповідно до встановленого графіка.
Якщо Ваша дитина припинить приймати Хуміру
Рішення про припинення застосування препарату Хуміра слід обговорити з лікарем дитини.Після припинення лікування симптоми дитини можуть повернутися. Якщо у Вас виникнуть додаткові запитання щодо застосування цього препарату, зверніться до лікаря або фармацевта.
Побічні ефекти Які побічні ефекти від Humira
Як і всі ліки, цей препарат може викликати побічні ефекти, хоча вони виникають не у всіх. Більшість побічних ефектів мають легкий або помірний характер. Однак деякі можуть бути важкими і вимагати лікування. Побічні ефекти можуть виникнути через 4 місяці після останньої ін’єкції Хуміри.
Негайно повідомте лікаря, якщо ви помітили будь -яку з наступних реакцій:
- сильна шкірна висипка, кропив’янка або інші ознаки алергічної реакції;
- набряк обличчя, рук, ніг;
- утруднене дихання, утруднення ковтання;
- задишка при навантаженні або при лежанні або набряку стоп.
Повідомте лікаря якомога швидше, якщо ви помітили будь -яку з наступних реакцій:
- ознаки інфекції, такі як лихоманка, погане самопочуття, рани, проблеми зі зубами, печіння при сечовипусканні;
- втома або слабкість;
- кашель;
- поколювання;
- оніміння;
- подвійне бачення;
- слабкість в руках або ногах;
- набряк або відкрита рана, яка не загоюється
- ознаки та симптоми, що свідчать про появу порушень, що впливають на систему кровотворення, таких як наявність постійної лихоманки, синців, крововиливів, блідості.
Описані вище симптоми можуть бути ознаками таких побічних ефектів, які спостерігалися при прийомі препарату Хуміра:
Дуже часто (можуть зачіпати більш ніж 1 з 10 осіб):
- реакції в місці ін’єкції (включаючи біль, набряк, почервоніння або свербіж);
- інфекції дихальних шляхів (включаючи застуду, ринорею, синусит та пневмонію);
- головний біль;
- біль у животі;
- нудота і блювота;
- висип;
- м’язово -скелетні болі.
Поширені (можуть вражатися до 1 з 10 осіб):
- важкі інфекції (включаючи септицемію та грип);
- шкірні інфекції (включаючи целюліт та оперізувальний герпес);
- вушні інфекції;
- інфекції ротової порожнини (включаючи інфекції зубів та простий герпес);
- інфекції статевої системи;
- інфекції сечовивідних шляхів;
- грибкові інфекції;
- інфекції суглобів;
- доброякісні пухлини;
- рак шкіри;
- алергічні реакції (включаючи сезонну алергію);
- зневоднення;
- зміни настрою (включаючи депресію);
- тривожність;
- порушення сну;
- розлади чутливості, такі як поколювання, посмикування або оніміння;
- мігрень;
- здавлення кореня нерва (включаючи біль у попереку та ногах);
- порушення зору;
- запалення очей;
- запалення повік і набряк очей;
- запаморочення;
- відчуття прискореного серцебиття;
- гіпертонія;
- припливи;
- гематома;
- кашель;
- астма;
- задишка;
- шлунково -кишкова кровотеча;
- диспепсія (розлад травлення, здуття живота, печія);
- кислотний рефлюкс;
- сикка сика (включаючи сухість очей і рота);
- свербіж;
- свербляча висипка;
- синці;
- запалення шкіри (наприклад, екзема);
- ламання нігтів пальців рук і ніг;
- підвищена пітливість;
- втрата волосся;
- початок або загострення псоріазу;
- м’язові спазми;
- кров у сечі;
- проблеми з нирками;
- біль у грудях;
- набряки;
- лихоманка;
- зменшення тромбоцитів у сангві, що збільшує ризик кровотеч або синців;
- труднощі з загоєнням.
Нечасті (можуть виникнути до 1 з 100 осіб):
- опортуністичні інфекції (які включають туберкульоз та інші інфекції, що виникають при зниженні імунного захисту);
- неврологічні інфекції (включаючи вірусний менінгіт);
- очні інфекції;
- бактеріальні інфекції;
- дивертикуліт (запалення та інфекція товстого кишечника);
- пухлини;
- пухлини лімфатичної системи;
- меланома;
- порушення імунної системи, які можуть вражати легені, шкіру та лімфатичні вузли (найчастіше проявляються як саркоїдоз);
- васкуліт (запалення кровоносних судин);
- тремор;
- інсульт;
- нейропатія;
- подвійне бачення;
- зниження слуху, дзвін;
- відчуття нерегулярного серцебиття, такого як серцебиття;
- проблеми з серцем, які можуть викликати задишку або набряк щиколоток;
- гострий інфаркт міокарда;
- утворення мішка в стінці магістральної артерії, запалення і згусток у вені, закупорка судини;
- захворювання легенів, що викликає задишку (включаючи запалення);
- легенева емболія (закупорка легеневої артерії);
- плевральний випіт (ненормальний збір рідини в плевральному просторі);
- запалення підшлункової залози, що викликає сильний біль у животі та спині;
- утруднення ковтання;
- набряк обличчя;
- запалення жовчного міхура, каменів у жовчному міхурі;
- жирна печінка;
- нічна пітливість;
- рубець;
- аномальний м’язовий катаболізм;
- системний червоний вовчак (включаючи запалення шкіри, серця, легенів, суглобів та інших органів)
- перерваний сон;
- імпотенція;
- запалення.
Рідкісні (можуть виникнути до 1 з 1000 осіб):
- лейкемія (злоякісне новоутворення, що вражає кровотворну систему на периферійному рівні (кров) та кістковий мозок);
- важка алергічна реакція з шоком;
- розсіяний склероз;
- неврологічні розлади (такі як запалення зорового нерва та синдром Гійєна-Барре, які можуть викликати м’язову слабкість, ненормальні відчуття, поколювання в руках та верхній частині тіла);
- зупинка серця;
- легеневий фіброз (рубцювання легені);
- перфорація кишечника;
- гепатит;
- реактивація гепатиту В;
- аутоімунний гепатит (запалення печінки, викликане вашою власною імунною системою);
- шкірний васкуліт (запалення кровоносних судин шкіри);
- Синдром Стівенса-Джонсона (ранні симптоми включають нездужання, лихоманку, головний біль та висип);
- набряк обличчя, пов’язаний з алергічними реакціями;
- мультиформна еритема (запальна шкірна висипка);
- вовчакоподібний синдром.
Невідомо (частоту неможливо оцінити за наявними даними):
- гепато-селезінкова Т-клітинна лімфома (рідкісний рак крові, який часто призводить до летального результату);
- Карцинома клітин Меркеля (тип раку шкіри);
- Печінкова недостатність;
- погіршення стану, званого дерматоміозитом (проявляється у вигляді висипу, що супроводжується м’язовою слабкістю).
Деякі з побічних ефектів, що спостерігаються при застосуванні Humira, можуть бути безсимптомними і можуть бути виявлені лише в аналізах крові. До них відносяться:
Дуже часто (можуть зачіпати більш ніж 1 з 10 осіб):
- низький рівень лейкоцитів;
- низька кількість еритроцитів;
- збільшення ліпідів крові;
- збільшення ферментів печінки.
Поширені (можуть вражатися до 1 з 10 осіб):
- збільшення кількості лейкоцитів;
- знижена кількість тромбоцитів;
- підвищення рівня сечової кислоти в крові;
- зміна натрію в крові;
- зниження вмісту кальцію в крові;
- зниження вмісту фосфору в крові;
- підвищення рівня цукру в крові;
- підвищення рівня лактатдегідрогенази крові;
- наявність аутоантитіл у крові.
Рідкісні (можуть виникнути до 1 з 1000 осіб):
- низька кількість лейкоцитів, еритроцитів і тромбоцитів.
Невідомо (частоту неможливо оцінити за наявними даними):
- печінкова недостатність.
Повідомлення про побічні ефекти
Якщо у Вашої дитини виникають будь -які побічні ефекти, зверніться до лікаря або фармацевта Вашої дитини, що включає будь -які можливі побічні ефекти, не зазначені у цій брошурі. Ви також можете повідомляти про побічні ефекти безпосередньо за допомогою національної системи звітності, наведеної у Додатку V. Повідомляючи про побічні ефекти, ви можете допомогти надати більше інформації про безпеку застосування цього лікарського засобу.
Термін придатності та утримання
Зберігайте цей препарат подалі від очей та недоступного для дітей місця.
Не використовуйте цей препарат після закінчення терміну придатності, зазначеного на етикетці / блістері / картонній упаковці після закінчення терміну придатності. Термін придатності відноситься до останнього дня цього місяця.
Зберігати в холодильнику (2 ° C - 8 ° C). Не заморожувати.
Зберігайте флакон у відповідній упаковці, щоб захистити ліки від світла.
Не викидайте будь -які ліки через стічні води або побутові відходи. Запитайте у свого лікаря або фармацевта, як викидати ліки, які ви більше не використовуєте. Це допоможе захистити навколишнє середовище.
Склад та лікарська форма
Що містить Хуміра
Діюча речовина - адалімумаб.
Допоміжні інгредієнти: маніт, моногідрат лимонної кислоти, цитрат натрію, натрію дигідрофосфат дигідрат, динатрію фосфату дигідрат, хлорид натрію, полісорбат 80, гідроксид натрію та вода для ін’єкцій.
Цей лікарський засіб містить менше 1 ммоль (23 мг) на дозу 0,8 мл, тому по суті він не містить натрію і не містить консервантів.
Як виглядають флакони Humira та вміст упаковки
Розчин для ін’єкцій Хуміра 40 мг у флаконах поставляється у вигляді стерильного розчину 40 мг адалімумабу, розчиненого у 0,8 мл розчину.
Флакони Humira складаються з розчину адалімумабу, що міститься у скляній флаконі. Одна упаковка містить 2 коробки, кожна з яких містить 1 флакон, один порожній стерильний шприц, 1 голку, 1 адаптер для флакона та 2 тампони зі спиртом.
Humira також випускається у попередньо заповненому шприці або попередньо заповненій ручці.
+ Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
HUMIRA 40 МГ / 0,8 мл РОЗЧИН ДЛЯ ІНЖЕКЦІЙ ДЛЯ ПЕДІАТРІЧНОГО ВИКОРИСТАННЯ
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Кожен флакон одноразової дози 0,8 мл містить 40 мг адалімумабу.
Адалімумаб є рекомбінантним людським моноклональним антитілом, експресованим у клітинах яєчника китайського хом'яка.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Прозорий розчин для ін’єкцій.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Ювенільний ревматоїдний артрит
Поліартикулярний ювенільний ідіопатичний артрит
Humira в поєднанні з метотрексатом показаний для лікування активного поліартикулярного ювенільного ідіопатичного артриту у пацієнтів віком від 2 років, які мали неадекватну відповідь на один або кілька протиревматичних препаратів, що модифікують хворобу (DMARDs). Humira може призначатися як монотерапія у разі непереносимості метотрексату або коли продовження лікування метотрексатом є недоцільним (щодо ефективності монотерапії див. розділ 5.1). Humira не вивчався у пацієнтів віком до 2 років.
Артрит, пов'язаний з ентезитом
Humira призначений для лікування активних форм ентезит-асоційованого артриту у пацієнтів віком від 6 років, які мали неадекватну відповідь або мають непереносимість традиційної терапії (див. Розділ 5.1).
Хвороба Крона у педіатричних пацієнтів
Humira призначений для лікування важкої активної хвороби Крона у педіатричних пацієнтів (від 6 років), які мали неадекватну відповідь на звичайну терапію, включаючи первинну дієту, кортикостероїдну терапію та імуномодулятор, або мають непереносимість або мають протипоказання до такі методи лікування.
04.2 Дозування та спосіб введення
Дозування
Терапію Хумірою повинні розпочинати та контролювати лікарі -спеціалісти, які мають досвід у діагностиці та лікуванні станів, при яких показано застосування препарату Хуміра. Пацієнтам, які отримують препарат Хуміра, необхідно надати спеціальну картку попередження.
Після належного вказівки щодо техніки ін’єкції Хуміра пацієнти можуть робити собі ін’єкції самостійно, якщо їх лікар вважатиме за доцільне, і при необхідності проводити періодичні медичні огляди.
Педіатричне населення
Ювенільний ревматоїдний артрит
Поліартикулярний ювенільний ідіопатичний артрит у віці від 2 до 12 років.
Рекомендована доза Humira для пацієнтів з поліартикулярним ювенільним ідіопатичним артритом у віці від 2 до 12 років становить 24 мг / м2 площі поверхні тіла до максимальної разової дози 20 мг адалімумабу (для пацієнтів віком від 2 років підшкірно. Вибирається об’єм d ») виходячи з зросту та ваги пацієнта (табл. 1).
Таблиця 1. Доза Humira в мілілітрах (мл) за зростом і вагою пацієнтів з поліартикулярним ювенільним ідіопатичним артритом та артритом, асоційованим з ентезитом
* Максимальна разова доза становить 40 мг (0,8 мл)
Поліартикулярний ювенільний ідіопатичний артрит з 13 років
Пацієнтам віком від 13 років і старше вводять дозу 40 мг через тиждень, незалежно від площі поверхні тіла.
Для таких пацієнтів також доступні ручки 40 мг та наповнені шприци 40 мг для введення повної дози 40 мг.
Наявні дані свідчать про те, що клінічна відповідь зазвичай досягається протягом 12 тижнів лікування. Пацієнтам, у яких відповідь на терапію протягом цього періоду недостатня, слід ретельно обміркувати необхідність продовження терапії.
Немає відповідного застосування Humira пацієнтам віком до 2 років за цим показанням
Артрит, пов'язаний з ентезитом
Рекомендована доза Humira для пацієнтів з ентезит-асоційованим артритом у віці від 6 років і старше становить 24 мг / м2 площі поверхні тіла до максимальної разової дози адалімумабу 40 мг, що вводиться кожні два тижні шляхом підшкірної ін’єкції. Об’єм ін’єкції вибирається залежно від зросту та ваги пацієнта (табл. 1).
Humira не вивчався у пацієнтів віком до 6 років з ентезит-асоційованим артритом.
Хвороба Крона у педіатричних пацієнтів
Хвороба Крона у педіатричних пацієнтів
Рекомендована індукційна доза Humira для педіатричних пацієнтів з важкою формою хвороби Крона становить 40 мг на тиждень 0, а потім 20 мг на тиждень 2. Якщо потрібна більш швидка реакція на терапію, можна використовувати режим 80 мг на тиждень 0 ( доза може бути введена у вигляді двох ін’єкцій за один день) та 40 мг на 2 -му тижні, з розумінням того, що ризик розвитку побічних ефектів може бути більшим при застосуванні більшої індукційної дози.
Після індукційного лікування рекомендована доза становить 20 мг через тиждень шляхом підшкірної ін’єкції. Деякі особи з недостатньою відповіддю можуть отримати користь від збільшення частоти доз до Humira 20 мг щотижня.
Хвороба Крона у педіатричних пацієнтів ≥ 40 кг:
Рекомендована індукційна доза Humira для педіатричних пацієнтів з важкою формою хвороби Крона становить 80 мг на тиждень 0, а потім 40 мг на тиждень 2. Якщо потрібна більш швидка реакція на терапію, можна застосувати режим 160 мг на тиждень 0. ( доза може бути введена у вигляді чотирьох ін’єкцій в один день або у вигляді двох ін’єкцій на день протягом двох днів поспіль) та 80 мг на 2 -му тижні, з розумінням того, що ризик розвитку побічних ефектів може бути більшим при застосуванні більшої дози індукція.
Після індукційного лікування рекомендована доза становить 40 мг через тиждень шляхом підшкірної ін’єкції. Деякі особи з недостатньою відповіддю можуть отримати користь від збільшення частоти доз до 40 мг Humira щотижня.
Необхідно ретельно продумати продовження терапії у пацієнта, який не реагує на 12 тиждень.
Пацієнтам, яким потрібна повна доза 40 мг, також доступні ручка 40 мг та наповнений шприц 40 мг.
Немає відповідного застосування Хуміри дітям віком до 6 років за цим показанням
Ниркова та / або печінкова недостатність
У цьому типі популяції гуміра не вивчалася. Не можна давати жодних рекомендацій щодо дозування.
Спосіб введення
Humira вводять шляхом ін’єкції під шкіру. Повна інструкція із застосування міститься в інструкції з експлуатації.
04.3 Протипоказання
Підвищена чутливість до активної речовини або до будь -якої з допоміжних речовин, перерахованих у розділі 6.1.
Активний туберкульоз або інші серйозні інфекції, такі як сепсис та умовно -патогенні інфекції (див. Розділ 4.4).
Помірна або тяжка серцева недостатність (NYHA клас III / IV) (див. Розділ 4.4).
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
З метою покращення простежуваності біологічних лікарських засобів торговельна марка та номер партії введеного препарату повинні бути чітко записані (або позначені).
Інфекції
Пацієнти, які отримують антагоністи TNF, більш схильні до важких інфекцій. Порушення функції легенів може збільшити ризик розвитку інфекцій, тому пацієнтів слід ретельно обстежувати на наявність інфекцій, включаючи туберкульоз, до, під час та після лікування препаратом Хуміра. Оскільки виведення адалімумабу може тривати до чотирьох місяців, протягом цього періоду слід продовжувати моніторинг.
Терапію Humira не слід розпочинати у пацієнтів з активними інфекціями, включаючи хронічні або локалізовані інфекції, поки вони не будуть контрольовані. У пацієнтів, які перенесли туберкульоз, і у пацієнтів, які подорожували районами з високим ризиком розвитку туберкульозу або ендемічного мікозу, такими як гістоплазмоз, кокцидіоїдомікоз або бластомікоз, перед початком терапії слід враховувати ризик та користь лікування препаратом Хуміра. (Див. Інші умовно -патогенні інфекції).
Пацієнти, у яких під час терапії препаратом Хуміра виникає нова інфекція, повинні уважно стежити і пройти повну діагностичну оцінку. Якщо розвивається нова важка інфекція або сепсис, введення препарату Хуміра слід припинити та розпочати відповідну протимікробну або протигрибкову терапію, доки інфекція не буде контрольована. Лікарям слід бути обережними при застосуванні препарату Хуміра у пацієнтів з рецидивуючими інфекціями в анамнезі або з супутніми станами, які можуть схильність пацієнтів до інфекцій, включаючи одночасне застосування імуносупресивних препаратів.
Важкі інфекції:
Повідомлялося про серйозні інфекції, включаючи сепсис, спричинений бактеріями, мікобактеріями, інвазійними грибками, паразитами, вірусами або іншими умовно -патогенними інфекціями, такими як лістеріоз, легіонельоз та пневмоцистоз у пацієнтів, які отримували препарат Хуміра.
Інші серйозні інфекції, що спостерігаються під час клінічних випробувань, включають пневмонію, пієлонефрит, септичний артрит та септицемію. Повідомлялося про випадки госпіталізації або летальних випадків, пов’язаних з інфекціями.
Туберкульоз:
Туберкульоз, включаючи реактивацію та новий початок туберкульозу, повідомлявся у пацієнтів, які застосовували Хуміру. Повідомлялося про випадки легеневого та позалегеневого (тобто розповсюдженого) туберкульозу.
Перед початком терапії препаратом Хуміра всіх пацієнтів слід обстежити на наявність активного чи неактивного («прихованого») туберкульозу. Ця оцінка повинна включати "детальну історію хвороби пацієнтів з попередньою історією туберкульозу або будь-яких контактів з людьми з активним туберкульозом, а також з попередньою та / або супутньою імуносупресивною терапією. Відповідні скринінгові тести (тобто шкірний тест на туберкулін та рентген грудної клітини) ) у всіх пацієнтів (можливе дотримання місцевих вказівок) .Рекомендується провести ці тести та записати результати у картку попередження пацієнта. Лікарі повинні бути обережні щодо ризику хибнонегативних результатів шкірного тесту на туберкулін, особливо у важкохворих або пацієнтів з ослабленим імунітетом.
Якщо діагностовано активний туберкульоз, терапію препаратом Хуміра не слід розпочинати (див. Розділ 4.3).
У всіх описаних нижче ситуаціях слід проводити «ретельну оцінку співвідношення ризику та користі від терапії препаратом Хуміра.
При підозрі на прихований туберкульоз бажано звернутися до лікаря, який спеціалізується на лікуванні туберкульозу.
Якщо діагностовано прихований туберкульоз, перед початком терапії препаратом Хуміра слід розпочати протитуберкульозну профілактику відповідно до місцевих рекомендацій.
Про початок лікування протитуберкульозної профілактики також слід розглянути перед початком лікування препаратом Хуміра у пацієнтів з різними чи значними факторами ризику розвитку туберкульозу, незважаючи на негативний тест на туберкульоз, і у тих пацієнтів, чия історія хвороби свідчить про наявність прихованого або активного туберкульозу в анамнезі. що неможливо підтвердити, чи адекватний був курс лікування, який вони пройшли.
Незважаючи на профілактичне лікування туберкульозу, випадки реактивації туберкульозу мали місце у пацієнтів, які отримували препарат Хуміра. Деякі пацієнти, які успішно лікувалися від активного туберкульозу, знову хворіли на туберкульоз під час лікування препаратом Хуміра.
Пацієнтам слід порадити звернутися за медичною допомогою, якщо під час або після терапії препаратом Хуміра виникають ознаки / симптоми, що свідчать про можливу туберкульозну інфекцію (наприклад, постійний кашель, втрата ваги, втрата ваги, помірна температура, млявість).
Інші умовно -патогенні інфекції:
Випадки опортуністичних інфекцій, включаючи інвазивні грибкові інфекції, спостерігалися у пацієнтів, які приймали Хуміру. Ці інфекції не були правильно діагностовані у пацієнтів, які приймали антагоністи TNF, і це призвело до затримки відповідного лікування, іноді з летальним результатом.
У пацієнтів, у яких з’являються такі ознаки та симптоми, як лихоманка, нездужання, втрата ваги, пітливість, кашель, задишка та / або легеневий інфільтрат або інше серйозне системне захворювання з супутнім шоком або без нього, слід запідозрити інвазивну грибкову інфекцію та негайно припинити лікування Введення діагнозу Humira та емпірична протигрибкова терапія у цих пацієнтів повинна проводитися за погодженням з лікарем, який спеціалізується на лікуванні пацієнтів з інвазивними грибковими інфекціями.
Реактивація гепатиту В.
Реактивація гепатиту В (наприклад, позитивного поверхневого антигену) сталася у хронічних носіїв вірусу гепатиту В, які отримували антагоністи TNF, включаючи Humira. Деякі випадки мали летальний результат. Перед початком лікування препаратом Хуміра пацієнти повинні пройти обстеження на наявність вірусу гепатиту В.Консультація лікаря, який має досвід лікування гепатиту В, рекомендується тим пацієнтам, у яких позитивний тест на гепатит В.
За носіями вірусу гепатиту В, які потребують лікування препаратом Хуміра, слід уважно стежити за ознаками та симптомами активної інфекції вірусу гепатиту В не тільки протягом усієї терапії, а й протягом місяців після припинення терапії. Адекватних даних щодо лікування пацієнтів немає з вірусом гепатиту В, який проходить противірусну терапію, щоб уникнути повторної активації вірусу гепатиту В одночасно з терапією антагоністами ФНП. У пацієнтів, у яких розвивається реактивація вірусу гепатиту В, слід припинити введення препарату Хуміра та розпочати ефективну противірусну терапію, що супроводжується адекватне підтримуюче лікування.
Неврологічні події
Антагоністи TNF, включаючи Хуміру, у рідкісних випадках асоціювалися з новим початком або загостренням клінічних симптомів та / або рентгенологічними ознаками демієлінізуючих захворювань центральної нервової системи, включаючи розсіяний склероз, неврит зорового нерва та периферичні демієлінізуючі захворювання, включаючи синдром Гійєна-Барре. слід застосовувати Humira пацієнтам з попереднім або нещодавнім початком центральних або периферичних демієлінізуючих розладів.
Алергічні реакції
У клінічних випробуваннях серйозні алергічні реакції, пов'язані з Humira, були рідкістю. Несерйозні алергічні реакції, пов'язані з Humira під час клінічних випробувань, були рідкістю. Повідомлялося про серйозні алергічні реакції, включаючи анафілаксію після введення препарату Хуміра.Якщо виникають анафілактичні реакції або інші тяжкі алергічні прояви, введення препарату Хуміра слід негайно припинити та розпочати відповідну терапію.
Імуносупресія
У дослідженні 64 пацієнтів з ревматоїдним артритом, які отримували лікування препаратом Хуміра, не було жодних доказів інгібування затримки гіперчутливості, зниження рівня імуноглобулінів або зміни кількості Т, В, NK, моноцитарних / клітинних лімфоцитів. Макрофагів та нейтрофілів .
Новоутворення та лімфопроліферативні захворювання
У контрольних розділах клінічних випробувань антагоністів ФНП у пацієнтів, які отримували блокатор ФНВ, спостерігалося більше випадків злоякісних пухлин, включаючи лімфому, ніж у контрольній групі. Однак випадки були рідкісними. У постмаркетингових дослідженнях повідомлялося про випадки лейкемії у пацієнтів, які отримували антагоніст TNF. Існує більший ризик розвитку лімфом та лейкемії у пацієнтів з важко активним і тривалим ревматоїдним артритом, запальним захворюванням, яке ускладнює оцінку ризику. З наявними знаннями не можна виключати розвиток лімфом. Лейкемія та інші злоякісні утворення у пацієнтів лікувати препаратами проти TNF.
У постмаркетингових дослідженнях повідомлялося про випадки раку, деякі з летальним результатом у дітей, підлітків та молодих людей (до 22 років), які отримували антагоністи ФНО (початок терапії ≤ 18 років), включаючи адалімумаб. Близько половини випадків були лімфомами. Інші випадки представляли безліч різних видів раку і включали рідкісні види раку, зазвичай пов'язані з імуносупресією. Не можна виключити ризик розвитку пухлин у дітей та підлітків, які отримують антагоністи ФНО
У пацієнтів, які отримували адалімумаб, спостерігалися рідкісні постмаркетингові випадки гепатоспленочної Т-клітинної лімфоми.Цей рідкісний тип Т-клітинної лімфоми має дуже агресивний клінічний перебіг і часто є летальним. Деякі з цих випадків гепатоспленочної Т-клітинної лімфоми траплялися у молодих дорослих пацієнтів, які отримували препарат Хуміра та отримували супутню терапію азатіоприном або 6-меркаптопурином-препаратами, що використовуються для лікування запальних захворювань кишечника. Необхідно ретельно розглянути потенційний ризик від комбінації азатіоприну або 6-меркаптопурину та Хуміри. Не можна виключити ризик розвитку гепатоспленочної Т-клітинної лімфоми у пацієнтів, які отримують препарат Хуміра (див. Розділ 4.8).
Клінічні дослідження не проводилися у пацієнтів з онкологічними захворюваннями в анамнезі або у пацієнтів, лікування яких Humira тривало після розвитку раку. Тому лікування препаратом Хуміра у цій популяції пацієнтів слід розглядати з особливою обережністю (див. Розділ 4.8).
До та під час лікування препаратом Хуміра всі пацієнти, особливо пацієнти з анамнезом обширної імуносупресивної терапії або хворі на псоріаз, які в анамнезі отримували лікування ПУВА, повинні бути обстежені на наявність можливого немеланотичного раку шкіри. Також повідомлялося про меланому та клітинний рак Меркеля у пацієнтів, які отримували антагоністи TNF, включаючи адалімумаб (див. Розділ 4.8).
У дослідницькому клінічному дослідженні, в якому оцінювалося застосування іншого антагоніста ФНП, інфліксимабу, у пацієнтів із помірним та тяжким перебігом хронічної обструктивної хвороби легенів (ХОЗЛ), у пацієнтів, які отримували інфліксимаб, було зареєстровано більше злоякісних пухлин, ніж у пацієнтів контрольної групи. і шия. Усі пацієнти в анамнезі були завзятими курцями. Тому слід бути обережним при застосуванні будь-яких антагоністів ФНП у пацієнтів із ХОЗЛ, а також у пацієнтів з підвищеним ризиком злоякісних новоутворень через надмірне куріння.
На основі поточних даних невідомо, чи впливає лікування адалімумабом на ризик розвитку дисплазії або раку товстої кишки. Усі пацієнти з виразковим колітом, які мають підвищений ризик розвитку дисплазії або карциноми товстої кишки (наприклад, пацієнти з тривалим виразковим колітом або первинним склерозуючим холангітом), або які раніше мали дисплазію або рак товстої кишки в анамнезі. дисплазія протягом усього захворювання. Ця оцінка повинна включати колоноскопію та біопсію на основі місцевих рекомендацій.
Реакції, що впливають на систему кровотворення
Повідомлялося про поодинокі випадки панцитопенії, включаючи появу апластичної анемії, після застосування препаратів проти ФНП. Побічні дії, що впливають на систему кровотворення, включаючи значні цитопенії, були зареєстровані у пацієнтів, які отримували препарат Хуміра з медичної точки зору. (наприклад, тромбоцитопенія, лейкопенія). Під час лікування препаратом Хуміра всі пацієнти повинні бути проінформовані про необхідність негайного звернення до лікаря, щоб отримати належну допомогу у разі появи ознак та симптомів, що свідчать про наявність дискразії крові (наприклад, тривала температура, синці, крововиливи, блідість) У разі пацієнтів з підтвердженими значними змінами в системі кровотворення, слід розглянути необхідність припинення терапії препаратом Хуміра.
Щеплення
Подібні реакції антитіл до стандартної 23-валентної пневмококової вакцини та вакцини проти тривалентного вірусу грипу були виявлені у дослідженні за участю 226 дорослих пацієнтів з ревматоїдним артритом, які лікувалися адалімумабом або плацебо. Немає даних. Про вторинну передачу інфекції від живих вакцин у пацієнти, які приймають Хуміру.
Педіатричним пацієнтам рекомендується, по можливості, реалізувати запланований графік щеплень відповідно до чинних вказівок щодо вакцинації перед початком терапії на основі препарату Хуміра.
Пацієнти, які отримують Хуміру, можуть отримувати одночасну вакцинацію, за винятком живих вакцин. Не рекомендується введення живих вакцин немовлятам, які зазнали впливу адалімумабу внутрішньоутробно, протягом 5 місяців після останнього введення матір’ю адалімумабу під час вагітності.
Застійна серцева недостатність
Погіршення застійної серцевої недостатності та асоційованої смертності спостерігалося у клінічному дослідженні з іншим препаратом проти ФНП. Погіршення застійної серцевої недостатності також спостерігалося у пацієнтів, які отримували препарат Хуміра. Пацієнтам з легкою серцевою недостатністю (клас I / II NYHA) слід з обережністю застосовувати Хуміру. Humira протипоказана при помірній або важкій серцевій недостатності (див. Розділ 4.3). Лікування препаратом Humira слід припинити у пацієнтів із погіршенням або новими симптомами застійної серцевої недостатності.
Аутоімунні процеси
Лікування препаратом Хуміра може викликати утворення аутоімунних антитіл. Вплив тривалого лікування Humira на розвиток аутоімунних захворювань невідомий. Якщо після лікування препаратом Humira у пацієнта з’являються симптоми, що свідчать про вовчакоподібний синдром, і позитивний вплив на антитіла до дволанцюгової ДНК, не продовжуйте лікування Humira слід надати (див. розділ 4.8).
Одночасне введення біологічних антагоністів DMARDS або TNF
У клінічних випробуваннях комбінованої терапії з анакінрою та іншим препаратом проти ФНО, етанерцептом, спостерігалися серйозні інфекції, що не мали клінічної користі, порівняно з одним етанерцептом. Враховуючи тип побічних ефектів, що спостерігаються при комбінації анакінри та етанерцепту, подібні побічні ефекти можуть виникнути після комбінації анакінри та іншого препарату проти ФНП. Тому комбінація адалімумабу з анакінрою не рекомендується (див. Розділ 4.5).
Одночасний прийом адалімумабу з іншими біологічними ДМАРДС (наприклад, анакінрою та абатацептом) або іншими антагоністами ФНП не рекомендується через можливий підвищений ризик інфекцій, включаючи серйозні інфекції та інші потенційні лікарські взаємодії (див. Розділ 4.5).
Хірургічні втручання
Існує "обмежений" досвід щодо безпеки хірургічних процедур у пацієнтів, які отримують препарат Хуміра. При плануванні операції слід враховувати тривалий період напіввиведення адалімумабу. Пацієнта, який проходить операцію під час лікування препаратом Хуміра, слід уважно стежити за розвитком інфекцій, і в цьому випадку слід вжити заходів. Існує "обмежений" досвід щодо безпеки у пацієнтів, які проходять операцію з заміни суглобів під час лікування препаратом Хуміра.
Непрохідність тонкої кишки
Невдача відповіді на лікування хвороби Крона може свідчити про наявність жорсткого фіброзного стенозу, який може потребувати операції. Наявні дані свідчать про те, що Humira не погіршує і не викликає стриктур.
Старші люди
Частота серйозних інфекцій серед пацієнтів, які отримували Хуміру, старше 65 років (3,5%), була вищою, ніж пацієнтів віком до 65 років (1,5%). Деякі з них мали смертельний результат. Особливу увагу щодо ризику зараження слід приділяти лікуванню пацієнтів літнього віку.
Педіатричне населення
Див. Вакцинацію вище.
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Терапія Humira вивчалася як монотерапія та у поєднанні з метотрексатом у пацієнтів з ревматоїдним артритом, поліартикулярним ювенільним ідіопатичним артритом та псоріатичним артритом. Утворювання антитіл було нижчим при одночасному застосуванні Humira з метотрексатом, ніж при монотерапії. Введення препарату Хуміра без метотрексату призвело до збільшення утворення антитіл, збільшення кліренсу та зниження ефективності адалімумабу (див. Розділ 5.1).
Поєднання Humira та анакінри не рекомендується (див. Розділ 4.4 «Одночасне застосування біологічних DMARD або антагоністів TNF»).
Поєднання препарату Хуміра та абатацепту не рекомендується (див. Розділ 4.4 «Одночасне застосування біологічних ДМАРД або антагоністів ФНП»).
04.6 Вагітність та лактація
Вагітність
Для Humira доступні обмежені клінічні дані про вагітність, що зазнала впливу.
У дослідженні токсичності розвитку, проведеному на мавпах, не виявлено токсичності для матері, ембріотоксичності чи тератогенності. Немає доклінічних даних про постнатальну токсичність адалімумабу (див. Розділ 5.3).
Через інгібування TNFα введення адалімумабу під час вагітності може перешкоджати нормальній імунній відповіді новонародженого. Тому введення адалімумабу у період вагітності не рекомендується.
Адалімумаб може проникати через плаценту і досягати сироватки крові дітей, народжених від матерів, які отримували адалімумаб під час вагітності. Отже, ці діти піддаються більшому ризику зараження. Не рекомендується введення живих вакцин немовлятам, які зазнали впливу адалімумабу внутрішньоутробно, протягом 5 місяців після останнього введення матір’ю адалімумабу під час вагітності.
Час годування
Невідомо, чи проникає адалімумаб у жіноче молоко або системно всмоктується після прийому всередину.
Однак, оскільки імуноглобуліни людини виділяються з молоком, жінки не повинні годувати грудьми щонайменше п’ять місяців після останнього лікування препаратом Хуміра.
Родючість
Немає доклінічних даних про вплив адалімумабу на фертильність.
Жінки дітородного віку. Контрацепція у чоловіків і жінок
Жінки репродуктивного віку повинні використовувати адекватну контрацепцію для запобігання вагітності та продовжувати її застосування принаймні п’ять місяців після останнього лікування препаратом Хуміра.
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Humira має незначний вплив на здатність керувати автомобілем або працювати з механізмами. Після застосування препарату Хуміра можуть виникнути запаморочення та порушення зору (див. Розділ 4.8).
04.8 Побічні ефекти
Humira вивчали у 8198 пацієнтів у основних контрольованих та відкритих клінічних випробуваннях протягом 60 місяців або довше.Ці дослідження проводилися у пацієнтів з раннім початком та тривалим ревматоїдним артритом, ювенільним ідіопатичним артритом (поліартикулярний ювенільний ідіопатичний артрит та ентезит-асоційований артрит), а також у пацієнтів з осьовим спондилоартритом (анкілозуючий спондилоартрит та осьовий спондилоартрит без рентгенографічних ознак анкілозуючого артриту) ), псоріатичний артрит, хвороба Крона, виразковий коліт та псоріаз. Основні контрольовані дослідження були проведені у 5343 пацієнтів, які отримували Humira, та 3148 пацієнтів, які отримували плацебо або активний компаратор протягом контрольного періоду.
Відсоток пацієнтів, які припинили лікування через побічні ефекти під час подвійного сліпого, контрольованого етапу ключових досліджень, становив 6,1% для пацієнтів, які приймали Хуміру, та 5,7% для пацієнтів, які лікувалися.
Короткий опис профілю безпеки
Найбільш поширеними побічними реакціями є інфекції (такі як назофарингіт, інфекція верхніх дихальних шляхів та синусит), реакції на місці введення (еритема, свербіж, крововилив, біль або набряк), головний біль та м’язово -скелетна біль.
Повідомлялося про серйозні побічні реакції на Humira. Препарати, що блокують TNF, такі як Humira, впливають на імунну систему, і їх застосування може вплинути на захист організму від інфекцій та раку.
Також повідомлялося про випадки смертельних інфекцій (включаючи випадки сепсису, опортуністичних інфекцій та туберкульозу), реактивації інфекції ВГВ та різних видів злоякісних утворень (включаючи випадки лейкемії, лімфоми та гепато-лімфоми) після введення препарату Хуміра. Селезінкова T-HSTCL клітини).
Повідомлялося також про важкі гематологічні, неврологічні та аутоімунні реакції. Останні включають рідкісні випадки панцитопенії, апластичної анемії, подій центральної та периферичної демієлінізації та випадки вовчака, пов’язаних з вовчаком станів та синдрому Стівенса-Джонсона.
Педіатричне населення
Побічні ефекти у педіатричних пацієнтів
Загалом, побічні ефекти у педіатричних пацієнтів були подібними до тих, що спостерігалися у дорослих пацієнтів, як за частотою, так і за типом.
Таблиця зі списком побічних реакцій
Нижче наведений перелік побічних реакцій ґрунтується на досвіді клінічних випробувань та постмаркетинговому досвіді та класифікований за системою / органом та частотою (дуже часто ≥ 1/10; часто ≥ 1/100 до
Таблиця 2
Побічні ефекти
* Інша інформація міститься у розділах 4.3, 4.4 та 4.8
** включаючи відкриті розширені дослідження
1) включаючи дані зі спонтанних звітів
Опис окремих побічних реакцій
Реакції в місці ін’єкції
У основних контрольованих клінічних випробуваннях у дорослих та дітей у 13,6% пацієнтів, які отримували Humira, виникали реакції на місці ін’єкції (еритема та / або свербіж, крововилив, біль чи набряк), проти 7,6% пацієнтів, які отримували плацебо або активний контроль. як правило, не вимагало відміни препарату.
Інфекції
У основних контрольованих клінічних випробуваннях у дорослих та дітей рівень інфекції становив 1,52 на пацієнта / рік у групі Humira та 1,45 на пацієнта / рік у групах плацебо та активного контролю. Інфекції були переважно представлені назофарингітом, інфекціями верхніх дихальних шляхів та інфекція сечовивідних шляхів. Більшість пацієнтів продовжували приймати Хуміру після зникнення інфекції.
Частота серйозних інфекцій становила 0,04 на пацієнта на рік у групі препарату Хуміра та 0,03 на пацієнта на рік у групах плацебо та групи активного контролю.
У контрольованих та відкритих дослідженнях з Humira у дорослих та дітей повідомлялося про серйозні інфекції (включаючи смертельні інфекції, які траплялися рідко), включаючи повідомлення про випадки туберкульозу (включаючи міліарні та позалегеневі місця) та інвазивні опортуністичні інфекції ( наприклад, розповсюджений або позалегеневий гістоплазмоз, бластомікоз, кокцидіоїдомікоз, пневмоцистоз, кандидоз, аспергільоз та лістеріоз). Більшість випадків туберкульозу сталося протягом перших восьми місяців після початку терапії і їх можна інтерпретувати як поновлення прихованої хвороби.
Новоутворення та лімфопроліферативні захворювання
У дослідженнях, проведених при введенні Humira пацієнтам з ювенільним ідіопатичним артритом (поліартикулярний ювенільний ідіопатичний артрит та ентезит-асоційований артрит), злоякісних пухлин у 249 педіатричних пацієнтів з експозицією 655,6 пацієнтних років не спостерігалося. пацієнти з експозицією 258,9 пацієнто-років під час дослідження, що вводили Хуміру педіатричним пацієнтам з хворобою Крона.
У контрольованих розділах основних досліджень для дорослих з Humira тривалістю щонайменше 12 тижнів у пацієнтів з помірним та важким активним ревматоїдним артритом, анкилозирующим спондилоартритом, осьовим спондилоартритом без рентгенографічних ознак хвороби Бехтерева, псоріатичним артритом, псоріазом, хворобою Крона та виразковим колітом, новоутвореннями а також лімфому та немеланотичний рак шкіри спостерігалися зі швидкістю (95% -й довірчий інтервал) 6,0 (3,7, 9,8) на 1000 пацієнто-років серед 4622 пацієнтів, які отримували Humira до коефіцієнт 5,1 (2,4, 10,7) на 1000 пацієнто-років у 2828 контрольних пацієнтів (середня тривалість лікування становила 5,1 місяця для пацієнтів, які отримували Humira, та 4,0 місяці для пацієнтів, які пройшли обстеження). Частота (95% довірчий інтервал) немеланотичного раку шкіри становила 9,7 (6,6; 14,3) на 1000 пацієнто-років у пацієнтів, які отримували Humira, і 5,1 (2,4; 10, 7) на 1000 пацієнто-років у контрольних пацієнтів. З цих видів раку шкіри плоскоклітинні карциноми виникали з частотою (95% -й довірчий інтервал) 2,6 (1,2; 5,5) на 1000 пацієнто-років у пацієнтів, які отримували Humira, і 0,7 (0,1; 5,2) на 1000 пацієнто-років у контрольних пацієнтів. Частота (95% -й довірчий інтервал) лімфом становила 0,7 (0,2, 3,0) на 1000 пацієнто-років у пацієнтів, які отримували Humira, і 1,5 (0,4, 5,8) на 1000 пацієнт-років у контрольних пацієнтів.
Якщо об’єднати частини цих досліджень, як поточні, так і завершені відкриті розширені дослідження із середньою тривалістю приблизно 3,4 року, включаючи 5 727 пацієнтів та понад 24 568 пацієнто-років терапії, спостерігаються новоутворення, крім лімфом та немеланотичних рак шкіри, становить приблизно 8,8 на 1000 пацієнто-років. Частота немеланотичного раку шкіри становить приблизно 10,3 на 1000 пацієнто-років, а лімфом-приблизно 1,4 на 1000 пацієнто-років.
У постмаркетинговому досвіді з січня 2003 р. По грудень 2010 р., Переважно у пацієнтів з ревматоїдним артритом, зареєстрована кількість злоякісних пухлин становить приблизно 2,7 на 1000 лікування / пацієнтний рік. Повідомляється, що показники немеланотичного раку шкіри та лімфом становлять приблизно 0,2 та 0,3 на 1000 лікування / пацієнтний рік відповідно (див. Розділ 4.4).
У постмаркетинговому дослідженні повідомлялося про поодинокі випадки гепатоспленочної Т-клітинної лімфоми у пацієнтів, які отримували адалімумаб (див. Розділ 4.4).
Аутоантитіла
У IV дослідженнях з ревматоїдного артриту зразки сироватки крові пацієнта неодноразово перевіряли на наявність аутоантитіл. позитивні значення на 24-му тижні. У двох із 3441 пацієнтів, які лікувалися препаратом Хуміра при всіх ревматоїдних артритах та псоріатичних артритах, виявили клінічні ознаки, що свідчать про початок вовчакоподібного синдрому. системні симптоми.
Печінково-жовчні події
У контрольованих клінічних випробуваннях 3-ї фази Humira у пацієнтів з ревматоїдним артритом та псоріатичним артритом з тривалістю контрольного періоду від 4 до 104 тижнів підвищення рівня трансаміназ АЛТ, що перевищувало або дорівнювало у 3 рази, перевищувало максимальне нормальне значення у 3,7% пацієнтів з препаратом Хуміра пацієнтів, які отримували лікування, та 1,6% пацієнтів, які отримували контроль.
У контрольованих клінічних випробуваннях 3-ї фази Humira у пацієнтів з бляшковим псоріазом з тривалістю контрольного періоду від 12 до 24 тижнів підвищення рівня трансаміназ АЛТ, що перевищує або дорівнює 3-кратному максимальному нормальному значенню, спостерігалося у "1,8% пацієнтів, які отримували Хуміру, і 1,8% % контрольних пацієнтів.
У контрольованих клінічних випробуваннях 3-ї фази Humira у пацієнтів з поліартикулярним ювенільним ідіопатичним артритом у віці від 4 до 17 років та у пацієнтів з артритом, асоційованим з ентезитом, у віці від 6 до 17 років, підвищення АЛТ більше або дорівнює 3-кратному ВГН зустрічалися у 6,1% пацієнтів, які отримували Хуміру, та 1,3% пацієнтів, які отримували контроль. Більшість підвищення рівня трансаміназ АЛТ відбувалося при одночасному застосуванні метотрексату. У клінічному дослідженні 3 -ї фази Humira у пацієнтів з поліартикулярним ювенільним ідіопатичним артритом фази 3 не спостерігалося підвищення рівня АЛТ -трансаміназ ≥ 3 -кратного ВМН.
У контрольованих клінічних випробуваннях 3-ї фази Humira у пацієнтів з хворобою Крона та виразковим колітом з контрольним періодом від 4 до 52 тижнів підвищення рівня АЛТ, що перевищувало або дорівнювало 3-кратному максимальному нормальному значенню, спостерігалося у 0,9% пацієнтів, які отримували Humira та 0,9% пацієнтів, які отримували контроль.
У дослідженні 3-ї фази Humira у педіатричних пацієнтів з хворобою Хрона, яке оцінювало безпеку та ефективність двох режимів доз з коригуванням ваги для підтримуючої терапії після індукційної терапії з коригуванням ваги до 52 тижнів, рівень АЛТ ≥ 3 x ГМН був виявлений у 2,6% усіх пацієнтів, які зазнали одночасного лікування базовими імунодепресантами.
У клінічних випробуваннях, за всіма ознаками, пацієнти з підвищеними рівнями трансаміназ були безсимптомними, а підвищення були тимчасовими і зникали під час лікування в більшості випадків. Однак, постмаркетингові випадки печінкової недостатності, а також менш тяжкі порушення печінки, які можуть передувати печінковій недостатності, такі як гепатит, включаючи аутоімунний гепатит, також були зареєстровані у пацієнтів, які отримували адалімумаб.
Одночасне лікування азатіоприном / 6-меркаптопурином
У дослідженнях хвороби Крона у дорослих спостерігалася більша частота побічних явищ, пов’язаних із серйозними інфекціями та злоякісними утвореннями, при поєднанні препарату Хуміра та азатіоприн / 6-меркаптопурин порівняно з одним препаратом Хуміра.
Повідомлення про підозрювані побічні реакції
Повідомлення про підозрювані побічні реакції, що виникають після реєстрації лікарського засобу, є важливими, оскільки вони дозволяють постійно контролювати співвідношення користь / ризик лікарського засобу. , веб -сайт: http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Передозування
Під час клінічних досліджень не було виявлено дозозалежної токсичності. Найвища оцінена доза - багаторазові дози 10 мг / кг внутрішньовенно; ця доза еквівалентна приблизно 15 -кратній рекомендованій дозі.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: Селективні імуносупресивні засоби. Код ATC: L04AB04
Механізм дії
Адалімумаб вибірково зв'язується з ФНП і нейтралізує його біологічну функцію, блокуючи його взаємодію з рецепторами ФНП клітинної мембрани, р55 і р75.
Адалімумаб також модулює біологічні реакції, які індукуються або регулюються TNF, включаючи зміни рівнів молекул адгезії, відповідальних за міграцію лейкоцитів (ELAM-1, VCAM-1 та ICAM-1 з IC50 0,1-0, 2 нМ).
Фармакодинамічні ефекти
Після лікування препаратом Humira у пацієнтів з ревматоїдним артритом у порівнянні з базальним спостерігалося швидке зниження білків гострої фази, показників запалення (С -реактивний білок -PCR, швидкість осідання еритроцитів -VES) та сироваткових цитокінів (IL -6). Сироваткові рівні матриксних металопротеїназ (ММР-1 та ММР-3), які беруть участь у ремоделюванні тканин, що відповідають за руйнування хряща, також були знижені після введення препарату Хуміра. Пацієнти, які отримували препарат Хуміра, загалом показали поліпшення біохімічних ознак хронічного запалення.
Швидке зниження рівня СРБ (С -реактивного білка) також спостерігалося у пацієнтів з поліартикулярним ювенільним ідіопатичним артритом, хворобою Крона та виразковим колітом після лікування препаратом Хуміра. Ендоскопічні дослідження слизової оболонки кишечника показали загоєння слизової у пацієнтів, які отримували адалімумаб.
Клінічна ефективність та безпека
Ювенільний ідіопатичний артрит (ЮІА)
Поліартикулярний ювенільний ідіопатичний артрит (pJIA)
Безпеку та ефективність препарату Humira оцінювали у двох дослідженнях (pJIA I та II) у дітей з активним поліартикулярним або поліартикулярним перебігом ювенільного ідіопатичного артриту, які мали різні типи початку ЮІА (найчастіше негативний чи позитивний ревматоїдний фактор та поліартрит з обширною формою олігоартриту).
pJIA-I
Безпеку та ефективність Humira оцінювали у багатоцентровому рандомізованому подвійному сліпому дослідженні з паралельними групами у 171 дитині (віком 4-17 років) з поліартикулярним ювенільним ідіопатичним артритом (ЮІА). = OL LI, пацієнти були стратифіковані на дві групи: групу МТХ (метотрексату) та групу, що не отримувала МТХ. Група, яка не отримувала МТХ, ніколи раніше не лікувалася МТХ або припинила прийом МТХ принаймні за два тижні до введення досліджуваного препарату. Пацієнтам давали постійні дози нестероїдних протизапальних препаратів (НПЗЗ) та / або преднізолону (≤0,2 мг / кг / добу або максимум 10 мг / добу). м2 до максимальної дози 40 мг через тиждень протягом 16 тижнів Розподіл пацієнтів за віком та мінімальною, середньою та максимальною дозою, що вводиться під час фази ОЛ ЛІ, наведено у Таблиці 3.
Таблиця 3
Розподіл пацієнтів за віком та дозою адалімумабу, що вводиться під час фази ПРЛ
Пацієнти, які продемонстрували педіатричну відповідь на ACR30 на 16 -му тижні, мали право бути рандомізованими у фазу подвійної сліпоти (DB) і отримували Humira 24 мг / м2 максимум до 40 мг або плацебо. Кожні два тижні протягом додаткових 32 тижнів або до захворювання спалахувати. Критерії визначення загострення хвороби були визначені на основі погіршення, яке перевищувало або дорівнювало 30% (≥ 30%) у порівнянні з вихідним значенням 3 або більше з 6 основних критеріїв "ядра ACR для дітей", у наявність 2 або більше активних суглобів і на основі поліпшення більш ніж на 30% не більше ніж у 1 із вищезазначених критеріїв 6. Після 32 тижнів або після загострення хвороби пацієнти вважалися правомочними бути госпіталізованими відкрита фаза розширення.
Таблиця 4
Відповідь PedACR 30 під час дослідження JIA
відповіді PedACR 30/50/70 на 48 тижні були значно вищими, ніж ті, що були досягнуті у пацієнтів, які отримували плацебо
b p = 0,015
c р = 0,031
Серед тих, хто відповів на лікування на 16 -му тижні (n = 144), відповіді Ped ACR 30/50/70/90 зберігалися протягом шести років під час фази OLE у пацієнтів, які отримували Humira протягом усієї студії. В цілому 19 пацієнтів, у тому числі 11 з базової групи у віці від 4 до 12 років та 8 з базової групи у віці від 13 до 17 років, проходили лікування протягом 6 років і більше.
Загалом відповіді були краще І у кількох пацієнтів розвинулися антитіла при лікуванні комбінованою терапією Humira та MTX порівняно з лікуванням Humira, що застосовується окремо. Беручи до уваги ці результати, застосування препарату Хуміра рекомендується у поєднанні з МТХ та як монотерапія пацієнтам, яким застосування МТХ не рекомендується (див. Розділ 4.2).
pJIA II
Безпеку та ефективність Humira оцінювали у відкритому багатоцентровому дослідженні у 32 дітей (2-2 площі поверхні тіла Humira до максимум 20 мг через тиждень у вигляді одноразової підшкірної дози протягом щонайменше 24 тижнів. у дослідженні більшість суб’єктів одночасно використовували МТХ, деякі з них повідомляли про застосування кортикостероїдів або нестероїдних протизапальних препаратів (НПЗЗ).
На 12 -му та 24 -му тижнях відповідь на PedACR30 становила 93,5% та 90,0% відповідно, використовуючи підхід до спостережень. Пропорції суб’єктів із PedACR50 / 70/90 на 12 -му та 24 -му тижнях становили відповідно 90,3% / 61,3%. / 38,7% та 83,3% / 73,3% / 36,7%. Серед тих, хто відповів (PedACR30) на 24 тижні (n = 27 із 30 пацієнтів), відповіді PedACR30 зберігалися протягом 60 тижнів у пацієнтів, які отримували Humira протягом цього періоду на відкритому повітрі -дослідження подовження етикетки. Загалом 20 суб’єктів лікувалися протягом 60 тижнів або довше.
Артрит, пов'язаний з ентезитом
Безпеку та ефективність Humira оцінювали у багатоцентровому рандомізованому подвійному сліпому дослідженні у 46 педіатричних пацієнтів (віком від 6 до 17 років) з помірним ентезитом, асоційованим з артритом. площі, максимум до 40 мг, або плацебо кожні два тижні протягом 12 тижнів. Після подвійного сліпого періоду слідував відкритий період дослідження, протягом якого пацієнти отримували Humira 24 мг / м2 площі поверхні тіла, до максимум 40 мг підшкірно кожні два тижні протягом додаткових 192 тижнів. Первинною кінцевою точкою була відсоткова зміна кількості суглобів з активним артритом від початкової до 12 тижня (набряк не через деформацію або суглобів із втратою руху плюс біль та / або ніжність), і це було досягнуто із середнім відсотковим зменшенням -62,6% (середня зміна відсотка - 88,9%) у пацієнтів у групі Humira проти -11,6%(середній відсоток зміни - 50,0%) у пацієнтів у групі плацебо. Поліпшення кількості активних суглобів з артритом зберігалося протягом відкритого періоду дослідження до 52 тижня. Хоча це не є статистично значущим, більшість пацієнтів продемонстрували клінічне поліпшення у вторинній кінцевій точці, наприклад кількість місць ентезиту , кількість хворобливих суглобів (TJC), кількість набряклих суглобів (SJC), відповідь ACR 50 у дітей та відповідь ACR 70 у дітей.
Ревматоїдний артрит у дорослих
У всіх клінічних випробуваннях ревматоїдного артриту Humira оцінювали у більш ніж 3000 пацієнтів.Ефективність та безпечність Humira оцінювали у п'яти рандомізованих подвійно сліпих добре контрольованих дослідженнях. Деякі пацієнти лікувалися до 120 місяців.
Дослідження РА I було проведено у 271 пацієнта віком ≥ 18 років з ревматоїдним артритом середньої та важкої форми, стійким до щонайменше одного ДМАРД, включаючи метотрексат, у дозах від 12,5 до 25 мг (10 мг при непереносимості метотрексату) на тиждень і у яких доза метотрексату залишалася постійний при 10-25 мг на тиждень. Humira 20, 40 або 80 мг або плацебо отримували кожні два тижні протягом 24 тижнів.
Дослідження AR II досліджувало 544 пацієнта у віці ≥ 18 років з ревматоїдним артритом середньої та важкої форми з недостатньою відповіддю щонайменше на один препарат DMARD. Дози Humira у 20 або 40 мг вводили шляхом підшкірної ін’єкції кожні два тижні з плацебо кожні два тижні або щотижня протягом 26 тижнів; плацебо призначали щотижня однаково. Використання інших DMARD не допускалося.
У дослідженні AR III взяли участь 619 пацієнтів віком ≥ 18 років із середнім та важким активним ревматоїдним артритом з неадекватною відповіддю на терапію метотрексатом у дозах від 12,5 до 25 мг або з непереносимістю до 10 мг метотрексату щотижня. У цьому дослідженні було сформовано 3 групи. Перший отримував ін’єкції плацебо щотижня протягом 52 тижнів. Другий отримував Хуміру по 20 мг на тиждень протягом 52 тижнів, а третій - 40 мг кожні два тижні та ін’єкції плацебо через тиждень. Після закінчення перших 52 тижнів 457 пацієнтів були включені у відкриту фазу подовження, в якій Humira / MTX вводили у дозі 40 мг через тиждень протягом 10 років.
Дослідження AR IV вперше оцінило безпеку застосування Humira у 636 пацієнтів з помірним та важким активним ревматоїдним артритом у віці ≥ 18 років. Досліджена популяція складалася з обох пацієнтів, які ніколи не отримували ДМАРД, та пацієнтів, які продовжували вже існуючу протиревматичну терапію за умови, що вона була стабільною мінімум 28 днів. Ці методи лікування включають метотрексат, лефлуномід, гідроксихлорохін, сульфасалазин та / або солі золота.
Дослідження V AR оцінювало 799 дорослих пацієнтів, які ніколи раніше не лікувалися метотрексатом і мали середньотяжкий до важкий ранній активний ревматоїдний артрит (середня тривалість захворювання менше 9 місяців). У цьому дослідженні оцінювалася ефективність препарату Хуміра 40 мг, що вводився раз на тиждень у поєднанні з метотрексатом, 40 мг Хуміра як монотерапія кожні два тижні та метотрексату окремо для зменшення ознак та симптомів захворювання та індексу прогресування пошкоджень суглобів, викликаних ревматоїдним артритом, для 104 тижні.
Первинною кінцевою точкою досліджень AR, I, II, III та вторинними кінцевими точками AR IV була оцінка частки пацієнтів, які досягли відповіді ACR 20 на 24 або 26 тижні. Первинною кінцевою точкою дослідження AR V була оцінка відсотка пацієнтів, які досягли відповіді ACR 50 на 52 -му тижні. Крім того, дослідження III та V AR мали основну мету продемонструвати пригнічення прогресування захворювання (за допомогою рентгенографічних досліджень) на 52 -му тижні. демонструючи покращену якість життя.
Відповідь ACR
Відсотки пацієнтів, які отримували Humira, які досягли ACR 20, 50 та 70 відповідей, були порівнянними у дослідженнях ІР, ІІ та ІІІ АР. Результати лікування 40 мг кожні два тижні узагальнено у Таблиці 5.
У дослідженнях РА I -IV усі параметри оцінювалися для визначення відповіді на АКР (кількість хворобливих і набряклих суглобів, оцінка активності захворювання лікарем і пацієнтом, оцінка болю пацієнтом, індекс інвалідності - HAQ) та значення CRP (Мг / дл) покращився на 24 або 26 тижні порівняно з плацебо. У дослідженні AR III ці поліпшення зберігалися протягом 52 тижнів.
На відкритій фазі продовження дослідження AR III більшість пацієнтів, які відчули відповідь на ACR, зберігали відповідь, продовжуючи лікування протягом 10 років. З 207 пацієнтів 114 продовжували приймати Хуміру по 40 мг через тиждень протягом 5 років. З них 86 пацієнтів (75,4%) мали відповіді ACR 20; 72 пацієнти (63,2%) мали відповіді ACR 50; і 41 пацієнт (36%) отримав відповіді ACR 70. З 207 пацієнтів 81 продовжив лікування препаратом Хуміра 40 мг через тиждень протягом 10 років. З них 64 пацієнти (79,0%) мали відповіді ACR 20; Відповіді ACR 50 мали 56 пацієнтів (69,1%); а 43 пацієнти (53,1%) мали відповіді ACR 70.
У IV дослідженні РА відповідь ACR 20 у пацієнтів, які отримували Хуміру, у поєднанні зі звичайною терапією була статистично достовірно кращою, ніж у пацієнтів, які отримували плацебо у поєднанні з традиційними препаратами (p
У дослідженнях РА I-IV пацієнти, які отримували Humira, досягли статистично достовірно вищих відповідей ACR 20 і 50, ніж плацебо, вже через 1-2 тижні після початку лікування.
У дослідженні РА у пацієнтів з раннім ревматоїдним артритом, які раніше ніколи не отримували лікування метотрексатом, комбінована терапія Гумірою / метотрексатом призвела до більш швидкої та значно більшої відповіді на АКР, ніж при монотерапії метотрексатом та монотерапії Хумірою на 52 тижні, і ці реакції зберігалися протягом 104 тижнів ( див. таблицю 6).
На 52 тижні 42,9% пацієнтів, які отримували комбіновану терапію препаратом Хуміра / метотрексат, досягли клінічної ремісії (DAS28
Рентгенологічна реакція
У дослідженні АР III, в якому пацієнти, які отримували Хуміру, мали середню тривалість захворювання приблизно 11 років, структурні пошкодження оцінювали рентгенологічно і виражали як зміну модифікованого загального гострого бала (TSS) та пов'язаних з ним компонентів, ерозії та звуження суглобового простору Індекси (JSN). Пацієнти, які отримували Humira / MTX, продемонстрували значно меншу рентгенологічну прогресію, ніж пацієнти, які отримували тільки MTX, у 6 та 12 місяців (див. Таблицю 7).
У відкритому продовженні III дослідження AR, зменшення швидкості прогресування структурного пошкодження зберігається протягом 8 та 10 років у підгрупі пацієнтів. Серед інших тижнів серед них 48 пацієнтів не виявили прогресування структурних пошкоджень, що визначаються зміною mTSS на 0,5 або менше від вихідного рівня. Через 10 років 79 із 207 пацієнтів, які спочатку отримували препарат Хуміра 40 мг через тиждень, з них 40 пацієнтів не демонструють прогресування структурних пошкоджень, визначених зміною mTSS на 0,5 або менше від вихідного рівня.
Таблиця 7
Середня рентгенографічна зміна після 12 місяців у дослідженні АР III
до метотрексату
b 95% довірчий інтервал для відмінностей у зміні індексу між метотрексатом та Humira.
c На основі аналізу рангів.
d Спільне звуження простору (зменшення суглобової щілини).
У дослідженні AR, V, структурні пошкодження суглобів оцінювались рентгенологічно і виражаються через зміну модифікованого загального балу Sharp (див. Таблицю 8).
Після 52 тижнів та 104 тижнів лікування частка пацієнтів, які не прогресували (зміна від вихідного рівня у зміненому загальному чіткому балі ≤ 0,5), була значно вищою при комбінованій терапії препаратом Гуміра / метотрексат (63,8% та 61,2% відповідно) у порівнянні з монотерапією метотрексатом. (37,4% та 33,5% відповідно, стор
Якість життя та фізичні функції
Якість життя та фізичні функції були оцінені за допомогою індексу інвалідності, отриманого за допомогою Анкети оцінки стану здоров’я (HAQ), у чотирьох оригінальних, адекватних та добре контрольованих дослідженнях, і це було однією з основних кінцевих точок дослідження ІІІ ІІ на 52-му тижні. Схеми Humira у чотирьох дослідженнях показали статистично значуще покращення індексу інвалідності HAQ між початковим та 6 -м місяцями порівняно з плацебо, а в дослідженні ІІ АР той самий результат спостерігався на 52 -му тижні. Форма дослідження здоров'я (SF -36) у чотирьох дослідженнях підтверджує ці висновки для всіх схем дозування Humira зі статистично значущими результатами. Щодо показників фізичної активності, болю та самопочуття, зареєстрованих за допомогою Humira 40 мг на тиждень чергуються. Статистично значуще зменшення почуття втоми, як показали показники функціональної оцінки, що стосується лікування хронічних захворювань (FACIT), було виявлено у всіх трьох дослідженнях, в яких його оцінювали (дослідження AR I, III, IV).
У дослідженні AR III більшість суб’єктів, які досягли поліпшення фізичної функції та продовжували лікування, зберігали поліпшення протягом 520 тижнів (120 місяців) відкритого лікування. Поліпшення якості життя вимірювалося до 156 тижня (36 місяців), і покращення зберігалося з плином часу.
У дослідженні АР V індекс інвалідності, оцінений на основі HAQ та фізичної складової SF 36, показав найкраще поліпшення (p
Хвороба Крона у педіатричних пацієнтів
Humira тестували у багатоцентровому рандомізованому подвійному сліпому клінічному дослідженні, призначеному для оцінки ефективності та безпеки залежно від ваги дозозалежного індукційного та підтримуючого лікування (30. Суб’єкти, напевно, не пройшли звичайну терапію (включаючи кортикостероїд та / або імуномодулятор) ) для компакт -дисків, і суб’єкти, можливо, раніше втратили відповідь або мали непереносимість інфліксимабу.
Усі суб’єкти отримували відкриту індукційну терапію з дозою, виходячи з ваги їхньої маси тіла на вихідному рівні: 160 мг на 0 тижні та 80 мг на 2 тижні для суб’єктів з масою тіла ≥ 40 кг та 80 мг та 40 мг відповідно.
На 4 -му тижні, виходячи з маси тіла, випробовувані були рандомізовані 1: 1 до схеми підтримки низької дози або стандартної дози, як показано в таблиці 9.
Результати ефективності
Первинною кінцевою точкою дослідження була клінічна ремісія на 26 тижні, визначена за шкалою PCDAI ≤ 10.
Частота клінічної ремісії та клінічної відповіді (визначена як зниження балів за PCDAI щонайменше на 15 балів від вихідного рівня) наведена у Таблиці 10. Частота припинення прийому кортикостероїдів або імуномодуляторів наведена у Таблиці 11.
Статистично значуще збільшення (поліпшення) індексу маси тіла та швидкості зростання від вихідного рівня до 26 та 52 тижнів спостерігалося для обох груп лікування.
Статистично та клінічно значущі поліпшення показників якості життя від вихідного рівня (включаючи IMPACT III) також були відзначені в обох групах лікування.
Хвороба Крона у дорослих
Безпеку та ефективність препарату Humira оцінювали у більш ніж 1500 пацієнтів з помірною та тяжкою активністю хвороби Крона (Індекс активності хвороби Крона (CDAI) ≥ 220 та ≤ 450) у рандомізованих, подвійних сліпих, плацебо-контрольованих дослідженнях. Допускалося одночасне введення постійних доз аміносаліцилатів, кортикостероїдів та / або імуномодулюючих засобів, і 80% пацієнтів продовжували приймати принаймні один із цих препаратів.
Індукція клінічної ремісії (визначається як CDAI
Підтримку клінічної ремісії оцінювали у дослідженні CD CD III (CHARM). У III дослідженні CD 854 пацієнти отримували відкриту Humira 80 мг на 0-му тижні і 40 мг на 2-му тижні. На 4-му тижні пацієнти були рандомізовані на 40 мг щотижня, 40 мг на тиждень або плацебо; загальна тривалість дослідження склала 56 тижнів. Пацієнтів, у яких на 4 -му тижні спостерігалася адекватна клінічна відповідь (зниження CDAI ≥ 70), проводили стратифікацію та аналізували окремо від тих, у кого не було адекватної клінічної відповіді на 4 -му тижні. Допускалося поступове зниження дози. Кортикостероїди після 8 -го тижня.
Швидкість індукції клінічної ремісії та відповіді з дослідження CD I та II дослідження CD наведено у таблиці 12.
Подібні показники ремісії спостерігалися у групі індукційних доз 160/80 мг та 80/40 мг на 8 -му тижні, а побічні ефекти частіше виникали у групі доз 160/80 мг. 80 мг.
У III дослідженні CD, на 4 тижні 58 % (499/854) пацієнтів зазнали адекватної клінічної відповіді та були оцінені в первинному аналізі. Відсотки для підтримки ремісії та клінічної відповіді наведені в Таблиці 13. Результати клінічної ремісії залишалися відносно постійними, незалежно від попереднього впливу протинаркотичних препаратів.
На 56 тижні госпіталізації та операції, пов’язані з хворобами, статистично достовірно зменшилися при застосуванні адалімумабу порівняно з плацебо.
Серед пацієнтів, які не виявили адекватної відповіді на 4 -му тижні, 43% пацієнтів, які отримували підтримуючу терапію Humira, відчули адекватну відповідь до 12 -го тижня порівняно з 30% пацієнтів, які отримували плацебо. Ці результати свідчать про те, що деякі пацієнти, які не виявили адекватної відповіді на 4 -му тижні, отримують користь від продовження підтримуючої терапії до 12 -го тижня.
117/276 пацієнтів з І дослідження CD та 272/777 пацієнтів з II та III досліджень CD спостерігалися протягом щонайменше 3 років відкритої терапії адалімумабом. 88 та 189 пацієнтів відповідно продовжували підтримувати клінічну ремісію. Клінічна відповідь (CR-100) зберігалася відповідно у 102 та 233 пацієнтів.
Якість життя
У дослідженнях CD I та CD II статистично значуще поліпшення загального балу опитувальника запальних захворювань кишечника (IBDQ) було досягнуто на 4-му тижні у пацієнтів, рандомізованих до препарату Хуміра 80/40 мг та 160/80 мг у порівнянні з плацебо, і спостерігалося при тиждень 26 та 56 у дослідженні D III, а також між групами лікування Humira порівняно з групою плацебо
Імуногенність
Утворення антиадалімумабних антитіл пов'язане зі збільшенням кліренсу та зниженням ефективності адалімумабу. Немає очевидної кореляції між наявністю антитіл до адалімумабу та виникненням побічних явищ.
У поліартикулярних ювенільних ідіопатичних артритів у віці 4-17 років антиадалімумабні антитіла були виявлені у 15,8% пацієнтів (27/171), які отримували адалімумаб. У пацієнтів, які не отримували метотрексат разом з Humira, частота склала 25,6% (22/86) проти 5,9% (5/85) при одночасному застосуванні адалімумабу з метотрексатом.
У пацієнтів з ентезит-асоційованим артритом антиадалімумабні антитіла були виявлені у 10,9% (5/46) пацієнтів, які отримували адалімумаб. У пацієнтів, які не отримували метотрексат одночасно з Humira, частота становила 13,6% (3/22), порівняно з 8,3% (2/24), коли адалімумаб застосовувався у поєднанні з метотрексатом.
Пацієнтів, які брали участь у дослідженнях ревматоїдного артриту, протягом різних періодів часу перевіряли на наявність антитіл до адалімумабу протягом 6-12 місяців. У ключових клінічних випробуваннях антитіла до адалімумабу були виявлені у 5,5% (58/1053) пацієнтів, які отримували адалімумаб, з 0,5% (2/370) пацієнтів, які отримували плацебо.У пацієнтів, яким одночасно не призначали метотрексат, частота становила 12,4% порівняно з 0,6% при одночасному застосуванні адалімумабу з метотрексатом.
Оскільки аналізи імуногенності є специфічними для конкретного продукту, порівняння кількості антитіл з іншими продуктами недоцільно.
05.2 Фармакокінетичні властивості
Поглинання та розподіл
Після підшкірного введення 24 мг / м2 (максимум 40 мг) через тиждень пацієнтам у віці від 4 до 17 років з поліартикулярним ювенільним ідіопатичним артритом (ЮІА) середнє мінімальне рівноважне значення концентрації адалімумабу в сироватці крові (виміряні значення починаючи з 20 тижня) до 48) становив 5,6 ± 5,6 мкг / мл (102% CV) з адалімумабом без одночасного застосування метотрексату та 10,9 ± 5,2 мкг / мл (47, 7% CV) одночасно з метотрексатом.
У пацієнтів з поліартикулярною ЮІА у віці від 2 до 2 років середня рівноважна концентрація адалімумабу в сироватці крові становила 6,0 ± 6,1 мкг / мл (101% CV) з адалімумабом без одночасного застосування метотрексату та 7,9 ± 5,6 мкг / мл (71,2% CV) при одночасному застосуванні з метотрексатом.
Після підшкірного введення 24 мг / м2 (максимум 40 мг) через тиждень пацієнтам віком 6-17 років з артритом, асоційованим з ентезитом, середнє мінімальне значення концентрації адалімумабу у сироватці крові у рівноважному стані (виміряні значення На 24 тижні) були 8,8 ± 6,6 мкг / мл з адалімумабом без одночасного застосування метотрексату та 11,8 ± 4,3 мкг / мл при одночасному застосуванні з метотрексатом.
У педіатричних пацієнтів з помірним та тяжким КБ індукційна доза відкритого адалімумабу становила 160/80 мг або 80/40 мг на 0 та 2 тижнях відповідно, залежно від граничного значення маси тіла при 40 кг. На 4 -му тижні пацієнти були рандомізовані 1: 1 на основі маси тіла до групи стандартної дози (40/20 мг через тиждень) або низької дози (20/10 мг через тиждень). Середні (± SD) сироваткові концентрації мінімальних рівнів адалімумабу, досягнутих на 4 тижні, становили 15,7 ± 6,6 мг / мл для пацієнтів ≥ 40 кг (160/80 мг) та 10,6 ± 6,1 мг / мл для пацієнтів
Для пацієнтів, які перебували на рандомізованій терапії, середні (± SD) мінімальні концентрації адалімумабу на 52 тижні становили 9,5 ± 5,6 мг / мл для групи зі стандартною дозою та 3,5 ± 2,2 мг / мл для групи з низькими дозами. Середні мінімальні концентрації зберігалися у пацієнтів, які продовжували лікування адалімумабом кожні два тижні протягом 52 тижнів. Для пацієнтів, які збільшували дозу з альтернативного тижня до тижневого режиму, середня (± SD) сироваткова концентрація адалімумабу на 52 тижні становила 15,3 ± 11,4 мкг / мл (40/20 мг, на тиждень) та 6,7 ± 3,5 мкг / мл (20/10 мг на тиждень).
Дорослі
Після підшкірного введення одноразової дози 40 мг всмоктування та розподіл адалімумабу відбувалося повільно, пікові концентрації в сироватці крові спостерігалися приблизно через 5 днів після введення. Середня абсолютна біодоступність адалімумабу у трьох дослідженнях після однієї дози підшкірної дози 40 мг становила 64 %. Після одноразових внутрішньовенних доз від 0,25 до 10 мг / кг концентрації були пропорційними дозі. Після доз 0,5 мг / кг (≈40 мг) кліренс коливався від 11 до 15 мл / год, об'єм розподілу (Vss) коливався від 5 до 6 літрів, а середній період напіввиведення заключної фази становив приблизно два тижні. Концентрація адалімумабу в синовіальній рідині у різних пацієнтів з ревматоїдним артритом коливалася від 31 до 96% від такої у сироватці крові.
Після підшкірного введення адалімумабу у дозі 40 мг кожні два тижні у дорослих пацієнтів з ревматоїдним артритом (РА) мінімальна концентрація становила в середньому приблизно 5 мг / мл (без супутнього метотрексату) та 8-9 мг / мл (у поєднанні з метотрексатом). Рівні адалімумабу у рівновазі після підшкірних доз 20, 40 та 80 мг кожні 2 тижні або щотижня збільшувалися майже залежно від дози.
Ліквідація
Популяційний фармакокінетичний аналіз на вибірці з більш ніж 1300 пацієнтів з РА показав тенденцію до очевидного збільшення кліренсу адалімумабу зі збільшенням маси тіла. Після корекції маси тіла гендерні та вікові відмінності мають мінімальний вплив на кліренс адалімумабу. вільний адалімумаб (незв’язаний з антиадалімумабними антитілами - ААА) був нижчим у пацієнтів з вимірюваними титрами ААА.
Печінкова або ниркова недостатність
Humira не вивчався у пацієнтів з печінковою або нирковою недостатністю.
05.3 Дані доклінічної безпеки
Неклінічні дані не виявляють особливої небезпеки для людини на підставі досліджень токсичності одноразової дози, токсичності при повторній дозі та генотоксичності.
Дослідження токсичності ембріонально-фетального розвитку / перинатального розвитку було проведено на мавпах-циномологах у дозах 0, 30 та 100 мг / кг (9-17 мавп / група); це дослідження не виявило пошкодження плоду, спричиненого адалімумабом. Випробування канцерогенності та стандартні оцінки фертильності та постнатальної токсичності не проводилися через відсутність відповідних моделей антитіл з обмеженою перехресною реактивністю до ФНП у гризунів та вироблення нейтралізуючих антитіл у гризунів.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Маніт
Лимонна кислота моногідрат
Цитрат натрію
Одноосновний натрію фосфат дигідрат
Динатрію фосфату дигідрат
Хлористий натрій
Полісорбат 80
Їдкий натр
Вода для ін'єкцій.
06.2 Несумісність
За відсутності досліджень сумісності цей лікарський засіб не слід змішувати з іншими лікарськими засобами.
06.3 Строк дії
24 місяці
06.4 Особливі умови зберігання
Зберігати в холодильнику (2 ° C - 8 ° C). Не заморожувати. Зберігайте флакон у картонній упаковці, щоб захистити ліки від світла.
06.5 Характер негайної упаковки та вміст упаковки
Розчин для ін’єкцій Humira 40 мг міститься у флаконі з одноразовою дозою (скло типу I), закритий гумовими пробками, покритий алюмінієвим шаром та відкидною кришкою.
1 упаковка з 2 коробок, кожна з яких містить:
1 флакон (0,8 мл стерильного розчину), 1 порожній стерильний шприц, 1 голка, 1 адаптер для флакона та 2 тампони зі спиртом.
06.6 Інструкції з використання та поводження
Розчин для ін’єкцій Humira 40 мг не містить консервантів. Невикористані ліки та відходи, отримані з цього препарату, слід утилізувати відповідно до місцевих правил.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
Maidenhead
SL6 4XE
Великобританія
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
EU/1/03/256/001 40 мг розчин для ін’єкцій 1 флакон 0,8 мл + 1 шприц + 2 тампони для підшкірного застосування 035946019/E
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
Дата першого дозволу: 8 вересня 2003 року
Дата останнього оновлення: 8 вересня 2008 року
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
09/2014