Діючі речовини: Прасугрел
Ефіент таблетки, вкриті оболонкою, 10 мг
Ефіент таблетки, вкриті оболонкою, 5 мг
Чому використовується Efient? Для чого це?
Ефіент, що містить діючу речовину прасугрел, належить до групи ліків, які називаються антитромбоцитарними засобами. Тромбоцити - це дуже маленькі клітини, які циркулюють у крові. Коли кровоносна судина пошкоджена, наприклад, якщо її розрізати, тромбоцити злипаються разом, сприяючи утворенню тромбу (тромбу). Тому тромбоцити необхідні для зупинки кровотечі. Якщо згустки утворюються всередині затверділої кровоносної судини, наприклад, артерії, вони можуть бути дуже небезпечними, оскільки можуть блокувати проходження крові, спричиняючи серцевий напад (інфаркт міокарда), інсульт або смерть Згустки в артеріях, які несуть кров до серця, також можуть зменшити приплив крові до серця, викликаючи нестабільну стенокардію (сильний біль у грудях).
Ефіент пригнічує агрегацію тромбоцитів і тому зменшує ймовірність утворення тромбів.
Ефіент вам призначили, тому що ви раніше перенесли серцевий напад або нестабільну стенокардію і проходили процедуру відкриття заблокованих серцевих артерій. Можливо, вам також був встановлений один або кілька стентів у заблокованій або звуженій артерії для відновлення кровотоку. Ефіент зменшує ймовірність того, що ви перенесете інший інфаркт або інсульт або померте від одного з цих атеротромботичних подій. Ваш лікар також призначить ацетилсаліцилову кислоту ( аспірин), інший антитромбоцитарний препарат.
Протипоказання Коли Ефіент не слід застосовувати
Не приймайте Ефіент
- Якщо у вас алергія (гіперчутливість) на прасугрел або будь -який інший інгредієнт препарату Ефіент. Алергічну реакцію можна розпізнати, оскільки вона викликає висип, свербіж, набряк обличчя, набряк губ або свистячі хрипи.
- Якщо у вас є захворювання, яке спричиняє кровотечу, наприклад кровотеча з шлунка або кишечника.
- Якщо у вас раніше був інсульт або транзиторна ішемічна атака (ТІА).
- Якщо у вас важке захворювання печінки.
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Ефіент
Якщо трапляється якась із згаданих нижче ситуацій, повідомте свого лікаря перед тим, як приймати Ефіент:
- Якщо у вас підвищений ризик кровотечі, наприклад:
- 75 років і старше. Ваш лікар призначить добову дозу 5 мг, оскільки існує підвищений ризик кровотечі у пацієнтів старше 75 років.
- недавня важка травма
- недавня операція (включаючи деякі стоматологічні процедури)
- нещодавні або періодичні кровотечі в шлунку або кишечнику (наприклад, виразка шлунка або поліп товстої кишки)
- маса тіла менше 60 кг. Ваш лікар призначить щоденну дозу 5 мг Ефієнта, якщо Ваша вага менше 60 кг - помірне захворювання печінки або нирок
- якщо ви приймаєте певні ліки (див. "Прийом Ефіенту з іншими ліками")
- якщо вам належить запланована операція (включаючи деякі стоматологічні процедури) протягом наступних семи днів. Ваш лікар може порадити вам тимчасово припинити прийом Ефієнта через підвищений ризик кровотечі
- Якщо у вас коли -небудь були алергічні реакції (гіперчутливість) на клопідогрель або будь -який інший антитромбоцитарний препарат, повідомте свого лікаря перед початком лікування Ефіентом. Якщо потім ви приймаєте Ефіент і відчуваєте алергічні реакції, які можуть бути розпізнані як «висип, свербіж, набряк обличчя, набряклі губи або задишка, вам слід негайно повідомити про це лікаря.
Під час прийому Ефієнта:
Негайно повідомте свого лікаря, якщо у вас виникло захворювання, яке називається тромботична тромбоцитопенічна пурпура (ПТТ), яке включає лихоманку та синці під шкірою, які можуть виглядати у вигляді крихітних червоних крапок, з незрозумілою глибокою втомою, плутаниною, зміною кольору. Жовтуватою шкірою чи очима (жовтяниця) (див. розділ 4 "Можливі побічні ефекти").
Діти та підлітки
Ефіент не призначений для застосування у дітей та підлітків віком до 18 років.
Взаємодії Які препарати або продукти харчування можуть змінити дію Ефієнта
Повідомте свого лікаря, якщо ви приймаєте, нещодавно приймали або могли б приймати будь -які інші ліки, включаючи ліки, що відпускаються без рецепта, біологічно активні добавки та рослинні засоби. Особливо важливо повідомити лікаря, якщо ви отримуєте клопідогрель (антиагрегантний препарат), варфарин (антикоагулянт) або «нестероїдні протизапальні препарати» для полегшення болю та зниження температури (наприклад, ібупрофену, напроксен, еторикоксиб). При одночасному застосуванні з Ефіентом ці ліки можуть збільшити ризик кровотечі.
Приймайте інші ліки під час прийому препарату Ефіент, тільки якщо ваш лікар скаже, що ви можете.
Попередження Важливо знати, що:
Вагітність та годування груддю
Скажіть своєму лікарю, якщо ви вагітні або плануєте завагітніти під час прийому Ефіенту. Використовувати Efient слід лише після обговорення з лікарем потенційних переваг та потенційних ризиків для майбутньої дитини.
Якщо ви годуєте грудьми, зверніться за порадою до лікаря або фармацевта, перш ніж приймати будь -які ліки
Водіння автомобіля та роботу з машинами
Навряд чи Efient вплине на здатність керувати автомобілем або працювати з механізмами.
Ефіент містить лактозу.
Якщо ваш лікар сказав вам, що у вас «непереносимість деяких цукрів, проконсультуйтеся з лікарем, перш ніж приймати цей препарат.
Доза, спосіб та час введення Як використовувати Ефіент: Дозування
Завжди приймайте Ефіент точно так, як вам сказав ваш лікар. Якщо є сумніви, зверніться до лікаря або фармацевта.
Звичайна доза Efient становить 10 мг на добу. Лікування розпочнеться з одноразової дози 60 мг. Якщо маса вашого тіла менше 60 кг або вам більше 75 років, доза становить 5 мг Ефієнта на день.
Ваш лікар також скаже вам приймати ацетилсаліцилову кислоту - він підкаже точну дозу (зазвичай від 75 мг до 325 мг на день).
Ви можете приймати Efient з їжею або без неї. Приймайте Ефіент щодня приблизно в один і той же час. Не розтрошуйте та не розламуйте таблетку.
Важливо повідомити свого лікаря, фармацевта та стоматолога, що ви приймаєте Ефіент.
Передозування Що робити, якщо ви прийняли занадто багато Ефіенту
Якщо ви прийняли більше Ефієнта, ніж слід
Негайно зверніться до лікаря або до найближчої лікарні через ризик надмірної кровотечі.
Якщо ви забули прийняти Ефіент
Якщо ви забули прийняти дозу, випийте одну таблетку, як тільки ви її помітите. Якщо ви забули прийняти дозу протягом усього дня, просто прийміть свою звичайну дозу Ефієнта наступного дня. Не приймайте дві дози в один день. Для упаковок із 14, 28, 56, 84 та 98 таблеток ви можете перевірити день, коли ви прийняли останню таблетку Efient, перевіривши календар, надрукований на блістері.
Якщо Ви припините прийом Ефієнта
Не припиняйте прийом препарату Ефіент, не поговоривши з лікарем. Якщо ви припините прийом препарату Ефіент занадто рано, ризик інфаркту міокарда може бути вищим.
Якщо у Вас виникнуть додаткові запитання щодо застосування цього препарату, зверніться до лікаря або фармацевта.
Побічні ефекти Які побічні ефекти Ефієнта
Як і всі ліки, Ефіент може викликати побічні ефекти, хоча вони виникають не у всіх.
Вам слід негайно звернутися до лікаря, якщо ви помітили будь -який з наступних побічних ефектів:
- Раптова сонливість або слабкість у руці, нозі чи обличчі, особливо якщо вони обмежені однією стороною тіла
- Раптове замішання, труднощі говорити або розуміти, що говорять інші
- Раптові труднощі при ходьбі або втрата рівноваги або координації
- Раптовий запаморочення або раптовий сильний головний біль без відомих причин.
Все вищесказане може бути ознакою інсульту. Інсульт - це рідкісний побічний ефект препарату Ефіент у пацієнтів, у яких ніколи не було інсульту або транзиторної ішемічної атаки (ТІА).
Також негайно зверніться до лікаря, якщо ви помітили будь -який з наступних побічних ефектів:
- лихоманка та синці під шкірою, які можуть виглядати у вигляді крихітних червоних крапок, з незрозумілою глибокою втомою, сплутаністю свідомості, пожовтінням шкіри або очей (жовтяниця) (див. розділ 2 "ПЕРЕД тим, як ви почнете діяти")
- "шкірний висип, свербіж або набряк обличчя, набряк губ / язика або хрипи. Все це може бути ознаками серйозної алергічної реакції (див. розділ 2" Що потрібно знати, перш ніж приймати Ефіент ")
Вам слід негайно звернутися до лікаря, якщо ви помітили будь -який з наступних побічних ефектів:
- Кров у сечі
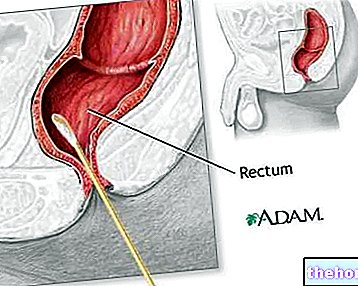
- Кровотеча з прямої кишки, кров у калі або чорний стілець
- Неконтрольована кровотеча, наприклад, від порізу
Все вищеперелічене може бути ознаками кровотечі, найпоширенішим побічним ефектом застосування Ефіенту. Хоча це рідкість, сильна кровотеча може бути небезпечною для життя.
Поширені побічні ефекти (можуть виникнути до 1 з 10 осіб)
- Кровотеча в шлунку або кишечнику
- Кровотеча з місця уколу голкою
- Кровотеча з носа
- Шкірний висип
- Невеликі червоні синці на шкірі (синці)
- Кров у сечі
- Гематома (кровотеча під шкірою в місці ін’єкції або в м’яз, що викликає набряк)
- Низький гемоглобін або низький рівень еритроцитів (анемія)
- Синці
Нечасті побічні ефекти (можуть виникнути до 1 з 100 осіб)
- Алергічна реакція (висип, свербіж, набряк губ / язика або хрипи)
- Спонтанна кровотеча з очей, прямої кишки, ясен або живота навколо внутрішніх органів
- Кровотеча після операції
- Відкашлювання крові
- Кров у калі
Рідкісні побічні ефекти (можуть виникнути до 1 з 1000 осіб)
- Низька кількість тромбоцитів у крові
- Підшкірна гематома (кровотеча під шкірою, що викликає набряк)
Повідомлення про побічні ефекти
Якщо будь -який з побічних ефектів стає серйозним або якщо Ви помітили будь -які побічні ефекти, не зазначені у цій інструкції, повідомте про це свого лікаря або фармацевта. Ви також можете повідомляти про побічні ефекти безпосередньо за допомогою національної системи звітності, наведеної у Додатку V. Повідомляючи про побічні ефекти, ви можете допомогти надати більше інформації про безпеку застосування цього лікарського засобу.
Термін придатності та утримання
Зберігайте Efient подалі від очей та недоступного для дітей місця.
Не використовуйте Ефіент після закінчення терміну придатності, зазначеного на блістері та картонній упаковці після закінчення терміну придатності. Термін придатності відноситься до останнього дня місяця.
Зберігати в оригінальній упаковці для захисту від повітря та вологи.
Ліки не слід утилізувати через стічні води або побутові відходи. Запитайте у фармацевта, як викидати ліки, які ви більше не використовуєте. Це допоможе захистити навколишнє середовище.
Що містить Ефіент
- Діюча речовина - прасугрел.
Ефіент 10 мг: кожна таблетка містить 10 мг прасугрелу (у вигляді гідрохлориду).
Ефіент 5 мг: кожна таблетка містить 5 мг прасугрелу (у вигляді гідрохлориду).
- Інші інгредієнти: целюлоза мікрокристалічна, маніт (Е421), кроскармелоза натрію, гіпромелоза (Е464), стеарат магнію, моногідрат лактози, діоксид титану (Е171), триацетин (Е1518), червоний оксид заліза (лише для таблеток по 10 мг) (Е172) , жовтий оксид заліза (Е172) і тальк.
Як виглядає Ефіент та вміст упаковки
Ефіент 10 мг: Таблетки бежевого кольору і мають форму подвійної стрілки, з тисненням «10 MG» з одного боку та «4759» з іншого боку.
Ефіент 5 мг: таблетки мають жовту форму та форму подвійної стрілки з тисненням «5 MG» з одного боку та «4760» з іншого боку.
Efient випускається в упаковках по 14, 28, 30, 56, 84, 90 та 98 таблеток.
Не всі розміри упаковок можна продавати.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
ЕФЕКТИВНІ ТАБЛЕТКИ по 10 мг, покриті плівкою
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Кожна таблетка містить 10 мг прасугрелу (у вигляді гідрохлориду).
Допоміжні речовини з відомими ефектами: кожна таблетка містить 2,1 мг лактози.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Таблетка, вкрита плівковою оболонкою (таблетка).
Таблетки бежевого кольору, у формі подвійної стрілки, з тисненням «10 MG» з одного боку та «4759» з іншого.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Ефіент у комбінації з ацетилсаліциловою кислотою (АСК) призначений для профілактики атеротромботичних явищ у дорослих пацієнтів з гострим коронарним синдромом (ГКС) (тобто нестабільна стенокардія, інфаркт міокарда без піднесення сегмента ST [UA / NSTEMI] або сегмента ST підвищений інфаркт міокарда [STEMI]), який проходить первинне або відстрочене черезшкірне коронарне втручання (ЧКВ).
Для отримання додаткової інформації див. Розділ 5.1.
04.2 Дозування та спосіб введення
Дозування
Дорослі
Ефіент слід починати з одноразової навантажувальної дози 60 мг, а потім продовжувати з 10 мг один раз на день. Пацієнти, які приймають Ефіент, також повинні приймати ацетилсаліцилову кислоту (АСК) 75 мг - 325 мг на день.
У пацієнтів з гострим коронарним синдромом (ГКС), які проходять черезшкірне коронарне втручання, раннє припинення застосування будь -яких антитромбоцитарних препаратів, включаючи Ефіент, може призвести до збільшення ризику тромбозу, інфаркту міокарда або смерті через основний медичний стан пацієнта. Лікування до 12 років рекомендована тривалість місяців, якщо клінічно не показано припинення застосування Ефієнта (див. розділи 4.4 та 5.1).
Вікові пацієнти ≥ 75 років
Застосування Ефієнта пацієнтам віком ≥ 75 років, як правило, не рекомендується. ≥ 75 років, то після навантажувальної дози 60 мг слід призначити знижену підтримуючу дозу 5 мг.Пацієнти у віці ≥ 75 років мають підвищену чутливість до кровотеч та підвищену дію метаболіту, активного інгредієнта прасугрелу (див. Розділи 4.4, 4.8, 5.1 та 5.2).
Пацієнти з масою тіла
Ефіент слід вводити у вигляді одноразової навантажувальної дози 60 мг з наступною дозою 5 мг один раз на день. Підтримуюча доза 10 мг не рекомендується. Це пов'язано зі збільшенням впливу активного метаболіту прасугрелу та збільшенням ризику кровотеч у пацієнтів з вагою.
Порушення функції нирок
Для пацієнтів з нирковою недостатністю, включаючи пацієнтів із термінальною стадією ниркової недостатності, коригувати дозу не потрібно (див. Розділ 5.2). Терапевтичний досвід у пацієнтів з нирковою недостатністю обмежений (див. Розділ 4.4).
Порушення функції печінки
Коригування дози для пацієнтів з печінковою недостатністю легкого та помірного ступеня (класи А та В за Чайлдом-П’ю) не потрібно (див. Розділ 5.2). Терапевтичний досвід у пацієнтів з печінковою недостатністю легкого та помірного ступеня обмежений (див. Розділ 4.4). Ефіент протипоказаний пацієнтам з тяжкою печінковою недостатністю (клас С за Чайлдом П’ю).
Педіатричне населення
Безпека та ефективність застосування Ефіенту у дітей віком до 18 років ще не встановлені.
Спосіб введення
Для перорального застосування. Ефіент можна вводити незалежно від їжі. Не роздавлюйте і не розламуйте планшет.
04.3 Протипоказання
Підвищена чутливість до активної речовини або до будь -якої з допоміжних речовин, перерахованих у розділі 6.1.
Триває патологічна кровотеча.
В анамнезі інсульт або транзиторна ішемічна атака (ТІА).
Важка печінкова дисфункція (клас С за Чайлдом-П’ю).
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
Ризик кровотечі
У клінічному дослідженні фази 3 ключові критерії виключення включали підвищений ризик кровотечі; анемія; тромбоцитопенія; історія результатів, що свідчать про внутрішньочерепну патологію.
Пацієнти з гострим коронарним синдромом, які проходять черезшкірне коронарне втручання, які отримували лікування Ефієнтом та АСК, показали підвищений ризик великих та незначних кровотеч відповідно до системи класифікації TIMI.
Тому застосування Ефіенту пацієнтам із підвищеним ризиком кровотечі слід розглядати лише тоді, коли вважається, що користь від профілактики ішемічних подій перевищує ризик серйозної кровотечі. Ця застереження стосується особливо пацієнтів:
• у віці ≥75 років (див. Нижче).
• зі схильністю до кровотеч (наприклад, через недавню травму, недавню операцію, недавню або періодичну кровотечу з шлунково -кишкового тракту або постійну виразкову хворобу)
• з масою тіла
• при одночасному лікуванні лікарськими засобами, які можуть збільшити ризик кровотеч, включаючи пероральні антикоагулянти, клопідогрель, нестероїдні протизапальні препарати (НПЗЗ) та фібринолітики.
Пацієнтам з тривалою кровотечею, яким потрібно змінити фармакологічні ефекти препарату Ефіент, може бути доцільним переливання тромбоцитів.
Введення препарату Ефіент пацієнтам у віці ≥ 75 років, як правило, не рекомендується, і його слід проводити з обережністю лише після того, як "ретельна індивідуальна оцінка користі / ризику, призначена лікарем, покаже, що користь від ішемії у профілактиці більша, ніж ризик серйозної кровотечі" У клінічному дослідженні фази 3 ці пацієнти мали підвищений ризик кровотеч, включаючи смертельну, порівняно з пацієнтами у віці
Терапевтичний досвід застосування прасугрелу обмежений у пацієнтів з порушеннями функції нирок (включаючи пацієнтів із термінальною стадією ниркової недостатності (ESRD)) та у пацієнтів з помірною печінковою дисфункцією. Ці пацієнти можуть мати підвищений ризик кровотечі.
Тому прасугрел слід з обережністю застосовувати таким пацієнтам.
Пацієнтів слід попередити, що під час прийому прасугрелу (у комбінації з АСК) припинення кровотечі може тривати довше, ніж зазвичай, і вони повинні повідомити свого лікаря про будь -які незвичайні кровотечі (за місцем чи тривалістю).
Хірургічне втручання
Перед будь -яким хірургічним втручанням і перед тим, як приймати нові ліки, пацієнти повинні повідомити своїм лікарям та стоматологам, що вони приймають прасугрел. Якщо пацієнту слід пройти планову операцію, а антитромбоцитарний ефект не вважається належним, застосування Ефієнта слід припинити принаймні за 7 днів до операції. У пацієнтів може спостерігатися збільшення (у 3 рази) частоти та тяжкості кровотечі. 7 днів після припинення прийому прасугрелу (див. Розділ 4.8). Переваги та ризики застосування прасугрелу слід ретельно обміркувати у тих пацієнтів, у яких анатомія коронарного суглоба не визначена та можлива термінова операція АКШ.
Гіперчутливість, включаючи ангіоневротичний набряк
Повідомлялося про реакції гіперчутливості, включаючи ангіоневротичний набряк, у пацієнтів, які отримували прасугрел, включаючи пацієнтів з анамнезом реакцій гіперчутливості до клопідогрелю. Рекомендується моніторинг ознак гіперчутливості у пацієнтів з відомою в анамнезі алергією на тієнопіридини (див. Розділ 4.8).
Тромботична тромбоцитопенічна пурпура (РТТ)
Повідомлялося про застосування РТТ при застосуванні прасугрелу. РТТ - серйозне захворювання, яке потребує негайного лікування.
Лактоза
Пацієнтам з рідкісними спадковими проблемами непереносимості галактози, дефіцитом лактази Лаппа або мальабсорбцією глюкози-галактози не слід приймати Ефіент..
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Варфарин: Одночасне застосування ефієнту та похідних кумарину, крім варфарину, не вивчалося. Через можливість підвищеного ризику кровотеч слід бути обережним при одночасному застосуванні варфарину (або інших похідних кумарину) та прасугрелу (див. Розділ 4.4).
Нестероїдні протизапальні препарати (НПЗЗ):
Одночасне застосування хронічних НПЗЗ не вивчалося. Через можливість підвищеного ризику кровотеч одночасне застосування хронічних НПЗЗ (включаючи інгібітори ЦОГ-2) та Ефієнту слід проводити з обережністю (див. Розділ 4.4).
Ефіент можна вводити в комбінації з лікарськими засобами, що метаболізуються ферментами цитохрому Р450 (включаючи статини), або лікарськими засобами, які є індукторами або інгібіторами ферментів цитохрому Р450. Ефіент також можна призначати у комбінації з АСК, гепарином, дигоксином та препаратами, що підвищують рН шлунка, включаючи інгібітори протонної помпи та блокатори Н2.
Хоча це не є предметом специфічних досліджень взаємодії, Efient вводили у клінічному дослідженні фази 3 у поєднанні з низькомолекулярним гепарином, бівалірудином та інгібіторами GP IIb / IIIa (інформація про тип інгібітора GP IIb / IIIa відсутня використовується) без ознак клінічно значущих побічних взаємодій.
Вплив інших лікарських засобів на Ефіент:
Ацетилсаліцилова кислота: Ефіент слід вводити в поєднанні з АСК. Хоча фармакодинамічна взаємодія з АСК з подальшим збільшенням ризику кровотечі можлива, докази ефективності та безпеки прасугрелу надходять від пацієнтів, які отримують комбінацію з АСК.
Гепарин: Одноразова болюсна доза внутрішньовенного введення нефракціонованого гепарину (100 ОД / кг) не суттєво змінила пригнічення агрегації тромбоцитів, опосередкованої прасугрелом. Так само прасугрел не суттєво змінив вплив гепарину на параметри згортання крові.
Тому обидва ліки можна приймати в комплексі. Можливий підвищений ризик кровотечі при одночасному застосуванні Ефієнта з гепарином.
Статини: Аторвастатин (80 мг на добу) не змінював фармакодинамічну активність прасугрелу або його інгібування агрегації тромбоцитів. Тому не очікується, що субстратні статини CYP3A впливають на фармакокінетику прасугрелу або його пригнічення агрегації прасугрелю..
Ліки, що підвищують рН шлунка: Одночасне застосування ранітидину (блокатора Н2) або лансопразолу (інгібітора протонної помпи) щодня не змінювало AUC та Tmax активного метаболіту прасугрелу, але знижувало Cmax на 14% та 29% відповідно.У клінічному дослідженні фази 3 Ефіент вводили незалежно від одночасного введення інгібітора протонної помпи або блокатора Н2. Введення навантажувальної дози 60 мг прасугрелу без одночасного застосування інгібіторів протонної помпи може призвести до більш швидкого початку дії препарату.
Інгібітори CYP3AКетоконазол (400 мг на добу), потужний та селективний інгібітор CYP3A4 та CYP3A5, не змінив інгібування агрегації тромбоцитів, опосередкованої прасугрелом, або AUC та T активного метаболіту прасугрелу, але знизив Cmax на 34% до 46% Тому інгібітори CYP3A, такі як азольні протигрибкові засоби, інгібітори протеази ВІЛ, кларитроміцин, телітроміцин, верапаміл, дилтіазем, індинавір, ципрофлоксацин та сік грейпфрута, як очікується, не матимуть значного впливу на фармакокінетику метаболіту.
Індуктори цитохрому Р450: Рифампіцин (600 мг на добу), потужний індуктор CYP3A та CYP2B6, а також індуктор CYP2C9, CYP2C19 та CYP2C8, не суттєво змінив фармакокінетику прасугрелу. Тому не очікується, що відомі індуктори CYP3A, такі як рифампіцин, карбамазепін та інші індуктори цитохромів Р450, матимуть значний вплив на фармакокінетику активного метаболіту.
Вплив Efient на інші лікарські засоби:
Дигоксин: Прасугрел не має клінічно значущого впливу на фармакокінетику дигоксину.
Лікарські засоби, що метаболізуються за допомогою CYP2C9: Прасугрел не інгібує CYP2C9, оскільки не впливає на фармакокінетику варфарину-S. Через можливий підвищений ризик кровотечі слід бути обережним при одночасному призначенні варфарину та ефієнта (див. Розділ 4.4).
Лікарські засоби, що метаболізуються CYP2B6: Прасугрел є слабким інгібітором CYP2B6. У здорових добровольців прасугрел зменшив вплив гідроксибупропіону, опосередкованого CYP2B6 метаболіту бупропіону, на 23%. Ймовірно, цей ефект буде викликати клінічну стурбованість лише тоді, коли прасугрел вводять у комбінації з лікарськими засобами, для яких єдиним метаболічним шляхом є CYP2B6 і які мають обмежене терапевтичне вікно (наприклад, циклофосфамід, ефавіренц).
04.6 Вагітність та лактація
Клінічні дослідження не проводилися у вагітних або жінок, що годують груддю.
Вагітність
Дослідження на тваринах не вказують на прямі шкідливі наслідки щодо вагітності, ембріонального / внутрішньоутробного розвитку, пологів або постнатального розвитку (див. Розділ 5.3). Оскільки дослідження репродуктивної активності на тваринах не завжди передбачають вплив на людину, Efient слід застосовувати під час вагітності, лише якщо потенційна користь виправдовує потенційний ризик для плоду.
Час годування
Невідомо, чи виділяється прасугрел у жіноче молоко. Дослідження на тваринах показали, що прасугрел виводиться з грудного молока. Використання прасугрелу під час годування груддю не рекомендується.
Родючість
Прасугрел не впливав на фертильність самців і самок у щурів, які зазнали пероральних доз, що до 240 разів перевищували рекомендовану добову дозу для людини (оцінювались у мг / м2).
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Не очікується, що прасугрел вплине або незначно вплине на здатність керувати автомобілем або працювати з механізмами.
04.8 Побічні ефекти
Короткий опис профілю безпеки
Безпеку у пацієнтів з гострим коронарним синдромом, які проходили черезшкірне коронарне втручання, оцінювали у клінічному дослідженні клопідогрелю (TRITON), в якому 6741 пацієнт отримував прасугрел (з навантажувальною дозою 60 мг та підтримуючою дозою 10 мг на день) медіана 14,5 місяців (5 802 пацієнта лікувалися більше 6 місяців, 4136 пацієнтів лікувалися більше 1 року). Частота припинення прийому досліджуваного препарату через побічні ефекти становила 7,2% для прасугрелу та 6,3% для клопідогрелю. З них кровотеча була найчастішою побічною реакцією, що призвела до припинення застосування обох препаратів досліджуваного препарату (2,5% для прасугрелу та 1,4% для клопідогрелю).
Кровотеча
Кровотеча, не пов'язана з аортокоронарним шунтуванням (АКШ)
У дослідженні TRITON частота пацієнтів, у яких був епізод кровотечі, не пов’язаної з аортокоронарним шунтуванням (АКШ), наведена в таблиці 1. Частота великих кровотеч (за визначеннями TIMI), не пов’язаних з аортокоронарним шунтуванням (АКШ), включаючи осіб, яким загрожує смерть та летальний результат, а також незначна кровотеча (згідно з визначеннями TIMI), було статистично достовірно вищим у пацієнтів, які отримували прасугрел, порівняно з суб'єктами, які отримували клопідогрель, як у UA / NSTEMI, так і у всій популяції ГКС . Значних відмінностей у популяції STEMI не спостерігалося. Найбільш поширеним місцем спонтанної кровотечі був шлунково -кишковий тракт (1,7% з прасугрелом і 1,3% з клопідогрелем); найбільш поширеним місцем індукованої кровотечі було місце артеріального доступу (1,3% з прасугрелом і 1,2% з клопідогрелем).
Таблиця 1: Частота кровотеч, не пов'язаних з операцією шунтування коронарних артерій (АКШ) a (% пацієнтів)
a Події, визначені критеріями Тромболізису досліджуваної групи при інфаркті міокарда (ТІМІ), що проходить оцінку централізована.
b Інші стандартні методи лікування призначалися відповідно.
c Будь -яка внутрішньочерепна кровотеча або будь -яка клінічно виражена кровотеча, пов'язана зі зменшенням гемоглобіну ≥5 г / дл.
d Кровотеча з ризиком смерті є підгрупою великих кровотеч (згідно з визначеннями TIMI) e включає перелічені нижче типи. Пацієнтів можна підрахувати в декількох рядах.
і ICH = внутрішньочерепний крововилив.
f Клінічно очевидна кровотеча, пов'язана зі зниженням гемоглобіну ≥3 г / дл, але
Вікові пацієнти ≥ 75 років
Частота великих або незначних кровотеч (TIMI), не пов'язаних з аортокоронарним шунтуванням (АКШ):
* Дослідження TRITON у пацієнтів з ГКС, які проходять ЧКВ
** Дослідження TRILOGY-ACS у пацієнтів, які не проходять ЧКВ (див. Розділ 5.1):
до прасугрел 10 мг; прасугрел 5 мг, якщо
Пацієнти з масою тіла
Частота великих або незначних кровотеч (TIMI), не пов'язаних з аортокоронарним шунтуванням (АКШ):
* Дослідження TRITON у пацієнтів з ГКС, які проходять ЧКВ
** Дослідження TRILOGY-ACS у пацієнтів, які не проходять ЧКВ (див. Розділ 5.1):
до прасугрел 10 мг; прасугрел 5 мг у віці ≥ 75 років
Пацієнти вагою ≥60 кг та віком
У пацієнтів з масою тіла ≥60 кг та вік
Кровотеча, пов'язана з аортокоронарним шунтування (АКШ)
У клінічному дослідженні фази 3 437 пацієнтам було зроблено шунтування коронарної артерії (АКШ). З цих пацієнтів частота великих або незначних кровотеч (TIMI), пов'язаних з аортокоронарним шунтуванням (АКШ), становила 14,1% для групи прасугрелу та 4,5% для групи клопідогрелю. Найвищий ризик епізодів кровотеч у пацієнтів, які отримували прасугрел, зберігався протягом 7 днів після останньої дози досліджуваного препарату. Для пацієнтів, які отримували тієнопіридин протягом 3 днів до аортокоронарного шунтування (АКШ), частота великих або незначних кровотеч (ТІМІ) становила 26,7% (12 з 45 пацієнтів) у групі прасугрелю порівняно з 5,0% (3 з 60 пацієнтів) у групі клопідогрелю. Для пацієнтів, які отримали останню дозу тієнопіридину протягом 4-7 днів до аортокоронарного шунтування (АКШ), частота зменшилася до 11,3% (9 із 80 пацієнтів) у групі прасугрелу та 3,4 % (3 з 89 пацієнтів) у групі клопідогрелю. Понад 7 днів після припинення прийому препарату спостерігалися рівні кровотеч, пов’язані з аортокоронарним шунтуванням (АКШ), були подібними між 2 групами лікування (див. Розділ 4.4).
Зведена таблиця побічних реакцій
Таблиця 2 узагальнює геморагічні та негеморагічні побічні реакції у дослідженні TRITON або зі спонтанних повідомлень, класифікованих за частотою та органами системи. Їх частота визначається за допомогою таких умов: Дуже часто (≥ 1/10); поширені (≥ 1/100,
Таблиця 2: Геморагічні та негеморагічні побічні реакції
У пацієнтів з транзиторною ішемічною атакою (ТІА) або інсультом в анамнезі частота інсульту у дослідженні 3 фази була такою (див. Розділ 4.4):
* ICH = внутрішньочерепна кровотеча.
Повідомлення про підозрювані побічні реакції
Повідомлення про підозрювані побічні реакції, що виникають після реєстрації лікарського засобу, є важливими, оскільки вони дозволяють здійснювати постійний моніторинг співвідношення користь / ризик лікарського засобу. Медичних працівників просять повідомляти про будь -які підозрювані побічні реакції через національну систему звітності у "Додатку V" .
04.9 Передозування
Передозування препарату Ефіент може призвести до подовження часу кровотечі та подальших ускладнень кровотечі. Немає інформації про "скасування" фармакологічної активності прасугрелу; однак, коли потрібна швидка корекція тривалого часу кровотечі, можна розглянути можливість переливання тромбоцитів або інших продуктів крові.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: антиагреганти, крім гепарину.
Код ATC: B01AC22.
Фармакодинамічні ефекти
Прасугрел є інгібітором активації та агрегації тромбоцитів, який діє шляхом незворотного зв’язування його активного метаболіту з рецепторами тромбоцитів АДФ класу P2Y12. Функція тромбоцитів може призвести до зменшення частоти серцево -судинних подій, таких як смерть, інфаркт міокарда або інсульт.
Після навантажувальної дози 60 мг прасугрелу індуковане АДФ інгібування агрегації тромбоцитів відбувається через 15 хвилин з 5 мкМ АДФ та через 30 хвилин з 20 мкМ АДФ. Максимальне інгібування агрегації тромбоцитів. з 5 мкМ АДФ і 79% з 20 мкМ АДФ, в обох випадках у 89% здорових суб'єктів та пацієнтів зі стабільним атеросклерозом досягнення принаймні 50% інгібування агрегації тромбоцитів протягом 1 години. Інгібування агрегації тромбоцитів, досягнуте за допомогою Prasugrel, демонструє зменшення між- (9%) та внутрішньоодиничної (12%) мінливості як з 5 мкМ, так і з 20 мкМ АДФ. Середнє інгібування агрегації тромбоцитів у рівновазі становило 74% та 69%, з 5 мкМ АДФ та 20 мкМ АДФ відповідно, і було досягнуто після періоду від 3 до 5 днів введення одноразової дози. Підтримуюча доза 10 мг прасугрелу, якому передувала навантажувальна доза 60 мг. Понад 98% пацієнтів мали інгібування агрегації тромбоцитів ≥ 20% під час підтримуючої дози.
Після лікування агрегація тромбоцитів поступово поверталася до вихідного рівня протягом періоду від 7 до 9 днів після введення разової навантажувальної дози 60 мг прасугрелу та протягом 5 днів після припинення підтримуючої дози балансу.
Дані про перехід з клопідогрелю на прасугрелПісля введення клопідогрелю 75 мг один раз на день протягом 10 днів 40 здорових суб’єктів перейшли на прасугрел у дозі 10 мг один раз на день з навантажувальною дозою 60 мг або без неї. Подібне або вище інгібування агрегації тромбоцитів спостерігалося при застосуванні прасугрелу.Після введення навантажувальної дози 900 мг клопідогрелю (у поєднанні з АСК) 56 суб’єктів із ГКС протягом 14 днів отримували лікування прасугрелом у дозі 10 мг 1 раз на добу або клопідогрелем у дозі 150 мг 1 раз на день та перейшли на лікування 150 мг або прасугрел 10 мг протягом додаткових 14 днів відповідно ("перехід"). Найбільше пригнічення агрегації тромбоцитів спостерігалося у пацієнтів, які перейшли на 10 мг прасугрелу порівняно з тими, хто отримував 150 мг клопідогрелю.У дослідженні 276 пацієнтів з ГКС, які проходили ЧКВ, переходили з початкової навантажувальної дози 600 мг клопідогрелю або плацебо при госпіталізації, до проведення коронарографії, у навантажувальній дозі 60 мг прасугрелу, що вводилася під час перкутанного коронарного втручання, призводило до подібного збільшення кількості інгібування агрегації тромбоцитів протягом 72-годинного дослідження.
Ефективність та безпека при гострому коронарному синдромі
У дослідженні TRITON фази 3 Ефіент (прасугрел) порівнювали з клопідогрелем, обидва призначалися в комбінації з АСК та іншими стандартними методами лікування. TRITON-це міжнародне, рандомізоване, подвійне сліпе, паралельне групове, багатоцентрове дослідження, в якому взяли участь 13608 пацієнтів. Пацієнти мали ГКС з помірним та високим ризиком УА та NSTEMI або STEMI, і їх лікували за допомогою ЧКВ.
Пацієнти з UA / NSTEMI протягом 72 годин від початку симптомів або зі STEMI від 12 годин до 14 днів від початку симптомів були рандомізовані після знання анатомії коронарного кровообігу. можна було рандомізувати без відома коронарної картини.У всіх пацієнтів навантажувальну дозу можна було вводити в будь -який час від рандомізації до 1 години після виходу пацієнта з лабораторії, де проводилася катетеризація серця.
Пацієнтів, рандомізованих до прасугрелу (навантажувальна доза 60 мг, потім 10 мг один раз на день) або клопідогрелю (навантажувальна доза 300 мг, а потім 75 мг один раз на день), лікували середньо 14,5 місяців (максимум 15 місяців з мінімальним 6 місяців спостереження). Пацієнти також отримували АСК (від 75 мг до 325 мг один раз на день).
Критерієм виключення було використання будь -якого тієнопіридину за 5 днів до зарахування. Інші методи лікування, такі як гепарин та інгібітори GPIIb / IIIa, призначалися на розсуд лікаря. Приблизно 40% пацієнтів (у кожній групі лікування) отримували інгібітори GPIIb / IIIa для підтримки ЧКВ (інформація про тип ГП IIb відсутня / Інгібітор IIIa.) Приблизно 98% пацієнтів (у кожній групі лікування) безпосередньо отримували антитромбіни (гепарин, низькомолекулярний гепарин, бівалірудин або інші ліки) як підтримку для ЧКВ.
Основним показником результату дослідження був час до настання першої події серцево-судинної (серцево-судинної) смерті, нефатального інфаркту міокарда (ІМ) або нефатального інсульту. Складений цільовий аналіз у всій популяції АКС (включаючи групи UA / NSTEMI та STEMI) був обумовлений демонстрацією статистичної переваги прасугрелу над клопідогрелем у групі UA / NSTEMI (p
Загальна популяція АКС: Efient продемонстрував вищу ефективність у порівнянні з клопідогрелем у зниженні первинної складової кінцевої точки, а також попередньо визначених вторинних кінцевих точок, включаючи тромбоз стента (див. Таблицю 3). Перевага прасугрелу була очевидною протягом перших 3 днів і тривала до кінця дослідження. Покращена ефективність супроводжувалася збільшенням великої кровотечі (див. Розділи 4.4 та 4.8). Населення пацієнтів складало 92% європеоїдів, 26% жінок та 39% у віці ≥ 65 років. Переваги, пов’язані з прасугрелом, не залежали від застосування інших гострих та тривалих серцево-судинних методів лікування, включаючи низькомолекулярні гепарин / гепарин, бівалірудин, внутрішньовенні інгібітори GPIIb / IIIa, ліпідознижувальні препарати, бета-адреноблокатори та інгібітори ангіотензинперетворюючого ферменту. Ефективність прасугрелу не залежала від дози АСК (75-325 мг 1 раз на добу). Застосування пероральних антикоагулянтів, антитромбоцитарних лікарських засобів, крім тих, що досліджуються, та хронічних НПЗЗ не було дозволено у дослідженні TRITON. нефатального інсульту порівняно з клопідогрелем, незалежно від вихідних характеристик, таких як вік, стать, маса тіла, географічний регіон, застосування інгібіторів GPIIb / IIIa та тип стента. Випадки ГІМ (див. Таблицю 3) Діабетики показали значне зниження первинних та всіх вторинних складних кінцевих точок.
Користь прасугрелу, що спостерігалася у пацієнтів віком ≥ 75 років, була меншою, ніж у пацієнтів з цукровим діабетом, СТЕМІ, підвищеним ризиком тромбозу стента або рецидивів.
Пацієнти з ТІА в анамнезі або з ішемічною атакою в анамнезі за більш ніж 3 місяці до терапії прасугрелом не мали зниження первинної складової мети.
Таблиця 3: Пацієнти з клінічними результатами в первинному аналізі дослідження TRITON
У загальній популяції ГКС аналіз кожної з вторинних кінцевих точок продемонстрував значну користь (стор
Прасугрел асоціювався зі зменшенням тромбозу стента на 50% протягом 15-місячного періоду спостереження. Зменшення тромбозу стента за допомогою Efient спостерігалося як на ранніх термінах, так і після 30 днів як для металевих, так і для медичних стентів.
В аналізі пацієнтів, які пережили ішемічну подію, прасугрел асоціювався зі зниженням частоти наступних первинних кінцевих подій (7,8% з прасугрелом проти 11,9% з клопідогрелем).
Хоча кровотеча збільшилася при застосуванні прасугрелу, комплексний "цільовий аналіз", що включає смерть від усіх причин, нефатальний інфаркт міокарда, нефатальний інсульт та велику кровотечу, не пов'язану з АКШ, був сприятливим для Ефієнта порівняно з клопідогрелем (HR 0,87 ; 95% ДІ, від 0,79 до 0,95; р = 0,004). У дослідженні TRITON на кожну 1000 пацієнтів, які отримували Ефіент, було на 22 пацієнти менше з інфарктом міокарда та ще на 5 з великими кровотечами, не пов'язаними з АКШ, порівняно з пацієнтами, які отримували клопідогрель.
Результати фармакодинамічного / фармакогеномічного дослідження у 720 азіатських хворих на ГКС, які пройшли ЧКВ, продемонстрували, що прасугрел досягає більш високих рівнів інгібування тромбоцитів, ніж клопідогрель, і що навантаження 60 мг прасугрелу / підтримуюча доза 10 мг є відповідним режимом дозування для азіатських пацієнтів з масою тіла щонайменше 60 кг і мають вік менше 75 років (див. розділ 4.2).
У 30-місячному дослідженні (TRILOGY-ACS), проведеному у 9326 пацієнтів, які проходили медикаментозне лікування з ГКС UA / NSTEMI, без реваскуляризації (незареєстроване показання), прасугрел не суттєво зменшив частоту складеної цілі смерті від ІМ або інсульту порівняно Частота великих кровотеч (ТІМІ) (включаючи ризик смерті, летального результату та внутрішньочерепної кровотечі) була подібною у пацієнтів, які отримували прасугрел та клопідогрель. ≥ 75 років або вагою менше 60 кг (N = 3022) рандомізовано до прасугрелу 5 мг. Як і у пацієнтів у віці
05.2 Фармакокінетичні властивості
Прасугрел є проліком і швидко метаболізується в природних умовах до активного метаболіту та неактивних метаболітів. Експозиція активного метаболіту (AUC) має середню та низьку варіабельність між суб’єктами (27%) та між суб’єктами (19%). Фармакокінетика прасугрелу однакова у здорових добровольців, пацієнтів зі стабільним атеросклерозом та у пацієнтів, які проходять черезшкірне коронарне втручання.
Поглинання
Абсорбція та метаболізм прасугрелу проходять швидко, максимальні концентрації активного метаболіту в плазмі (Cmax) досягаються приблизно через 30 хвилин. Вплив активного метаболіту (AUC) пропорційно збільшується у порівнянні з терапевтичною дозою. активний метаболіт не змінювався за допомогою їжі з високим вмістом жиру та калорій, але Cmax знизився на 49%, а час досягнення Cmax (Tmax) збільшився з 0, 5 до 1,5 години. У дослідженні TRITON Efient вводили незалежно від їжі, тому Efient можна вводити незалежно від їжі; проте введення навантажувальної дози прасугрелу натще може призвести до більш швидкого початку дії (див. розділ 4.2).
Розповсюдження
Зв’язування активного метаболіту з альбуміном сироватки людини (4% буферний розчин) становило 98%.
Обмін речовин
Після перорального застосування прасугрел не виявляється у плазмі крові. Він швидко гідролізується в кишечнику до тіолактону, який потім перетворюється в активний метаболіт на одному етапі метаболізму за допомогою цитохрому Р450, головним чином CYP3A4 та CYP2B6, і меншою мірою за допомогою CYP2C9 та CYP2C19. Активний метаболіт згодом метаболізується до двох сполук . неактивний шляхом S-метилювання або кон'югації з цистеїном.
У здорових добровольців, пацієнтів зі стабільним атеросклерозом та пацієнтів з ГКС, які отримували Efient, не було виявлено відповідного впливу генетичних змін CYP3A5, CYP2B6, CYP2C9 або CYP2C19 на фармакокінетику прасугрелу або його пригнічення агрегації тромбоцитів.
Ліквідація
Приблизно 68% дози прасугрелу виводиться із сечею та 27% з калом у вигляді неактивних метаболітів. Активний метаболіт має період напіввиведення приблизно 7,4 години (від 2 до 15 годин).
Особливі популяції:
Літні громадяни: У дослідженні на здорових добровольцях віком від 20 до 80 років вік не мав значного впливу на фармакокінетику прасугрелу або на пригнічення агрегації тромбоцитів, яку він виробляє. У "великому клінічному дослідженні фази 3" вплив активного метаболіту (AUC) був на 19% вищим у пацієнтів дуже літнього віку (вік ≥ 75 років) порівняно з суб'єктами у віці
Прасугрел слід з обережністю застосовувати пацієнтам віком ≥ 75 років через потенційний ризик кровотеч у цій популяції (див. Розділи 4.2 та 4.4). У дослідженні на пацієнтах зі стабільним атеросклерозом середня експозиція (AUC) активного метаболіту у пацієнтів віком ≥ 75 років, які приймали прасугрел у дозі 5 мг, була приблизно наполовину нижчою, ніж у пацієнтів віком ≥ 75 років.
Печінкова недостатність: Не потрібно коригувати дозу для пацієнтів з печінковою недостатністю легкого та помірного ступеня (клас А або В за Чайлдом-П’ю). Фармакокінетика прасугрелу та його інгібування агрегації тромбоцитів були подібними у пацієнтів з печінковою недостатністю легкого та помірного ступеня порівняно зі здоровими. Фармакокінетику та фармакодинаміку прасугрелу у пацієнтів з тяжкою печінковою недостатністю не вивчали. Його не слід застосовувати пацієнтам з тяжка печінкова недостатність (див. розділ 4. 3).
Ниркова недостатність: Коригування дози для пацієнтів з нирковою недостатністю, включаючи пацієнтів із термінальною стадією ниркової недостатності (ESRD), не потрібне. Фармакокінетика прасугрелу та його інгібування агрегації тромбоцитів подібні у пацієнтів з помірною нирковою недостатністю (швидкість клубочкової фільтрації (ШКФ) 30-2) та у здорових добровольців. Інгібування агрегації тромбоцитів, опосередкованої прасугрелом, було подібним. Також у пацієнтів із ССРЗ, які потребували гемодіалізу порівняно зі здоровими суб'єктами, хоча Cmax та AUC активного метаболіту знизилися відповідно на 51% та 42% у пацієнтів із ШОЕ.
Вага тіла: Експозиція активного метаболіту (AUC) прасугрелу приблизно на 30-40% вища у здорових осіб та пацієнтів з масою тіла
Етнічна приналежність: У клінічних фармакологічних дослідженнях, після коригування маси тіла, AUC активного метаболіту була приблизно на 19% вищою у суб’єктів Китаю, Японії та Кореї порівняно з кавказькими, головним чином у зв’язку з вищою експозицією у азіатських суб’єктів з масою тіла
Стать: У здорових осіб та пацієнтів фармакокінетика прасугрелу у жінок та чоловіків однакова.
Педіатричне населення: Фармакокінетику та фармакодинаміку прасугрелу не оцінювали у педіатричній популяції (див. Розділ 4.2).
05.3 Дані доклінічної безпеки
Неклінічні дані не виявили особливої небезпеки для людини на основі звичайних досліджень фармакології безпеки, токсичності при повторних дозах, генотоксичності, канцерогенного потенціалу чи токсичності для репродукції. Ефекти в неклінічних дослідженнях спостерігалися. максимальний вплив на людину, що свідчить про низьку релевантність для клінічного застосування.
Токсикологічні дослідження ембріонально-плодового розвитку у щурів та кроликів не показали жодних ознак вад розвитку, спричинених прасугрелом. У дуже високій дозі (> 240 разів більше рекомендованої добової дози, що підтримується людиною у мг / м2), що спричинила вплив на масу тіла матері та / або споживання їжі, відбулося незначне зменшення маси тіла у потомства (порівняно з контролем) в пре- та постнатальних дослідженнях на щурах лікування матері не впливало на поведінковий або репродуктивний розвиток потомства у дозах, що до 240 разів перевищували рекомендовану добову дозу для людини (виражену в мг / м2).
У 2-річному дослідженні на щурах із експозицією прасугрелю в 75 разів більше рекомендованої терапії людини (на основі експозиції плазми людини активним метаболітом та метаболітами людини), основних з яких в крові не спостерігалося. У мишей, які протягом 2 років зазнавали високих доз (> 75 разів більше, ніж вплив на людину), спостерігалося «збільшення захворюваності на пухлини (гепатоцелюлярні аденоми), але це вважалося вторинним у порівнянні з індукцією ферментів, викликаних прасугрелом. L» Специфічна асоціація печінки для гризунів пухлини та індукція індукованих ліками ферментів добре задокументована в літературі. Збільшення пухлин печінки при введенні прасугрелу у мишей не вважається відповідним ризиком для людини.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Ядро планшета:
Мікрокристалічна целюлоза
Маніт (E421)
Кроскармелоза натрію
Гіпромелоза (E464)
Стеарат магнію
Покриття:
Моногідрат лактози
Гіпромелоза (E464)
Діоксид титану (E171)
Триацетин (E1518)
Червоний оксид заліза (E172)
Жовтий оксид заліза (E172)
Талк
6.2 Несумісність
Не застосовується.
06.2 Несумісність
2 роки.
06.3 Строк дії
2 роки.
06.4 Особливі умови зберігання
Цей лікарський засіб не вимагає особливих температур зберігання. Зберігати в оригінальній упаковці для захисту від повітря та вологи.
06.5 Характер негайної упаковки та вміст упаковки
Алюмінієві блістери у картонній упаковці по 14, 28, 30, 30 (x1), 56, 84, 90 (x1) та 98 таблеток.
Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження
Ніяких спеціальних вказівок.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
Eli Lilly Nederland BV, Grootslag 1-5, NL-3991 RA Houten, Нідерланди.
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
ЄС/1/08/503/008
039055088
ЄС/1/08/503/009
039055090
ЄС/1/08/503/010
039055102
ЄС/1/08/503/011
039055114
ЄС/1/08/503/012
039055126
ЄС/1/08/503/013
039055138
ЄС/1/08/503/014
039055140
ЄС/1/08/503/016
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
Дата першого дозволу: 25 лютого 2009 року
Остання дата поновлення:
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
11.0 ДЛЯ РАДІОЛЕКЦІЙ, ПОВНІ ДАНІ ПРО ВНУТРІШНЮ РАДІАЦІЮ
12.0 ДЛЯ РАДІОЛЕКЦІЙ, ДОДАТКОВИХ ДЕТАЛЬНИХ ІНСТРУКЦІЙ З ВИКОРИСТОЇ ПІДГОТОВКИ І КОНТРОЛЮ ЯКОСТІ
ПОГОДЖЕНО З ЄВРОПЕЙСЬКИМ МЕДИЦИНАЛЬНИМ АГЕНТСТВОМ (EMA) І ІТАЛІЙСЬКИМ АГЕНТСТВОМ НАРКОТИКІВ (AIFA)
Грудень 2013 року
Підвищений ризик серйозної кровотечі у пацієнтів з нестабільною стенокардією / інфарктом міокарда з підвищеним сегментом ST (UA) / NSTEMI при введенні EFIENT (прасугрел) перед діагностичною коронарографією.
Шановний лікар, шановний лікарю,
"Європейське агентство з лікарських засобів та Італійське агентство з лікарських засобів - AIFA, за погодженням з Daiichi -Sankyo та Eli Lilly Italia, хочуть повідомити вас про таку рекомендацію щодо застосування EFIENT (прасугрелу), антиагрегантного препарату, призначеного для лікування гострих коронарний синдром (ГКС) у пацієнтів, які проходять черезшкірне коронарне втручання (ЧКВ):
У пацієнтів з нестабільною стенокардією / інфарктом міокарда з підняттям сегмента ST / NSTEMI, коли коронарографію проводять протягом 48 годин після госпіталізації, навантажувальну дозу EFIENT слід вводити лише під час ЧКВ, щоб мінімізувати ризик кровотечі.
Ця рекомендація ґрунтується на результатах нещодавно завершеного клінічного дослідження у пацієнтів з NSTEMI, які планували пройти коронарографію через 2–48 годин після рандомізації. У дослідженні порівнювали ефекти введення початкової навантажувальної дози прасугрелу 30 мг перед коронарною ангіографією (у середньому 4 години), а потім «додаткову дозу 30 мг під час ЧКВ, з ефектом, отриманим від введення повного навантажувальна доза 60 мг під час ЧКВ. Результати показали більший ризик кровотечі, пов'язаний із застосуванням початкової навантажувальної дози перед коронарною ангіографією, з подальшою додатковою дозою під час ЧКВ порівняно з одноразовою навантажувальною дозою прасугрелу під час ЧКВ. Різниці в ефективності не було спостерігається між двома режимами дозування.
Дослідження "ACCOAST" під назвою: Порівняння прасугрелу під час перкутанного коронарного втручання або як попереднє лікування під час діагностики у пацієнтів з інфарктом міокарда без підвищення ST.
Дізнайтеся більше про аспекти безпеки
ACCOAST-це 30-денне дослідження, проведене у 4 033 пацієнтів з NSTEMI та підвищеним вмістом тропоніну, яким планувалося пройти коронарографію з подальшим ЧКВ через 2–48 годин після рандомізації. Пацієнти, які отримували навантажувальну дозу прасугрелу в середньому 30 мг за 4 години до коронарної ангіографії, а потім навантажувальну дозу 30 мг під час ЧКВ (n = 2037), мали підвищений ризик перипроцедурної кровотечі. (не пов'язане з операцією шунтування коронарних артерій) і не має додаткових переваг у порівнянні з пацієнтами, які отримували навантажувальну дозу 60 мг під час ЧКВ (n = 1996). Зокрема, частота складеної мішені серцево-судинної смерті, інфаркту міокарда, інсульту, термінової реваскуляризації або використання інгібітора глікопротеїну (ГП) IIb / IIIa "в рятувальній терапії" протягом 7 днів після рандомізації не була суттєво знижена у суб'єктів які отримували прасугрел до коронарографії порівняно з пацієнтами, які отримували повну навантажувальну дозу прасугрелу під час ЧКВ. Крім того, частота виконання основної мети безпеки, представленої усіма великими кровотечами відповідно до TIMI (АКШ та не-АКШ) протягом 7 днів після рандомізації у всіх обстежених, була значно вищою у суб’єктів, які отримували прасугрел у двох розділених дозах (4 годин до коронарної ангіографії та під час ЧКВ) порівняно з пацієнтами, які отримували повну завантажувальну дозу прасугрелу при одноразовому введенні під час ЧКВ.
Повідомлення про підозрювані побічні реакції
Лікарі та інші медичні працівники повинні повідомляти про будь -які підозрювані побічні реакції, пов'язані з ліками, що містять прасугрел.
Лікарі та інші медичні працівники повинні, згідно із законом, надсилати повідомлення про підозру на побічні реакції, використовуючи спеціальну паперову форму (доступна на веб -сайті http://www.agenziafarmaco.gov.it/sites/default/files/tipo_filecb84.pdf) або негайно заповнивши електронну форму в Інтернеті (http://www.agenziafarmaco.gov.it/sites/default/files/scheda_aifa_oper_sanitario16.07.2 012.doc), менеджеру з фармаконагляду закладу охорони здоров’я, до якого вони належать, або , якщо вони працюють у приватних закладах охорони здоров’я, через Департамент охорони здоров’я, - до менеджера з фармаконагляду, відповідального за цю область.
Подальша інформація
З питань та / або додаткової інформації звертайтесь до відділу "Медична інформація" Елі Ліллі, зателефонувавши за таким безкоштовним номером: 800117678, або написавши на адресу: [email protected]
Звіти про підозрювану побічну реакцію від лікарських засобів необхідно надсилати керівнику відділу фармаконагляду структури, до якої належить Оператор.
Ця інформаційна записка також публікується на веб -сайті АІФА (www.agenziafarmaco.it), регулярні консультації якого рекомендуються для отримання найкращої професійної та службової інформації для громадян.














.jpg)