Діючі речовини: Голімумаб
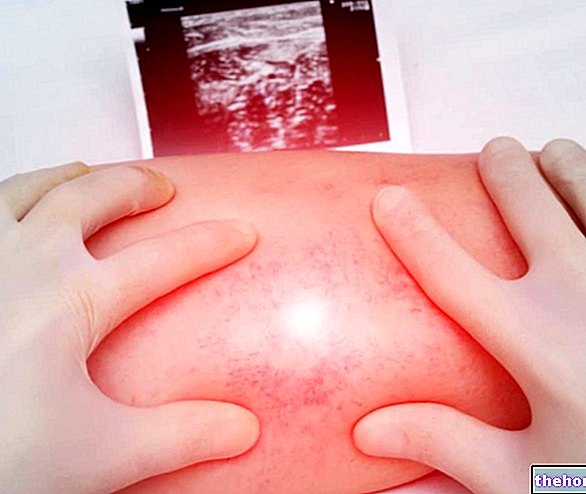
Симпоні 50 мг розчин для ін’єкцій у попередньо заповненій ручці
Вставки для упаковки Simponi доступні для розмірів упаковки:- Симпоні 50 мг розчин для ін’єкцій у попередньо заповненій ручці
- Симпоні 100 мг розчин для ін’єкцій у наповненій ручці
Показання Для чого використовується Симпоні? Для чого це?
Симпоні містить діючу речовину під назвою голімумаб.
Симпоні належить до групи ліків, які називаються "блокаторами ФНП". Застосовується у дорослих для лікування таких запальних захворювань:
- Ревматоїдний артрит
- Псоріатичний артрит
- Осьовий спондилоартрит, включаючи анкілозуючий спондилоартрит та нерентгенографічний осьовий спондилоартрит
- Виразковий коліт
У дітей з масою тіла не менше 40 кг Симпоні використовується для лікування поліартикулярного ювенільного ідіопатичного артриту.
Симпоні діє, блокуючи дію білка, який називається "фактором некрозу пухлини альфа" (TNF-α). Цей білок бере участь у запальних процесах організму, і, блокуючи його, можна зменшити запалення в організмі.
Ревматоїдний артрит
Ревматоїдний артрит - це запальне захворювання суглобів. Якщо у вас активний ревматоїдний артрит, вам спочатку буде надано лікування іншими препаратами. Якщо ви не реагуєте належним чином на ці ліки, вас лікуватимуть Сімпоні у поєднанні з іншим ліками, що називається метотрексатом:
- Зменшити ознаки та симптоми захворювання.
- Уповільнюють пошкодження кісток і суглобів.
- Поліпшити фізичні функції.
Псоріатичний артрит
Псоріатичний артрит - це запальне захворювання суглобів, яке зазвичай супроводжується псоріазом, запальним захворюванням шкіри. Якщо у вас активний псоріатичний артрит, вам спочатку будуть призначені інші ліки. Якщо ви не реагуєте належним чином на ці ліки, вам буде призначено лікування Симпоні для:
- Зменшити ознаки та симптоми захворювання.
- Уповільнюють пошкодження кісток і суглобів.
- Поліпшити фізичні функції.
Анкілозуючий спондилоартрит та нерентгенографічний осьовий спондилоартрит
Анкілозуючий спондилоартрит та нерентгенографічний осьовий спондилоартроз-запальні захворювання хребта. Якщо у вас є хвороба Бехтерева або нерентгенографічний осьовий спондилоартрит, вам спочатку будуть призначені інші ліки. Якщо ви не реагуєте належним чином на ці ліки, ви будете проходити лікування Симпоні:
- Зменшити ознаки та симптоми захворювання.
- Поліпшити фізичні функції.
Виразковий коліт
Виразковий коліт - це запальне захворювання кишечника. Якщо у вас виразковий коліт, вам спочатку дадуть інші ліки. Якщо ви не реагуєте належним чином на ці ліки, вам дадуть Сімпоні для лікування вашої хвороби.
Поліартикулярний ювенільний ідіопатичний артрит
Поліартикулярний ювенільний ідіопатичний артрит - це запальне захворювання, яке викликає біль і набряк у суглобах у дітей. Якщо у вашої дитини поліартикулярний ювенільний ідіопатичний артрит, вашій дитині спочатку дадуть інші ліки. Якщо Ваша дитина не реагує належним чином на ці ліки, Вашій дитині буде призначено Симпоні у поєднанні з метотрексатом для лікування захворювання.
Протипоказання Коли Симпоні не слід застосовувати
Не використовуйте Simponi:
- Якщо у вас алергія (гіперчутливість) до голімумабу або до будь -якого іншого інгредієнта цього препарату (перерахованого у розділі 6).
- Якщо у вас туберкульоз (ТБ) або будь -яка інша серйозна інфекція.
- Якщо у вас серцева недостатність середньої або важкої ступеня.
Якщо ви не впевнені, чи стосується вас будь -яка з вищезазначених умов, поговоріть зі своїм лікарем, фармацевтом або медсестрою перед застосуванням Симпоні.
Заходи безпеки при застосуванні Що потрібно знати, перш ніж приймати Симпоні
Перед застосуванням Симпоні поговоріть зі своїм лікарем, фармацевтом або медсестрою.
Інфекції
Негайно повідомте свого лікаря, якщо під час або після лікування препаратом Сімпоні у вас вже були або були симптоми інфекції. Симптомами інфекції є гарячка, кашель, задишка, грипоподібні симптоми, діарея, рани, проблеми з зубами або відчуття печіння при сечовипусканні.
- Ви можете легше заразитися інфекціями, використовуючи Simponi.
- Інфекції можуть прогресувати швидше і бути більш серйозними. Крім того, інфекції з минулого можуть повернутися.
Туберкульоз (ТБ)
Негайно повідомте лікаря, якщо ви помітили симптоми туберкульозу під час лікування. Симптоми туберкульозу включають постійний кашель, втрату ваги, відчуття втоми, лихоманку або нічну пітливість.
- Було зареєстровано кілька випадків туберкульозу у пацієнтів, які отримували Симпоні, в рідкісних випадках навіть у пацієнтів, які проходили лікування протитуберкульозними препаратами. Ваш лікар зробить аналізи, щоб перевірити, чи є у вас туберкульоз. Лікар запише ці аналізи на картку оповіщення пацієнта.
- Дуже важливо повідомити свого лікаря, якщо ви раніше хворіли на туберкульоз, або якщо ви тісно контактували з кимось, хто хворів на туберкульоз.
- Якщо ваш лікар вважає, що ви ризикуєте захворіти на туберкульоз, ви можете пройти лікування протитуберкульозними препаратами, перш ніж приймати Симпоні.
Вірус гепатиту В (HBV)
- Скажіть своєму лікарю, якщо ви є носієм, чи хворіли або перенесли гепатит В до того, як вам призначили Симпоні
- Скажіть своєму лікарю, якщо ви вважаєте, що у вас є ризик зараження гепатитом В.
- Ваш лікар повинен оцінити, чи є у вас гепатит В.
- Лікування блокаторами TNF, такими як Simponi, може викликати повторну активацію вірусу гепатиту В у пацієнтів, які переносять цей вірус, що в деяких випадках може призвести до смерті.
Інвазивні грибкові інфекції
Негайно повідомте лікаря, якщо ви жили або подорожували "місцем, де поширені інфекції, викликані певними типами грибків, які можуть вражати легені або інші частини тіла (так званий гістоплазмоз, кокцидіоїдомікоз або бластомікоз). Запитайте свого лікаря, якщо Ви не знаєте, чи поширені ці грибкові інфекції у тій місцевості, де ви жили або подорожували.
Рак і лімфома
Скажіть своєму лікарю, якщо у вас була або коли -небудь хворіла на лімфому (тип раку крові) або інші види раку, перш ніж ви отримаєте Симпоні.
- Якщо Ви використовуєте Симпоні або інші блокатори ФНП, Ви можете збільшити ризик розвитку лімфоми або іншого виду раку.
- Пацієнти з важким ревматоїдним артритом або іншими запальними станами, які тривалий час страждали від цього захворювання, можуть мати вищий за середній ризик розвитку лімфоми.
- Повідомлялося про рак, включаючи незвичайний, іноді смертельний рак, у дітей та підлітків, які приймали препарати, що блокують ФНП.
- У рідкісних випадках у пацієнтів, які приймали інші блокатори TNF, спостерігався специфічний та важкий тип лімфоми, яка називається гепатоспленова Т-клітинна лімфома. Більшість із цих пацієнтів були підлітками або молодими чоловіками. Ця форма раку зазвичай призводить до смерті. Майже всі ці пацієнти також отримували ліки, відомі як азатіоприн або 6-меркаптопурин. Скажіть своєму лікарю, якщо ви приймаєте азатіоприн або 6-меркаптопурин разом із Симпоні.
- Пацієнти з тяжкою персистуючою астмою, хронічною обструктивною хворобою легень (ХОЗЛ) або завзятими курцями можуть мати підвищений ризик раку при лікуванні Симпоні. Якщо у вас важка персистуюча астма, ХОЗЛ або ви завзято курите, вам слід обговорити з лікарем, чи доцільне лікування блокатором ФНП.
- Деякі пацієнти, які отримували голімумаб, розвинули певні типи раку шкіри. Якщо під час або після терапії ви відчуваєте будь -які зміни у зовнішньому вигляді шкіри або нарости на шкірі, повідомте про це свого лікаря.
Серцева недостатність
Негайно повідомте лікаря, якщо ви помітили нові або погіршення симптомів серцевої недостатності. Симптоми серцевої недостатності включають задишку або набряк ніг.
- Повідомлялося про випадки нового початку або загострення застійної серцевої недостатності при застосуванні блокаторів TNF, включаючи Симпоні. Деякі з цих пацієнтів померли.
- Якщо у вас легка серцева недостатність і ви лікуєтесь препаратом Симпоні, ваш лікар буде стежити за вами.
Захворювання нервової системи
Негайно повідомте лікаря, якщо у вас коли -небудь діагностували або розвивалися симптоми демієлінізуючого захворювання, такого як розсіяний склероз. Симптоми можуть включати зміни зору, слабкість в руках і ногах, оніміння або поколювання в будь -якій частині тіла. Ваш лікар вирішить, чи варто вам приймати Симпоні.
Стоматологічні операції або процедури
- Скажіть своєму лікарю, якщо у вас будуть якісь стоматологічні операції чи процедури.
- Скажіть хірургу або стоматологу, який виконує процедуру, що ви проходите курс лікування Simponi, показавши картку оповіщення пацієнта.
Аутоімунні захворювання
Скажіть своєму лікарю, якщо у вас з’являються симптоми захворювання, що називається вовчаком. Симптоми включають стійку висип, лихоманку, біль у суглобах та втому.
- У рідкісних випадках у людей, які отримували блокатори TNF, розвивався вовчак.
Хвороби крові
У деяких пацієнтів організм може не виробляти достатню кількість клітин крові, які допомагають організму боротися з інфекціями або зупинити кровотечу. Якщо у вас стійка лихоманка, яку ви не розумієте, синці або кровоточать легко або виглядаєте блідими, негайно зверніться до лікаря. Ваш лікар може прийняти рішення про припинення лікування.
Якщо ви не впевнені, чи стосується вас будь -яка з вищезазначених умов, поговоріть зі своїм лікарем або фармацевтом перед застосуванням Симпоні.
Щеплення
Скажіть своєму лікарю, якщо ви нещодавно були щеплені або плануєте щеплення.
- Ви не повинні отримувати певні (живі) вакцини під час лікування Симпоні.
- Деякі щеплення можуть викликати інфекції. Якщо ви отримували Симпоні під час вагітності, у вашої дитини може бути підвищений ризик зараження цією інфекцією протягом приблизно шести місяців після останньої дози, отриманої під час вагітності. Важливо повідомити свого педіатра та інших медичних працівників про застосування Симпоні. може вирішити, коли дитина повинна отримати якісь вакцини.
Порадьтеся з лікарем вашої дитини щодо щеплень для вашої дитини. Якщо можливо, перед використанням Симпоні Ваша дитина повинна бути в курсі всіх щеплень.
Інфекційні терапевтичні засоби
Поговоріть зі своїм лікарем, якщо ви нещодавно приймали або плануєте лікування інфекційним терапевтичним засобом (наприклад, ін'єкція БЦЖ, що використовується для лікування раку).
Алергічні реакції
Негайно повідомте лікаря, якщо у вас виникли симптоми алергічної реакції після лікування Симпоні. Симптоми алергічної реакції можуть включати набряк обличчя, губ, рота чи горла, що може спричинити утруднення ковтання або дихання, висип на шкірі, кропив’янку, набряк кистей, стоп та щиколоток.
- Деякі з цих реакцій можуть бути важкими або, рідко, загрожувати життю.
- Деякі з цих реакцій виникають після першого введення Симпоні.
Діти та підлітки
Симпоні не рекомендується дітям вагою менше 40 кг з поліартикулярним ювенільним ідіопатичним артритом або дітям та підліткам віком до 18 років для будь -яких інших станів.
Взаємодії Які ліки або продукти харчування можуть змінити дію Симпоні
- Повідомте свого лікаря або фармацевта, якщо ви приймаєте, нещодавно приймали або могли б приймати будь-які інші ліки, включаючи будь-які інші ліки для лікування ревматоїдного артриту, поліартикулярного ювенільного ідіопатичного артриту, псоріатичного артриту, хвороби Бехтерева, осьового спондилоартриту, нерентгенографічного чи виразкового коліту.
- Не слід приймати Симпоні з лікарськими засобами, що містять діючу речовину анакінру або абатацепт. Ці ліки використовуються для лікування ревматичних захворювань.
- Повідомте свого лікаря або фармацевта, якщо ви приймаєте інші ліки, що впливають на імунну систему.
- Його не можна лікувати певними (живими) вакцинами під час використання Симпоні.
Якщо ви не впевнені, чи стосується вас будь -яка з вищезазначених умов, поговоріть зі своїм лікарем або фармацевтом перед застосуванням Симпоні.
Попередження Важливо знати, що:
Вагітність та годування груддю
Перед застосуванням Симпоні поговоріть зі своїм лікарем, якщо:
- Ви вагітні або плануєте завагітніти під час використання Симпоні. Дія цього препарату на вагітних невідома. Застосування препарату Сімпоні вагітним жінкам не рекомендується. Якщо вам призначено лікування препаратом Сімпоні, вам слід уникати вагітності, використовуючи адекватну контрацепцію під час лікування та протягом щонайменше 6 місяців після останньої ін’єкції Сімпоні.
- Перед годуванням груддю останнє лікування Симпоні повинно бути принаймні на 6 місяців раніше.
- Якщо ви отримували Сімпоні під час вагітності, у вашої дитини може бути підвищений ризик зараження. Важливо повідомити свого педіатра та інших медичних працівників про ваше застосування Симпоні до того, як Ваша дитина отримає будь -які вакцини (докладнішу інформацію див. щеплення).
Якщо ви вагітні або годуєте грудьми, думаєте, що можете бути вагітними або плануєте народження дитини, зверніться за порадою до свого лікаря або фармацевта, перш ніж приймати цей препарат.
Водіння автомобіля та роботу з машинами
Симпоні може незначно погіршити вашу здатність керувати автомобілем та працювати з інструментами або машинами. Після використання препарату Симпоні може виникнути запаморочення.
Сімпоні містить латекс і сорбіт
Чутливість до латексу
Чутливість до латексу Одна частина попередньо заповненої ручки, ковпачок, що закриває голку, містить латекс. Оскільки латекс може викликати серйозні алергічні реакції, повідомте свого лікаря перед застосуванням Симпоні, якщо у вас або вашого опікуна є алергія на латекс.
Непереносимість сорбіту
Симпоні містить сорбіт (Е420). Якщо ваш лікар сказав вам, що у вас «непереносимість деяких цукрів, зверніться до лікаря, перш ніж приймати цей препарат.
Дозування та спосіб застосування Як користуватися Симпоні: Дозування
Завжди використовуйте цей препарат точно так, як вам сказав ваш лікар або фармацевт. Якщо є сумніви, слід проконсультуватися з лікарем або фармацевтом.
Скільки дається Simponi
Ревматоїдний артрит, псоріатичний артрит та осьовий спондилоартрит, включаючи анкілозуючий спондиліт та нерентгенографічний осьовий спондилоартрит:
- Рекомендована доза становить 50 мг (вміст 1 наповненої ручки), що вводиться один раз на місяць, в один і той же день кожного місяця.
- Поговоріть зі своїм лікарем, перш ніж приймати четверту дозу. Ваш лікар вирішить, чи варто продовжувати лікування Симпоні.
- Якщо ви важите більше 100 кг, дозу можна збільшити до 100 мг (вміст 2 попередньо заповнених ручок), що вводиться раз на місяць, завжди в один і той же день кожного місяця.
Поліартикулярний ювенільний ідіопатичний артрит:
- Рекомендована доза становить 50 мг один раз на місяць, в один і той же день кожного місяця.
- Поговоріть з лікарем вашої дитини, перш ніж дитина прийме четверту дозу. Лікар вашої дитини вирішить, чи варто продовжувати лікування Симпоні.
Виразковий коліт
- У наведеній нижче таблиці показано, як Ви зазвичай будете використовувати цей препарат.
- У пацієнтів з масою тіла менше 80 кг 50 мг (вміст 1 заповненої ручки) через 4 тижні після останнього лікування, потім кожні 4 тижні.
- У пацієнтів з масою тіла 80 кг і більше 100 мг (вміст 2 попередньо заповнених ручок) через 4 тижні після останнього лікування, потім кожні 4 тижні.
Як дається Simponi
- Симпоні вводять шляхом ін’єкції під шкіру (підшкірно).
- Спочатку ваш лікар або медперсонал вводять Сімпоні, проте Ви та Ваш лікар можете вирішити, що Ви можете вводити Симпоні самостійно.
Поговоріть зі своїм лікарем, якщо у вас виникнуть запитання щодо самостійного введення ін’єкції. В кінці цієї брошури ви знайдете докладну "Інструкцію щодо введення".
Якщо ви забули використовувати Simponi
Якщо ви забули використати Сімпоні у запланований день, введіть пропущену дозу, як тільки ви пам’ятаєте.
Не використовуйте подвійну дозу, щоб компенсувати пропущену дозу.
Коли вводити наступну дозу:
- Якщо ви запізнюєтеся менше ніж на 2 тижні, вкажіть пропущену дозу, як тільки ви згадаєте, і продовжуйте слідувати своєму початковому графіку.
- Якщо ви запізнилися більш ніж на 2 тижні, вкажіть забуту дозу, як тільки ви згадаєте, і повідомте свого лікаря або фармацевта та запитайте, коли вам слід прийняти наступну дозу.
Якщо ви не впевнені, що робити, запитайте свого лікаря, фармацевта або медсестру.
Якщо ви припините використання Simponi
Якщо ви плануєте припинити застосування Симпоні, спочатку поговоріть зі своїм лікарем або фармацевтом.
Якщо у вас виникнуть додаткові запитання щодо застосування цього препарату, зверніться до лікаря або фармацевта.
Передозування Що робити, якщо ви прийняли занадто багато препарату Симпоні
Якщо ви вживали або давали занадто багато препарату Сімпоні (вводили занадто багато за одну дозу або використовували його занадто часто), негайно повідомте про це свого лікаря або фармацевта. Завжди візьміть із собою зовнішню коробку та цю інструкцію, навіть якщо вона порожня.
Побічні ефекти Які побічні ефекти у Симпоні
Як і всі ліки, цей препарат може викликати побічні ефекти, хоча вони виникають не у всіх. У деяких пацієнтів можуть виникнути серйозні побічні ефекти, які можуть потребувати медикаментозного лікування. Ризик деяких побічних ефектів вищий при застосуванні дози 100 мг порівняно з дозою 50 мг. Побічні ефекти також можуть виникнути через кілька місяців після останньої ін’єкції.
Негайно повідомте лікаря, якщо ви помітили будь -який з таких серйозних побічних ефектів Симпоні, які включають:
- алергічні реакції, які можуть бути важкими або рідко небезпечними для життя (рідко).Симптоми алергічної реакції можуть включати набряк обличчя, губ, рота або горла, що може спричинити утруднення ковтання або дихання, висип на шкірі, кропив’янку, набряк кистей рук, ніг або щиколоток. Деякі з цих реакцій виникли після першого застосування Симпоні.
- важкі інфекції (включаючи туберкульоз, бактеріальні інфекції, включаючи важкі інфекції крові та пневмонію, важкі грибкові інфекції та інші умовно -патогенні інфекції) (поширені). Симптомами інфекції можуть бути гарячка, втома, (постійний) кашель, задишка, грипоподібні симптоми, втрата ваги, нічна пітливість, діарея, рани, проблеми з зубами та відчуття печіння при сечовипусканні.
- реактивація вірусу гепатиту В, якщо ви є носієм або раніше хворіли на гепатит В (рідко). Симптоми можуть включати пожовтіння шкіри та очей, темно -коричневу сечу, біль у правій частині живота, лихоманку, погане самопочуття, нездужання та відчуття сильної втоми.
- захворювання нервової системи, такі як розсіяний склероз (рідко). Симптоми захворювання нервової системи можуть включати зміни зору, слабкість в руках або ногах, оніміння або поколювання в будь -якій частині тіла.
- рак лімфатичних вузлів (лімфома) (рідко). Симптоми лімфоми можуть включати збільшення лімфатичних вузлів, зниження ваги або підвищення температури тіла.
- серцева недостатність (рідко). Симптоми серцевої недостатності можуть включати задишку або набряк ніг.
- ознаки порушень імунної системи називаються: - вовчак (рідко). Симптоми можуть включати біль у суглобах або висип на щоках або руках, чутливі до сонця. - саркоїдоз (рідко). Симптоми можуть включати постійний кашель, задишку, біль у грудях, лихоманку, збільшення лімфатичних вузлів, втрату ваги, висип на шкірі та помутніння зору.
- набряк дрібних кровоносних судин (васкуліт) (рідко). Симптоми можуть включати лихоманку, головний біль, втрату ваги, нічну пітливість, висип та нервові проблеми, такі як оніміння та поколювання.
- рак шкіри (нечасто). Симптоми раку шкіри можуть включати зміни у зовнішньому вигляді шкіри або нарости на шкірі.
- захворювання крові (поширене). Симптоми захворювання крові можуть включати лихоманку, яка не проходить, сильну схильність до синців або кровотеч або дуже блідий вигляд.
- рак крові (лейкемія) (рідко). Симптоми лейкемії можуть включати лихоманку, почуття втоми, часті інфекції, синці та нічну пітливість.
Негайно повідомте лікаря, якщо ви помітили будь -який із перерахованих вище симптомів.
Наступні додаткові побічні ефекти спостерігалися при застосуванні Симпоні:
Дуже поширені побічні ефекти (можуть виникнути більш ніж у 1 з 10 осіб):
- Інфекції верхніх дихальних шляхів, біль у горлі або захриплість, застуда
Поширені побічні ефекти (можуть виникнути до 1 з 10 осіб):
- Аномальні печінкові проби (підвищення печінкових ферментів), виявлені під час аналізу крові, зробленого вашим лікарем
- Відчувається запаморочення
- Головний біль
- Відчуття оніміння або поколювання
- Поверхневі грибкові інфекції
- Абсцес
- Бактеріальні інфекції (наприклад, целюліт)
- Зниження еритроцитів
- Позитивний аналіз крові на вовчак
- Алергічні реакції
- Порушення травлення
- Біль у животі
- Почуття нудоти (нудота)
- Вплив
- Бронхіт
- Інфекція пазухи
- Герпес на обличчі
- Гіпертонія
- Лихоманка
- Астма, задишка, хрипи
- Розлади шлунка та кишечника, які включають запалення внутрішньої частини шлунка та товстої кишки, що може викликати лихоманку
- Біль і виразки в роті
- Реакції в місці ін’єкції (включаючи почервоніння, твердість, біль, синці, свербіж, поколювання та подразнення)
- Втрата волосся
- Висип і свербіж шкіри
- Труднощі зі сном
- Депресія
- Відчуття слабкості
- Переломи кісток
- Біль у грудях
Нечасті побічні ефекти (можуть виникнути у 1 з 100 осіб):
- Інфекція нирок
- Рак, включаючи рак шкіри та неракові грудки або невеликі маси, включаючи родимки
- Пухирі на шкірі
- Псоріаз (включаючи долоні та / або підошви ніг та / або у вигляді шкірних пустул)
- Скорочення тромбоцитів
- Зниження лейкоцитів
- Комбіноване зниження тромбоцитів, еритроцитів та лейкоцитів
- Розлади щитовидної залози
- Підвищення рівня цукру в крові
- Підвищення рівня холестерину в крові
- Порушення балансу
- Порушення зору
- Відчуття нерегулярного серцебиття
- Звуження судин серця
- Згустки крові
- Почервоніння
- Запор
- Хронічне запалення легенів
- Кислотний рефлюкс
- Камені в жовчі
- Проблеми з печінкою
- Розлади грудей
- Порушення менструального циклу
Рідкісні побічні ефекти (можуть виникнути до 1 з 1000 осіб):
- Неможливість кісткового мозку виробляти клітини крові
- Інфекція суглобів або навколишніх тканин
- Складне зцілення
- Запалення кровоносних судин внутрішніх органів
- Лейкемія
- Меланома (тип раку шкіри)
- Лущення шкіри
- Імунологічні порушення, які можуть вражати легені, шкіру та лімфатичні вузли (дуже часто зустрічаються як саркоїдоз)
- Біль і зміна кольору в пальцях рук або ніг
- Порушення смаку
- Розлади сечового міхура
- Проблеми з нирками
- Запалення кровоносних судин на шкірі, що викликає висип
Частота побічних ефектів невідома:
- Меркель -клітинний рак (тип раку шкіри)
- Рідкісний рак крові, що вражає переважно молодих людей (гепатоспленочна Т-клітинна лімфома)
Повідомлення про побічні ефекти
Якщо у вас виникли будь -які побічні ефекти, зверніться до свого лікаря, фармацевта або медсестри.Це включає будь -які можливі побічні ефекти, не зазначені у цій брошурі. Ви також можете повідомити про побічні ефекти безпосередньо за допомогою національної системи повідомлень, наведеної у Додатку V. Побічні ефекти, яким ви можете допомогти надайте додаткову інформацію про безпеку цього ліки.
Термін придатності та утримання
- Зберігайте цей препарат подалі від очей та недоступного для дітей місця.
- Не використовуйте цей препарат після закінчення терміну придатності, зазначеного на етикетці та картонній упаковці після "EXP". Термін придатності відноситься до останнього дня цього місяця.
- Зберігати в холодильнику (2 ° C-8 ° C). Не заморожувати.
- Зберігайте попередньо заповнену ручку у зовнішній коробці, щоб захистити ліки від світла.
- Не використовуйте цей препарат, якщо ви помітили, що рідина не має світлого або світло -жовтого кольору, помутніла або містить сторонні частинки.
- Не викидайте будь -які ліки через стічні води або побутові відходи. Запитайте у свого лікаря або фармацевта, як викидати ліки, які ви більше не використовуєте. Це допоможе захистити навколишнє середовище.
Інша інформація
Що містить Сімпоні
Діюча речовина - голімумаб. Одна наповнена ручка 0,5 мл містить 50 мг голімумабу.
Інші інгредієнти: сорбіт (Е420), L-гістидин, L-гістидин моногідрохлорид моногідрат, полісорбат 80 та вода для ін’єкцій.
Зовнішній вигляд Сімпоні та вміст упаковки
Сімпоні поставляється у вигляді розчину для ін’єкцій у одноразовому наповненому перо. Сімпоні випускається в упаковках, що містять 1 попередньо заповнену ручку, та багатокомпонентних упаковках, що містять 3 (3 упаковки по 1) попередньо заповнених ручок. Не всі розміри упаковок можна продавати.
Розчин прозорий до злегка опалесцентний (блискучий, як перлина), безбарвний до світло -жовтого кольору і може містити деякі дрібні напівпрозорі або білі білі частинки. Не використовуйте Симпоні, якщо розчин змінив колір, помутнів або містить видимі сторонні частинки.
Джерело з інформацією про упаковку: AIFA (Італійське агентство з лікарських засобів). Вміст, опублікований у січні 2016 р. Наявна інформація може бути не актуальною.
Щоб мати доступ до найновішої версії, бажано зайти на веб-сайт AIFA (Італійське агентство з лікарських засобів). Відмова від відповідальності та корисна інформація.
01.0 НАЗВА ЛЕКАРСТВЕННОГО ПРОДУКТУ
SIMPONI 50 МГ ІНЖЕКЦІЙНИЙ РОЗЧИН
02.0 ЯКІСНИЙ І КІЛЬКІСНИЙ СКЛАД
Симпоні 50 мг розчин для ін’єкцій у попередньо заповненій ручці
Одна наповнена ручка 0,5 мл містить 50 мг голімумабу *.
Симпоні 50 мг розчин для ін’єкцій у попередньо заповненому шприці
Один наповнений шприц 0,5 мл містить 50 мг голімумабу *.
* IgG1 моноклональне антитіло людини? одержують з лінії клітин мишачої гібридоми з технологією рекомбінантної ДНК.
Допоміжна речовина з відомим ефектом:
Кожна наповнена ручка містить: 20,5 мг сорбітолу для дози 50 мг.
Кожен попередньо заповнений шприц містить: 20,5 мг сорбітолу для дози 50 мг.
Повний список допоміжних речовин див. У розділі 6.1.
03.0 ФАРМАЦЕВТИЧНА ФОРМА
Розчин для ін’єкцій у попередньо заповненій ручці (ін’єкція), SmartJect
Розчин для ін’єкцій у попередньо заповненому шприці (ін’єкція)
Розчин прозорий до слабо опалесцентного, від безбарвного до блідо -жовтого.
04.0 КЛІНІЧНА ІНФОРМАЦІЯ
04.1 Терапевтичні показання
Ревматоїдний артрит (РА)
Симпоні у поєднанні з метотрексатом (МТХ) показаний для:
• лікування помірного та важкого активного ревматоїдного артриту у дорослих пацієнтів, коли відповідь на модифіковані хворобою протиревматичні препарати (ДМАРД), включаючи МТХ, була недостатньою.
• лікування важкого, активного та прогресуючого ревматоїдного артриту у дорослих, які раніше не лікувалися МТХ.
Було показано, що Simponi у поєднанні з MTX зменшує швидкість прогресування пошкодження суглоба, виміряне за допомогою рентгенівських променів, та покращує фізичні функції.
Ювенільний ревматоїдний артрит
Поліартикулярний ювенільний ідіопатичний артрит (ПІА)
Симпоні у поєднанні з МТХ показаний для лікування поліартикулярного ювенільного ідіопатичного артриту у дітей вагою щонайменше 40 кг, які неадекватно реагували на попередню терапію МТХ.
Псоріатичний артрит (ПП)
Симпоні, окремо або в комбінації з метотрексатом (МТХ), показаний для лікування активного та прогресуючого псоріатичного артриту у дорослих, коли відповідь на попереднє лікування DMARD була недостатньою. Було показано, що Симпоні зменшує швидкість прогресування препарату. ураження периферичних суглобів, виміряне за допомогою рентгенівського випромінювання у пацієнтів з підтипами симетричних поліартикулярних захворювань (див. розділ 5.1), а також для поліпшення фізичної функції.
Осьовий спондилоартроз
Анкілозуючий спондиліт (АС)
Симпоні призначається для лікування важкого, активного анкілозуючого спондиліту у дорослих, які не реагували належним чином на звичайну терапію.
Нерентгенографічний осьовий спондилоартроз (осьовий SpA nr)
Симпоні призначений для лікування дорослих пацієнтів з важким активним нерентгенографічним осьовим спондилоартритом з об’єктивними ознаками запалення, на що свідчать дані про підвищений С-реактивний білок (СРБ) та / або магнітно-резонансну томографію (МРТ), які мали неадекватну відповідь або мають непереносимість нестероїдних протизапальних засобів (НПЗЗ).
Виразковий коліт (CU)
Симпоні показаний для лікування помірного та важкого активного виразкового коліту у дорослих пацієнтів, які не реагували належним чином на звичайну терапію, включаючи кортикостероїди та 6-меркаптопурин (6-МП) або азатіоприн (AZA), або мають непереносимість або для яких існує медичне протипоказання до цієї терапії.
04.2 Дозування та спосіб введення
Лікування Сімпоні має розпочинати та контролювати лікар-спеціаліст, який має досвід у діагностиці та лікуванні ревматоїдного артриту, поліартикулярного ювенільного ідіопатичного артриту, псоріатичного артриту, хвороби Бехтерева, нерентгенографічного осьового спондилоартриту чи виразкового коліту.Пацієнтам, які отримують Симпоні, слід повідомити пацієнта Картка.
Дозування
Ревматоїдний артрит
Симпоні 50 мг вводять один раз на місяць, в один і той же день кожного місяця.
Симпоні слід вводити одночасно з МТХ.
Псоріатичний артрит, анкілозуючий спондиліт або нерентгенографічний осьовий спондилоартрит
Симпоні 50 мг вводять один раз на місяць, в один і той же день кожного місяця.
За всіма вищезазначеними ознаками наявні дані свідчать про те, що клінічна відповідь зазвичай досягається протягом 12-14 тижнів після початку лікування (після 3-4 доз). Необхідно розглянути можливість продовження терапії у пацієнтів, які не показують доказів терапевтичної користі протягом цього терміну.
Пацієнти з масою тіла більше 100 кг
При всіх вищезазначених ознаках у пацієнтів з РА, АП, СА або осьовим SpA nr вагою понад 100 кг, які не досягають адекватної клінічної відповіді після 3 або 4 доз, збільшення дози голімумабу до 100 мг 1 раз на місяць, враховуючи підвищений ризик розвитку деяких серйозних побічних реакцій на ліки при застосуванні дози 100 мг порівняно з дозою 50 мг (див. розділ 4.8). Необхідно розглянути можливість продовження терапії у пацієнтів, які не мають жодних доказів терапевтичної користі після прийому 3- 4 додаткові дози по 100 мг.
Виразковий коліт
Пацієнти з масою тіла менше 80 кг
Початкова доза Симпоні становить 200 мг, потім - 100 мг на 2 -му тижні, потім - 50 мг кожні 4 тижні (див. Розділ 5.1).
Пацієнти з масою тіла більше або дорівнює 80 кг
Початкова доза Симпоні становить 200 мг, потім - 100 мг на 2 -му тижні, потім - 100 мг кожні 4 тижні (див. Розділ 5.1).
Під час підтримуючого лікування кортикостероїди можна поступово знижувати відповідно до рекомендацій клінічної практики.
Наявні дані свідчать про те, що клінічна відповідь зазвичай досягається протягом 12-14 тижнів лікування (після 4 доз). Слід розглянути можливість продовження терапії у пацієнтів, які протягом цього часу не демонструють доказів терапевтичної користі.
Пропущена доза
Якщо пацієнт забув ввести Симпоні в запланований день, пропущену дозу слід ввести, як тільки пацієнт пам’ятає. Пацієнтам слід наказувати не вводити подвійну дозу, щоб компенсувати пропущену дозу.
Наступну дозу слід вводити згідно з наступним посібником:
• Якщо відстрочена доза становить менше 2 тижнів, пацієнт повинен ввести пропущену дозу і продовжувати дотримуватися свого початкового графіка.
• Якщо затримка дозування становить більше 2 тижнів, пацієнт повинен ввести пропущену дозу, і з дня введення цієї ін’єкції необхідно визначити новий графік дозування.
Особливі популяції
Люди похилого віку (≥ 65 років)
У людей похилого віку корекція дози не потрібна.
Порушення функції нирок та печінки
Симпоні не вивчався у цих популяціях пацієнтів. Рекомендації щодо доз не можуть бути надані.
Педіатричне населення
Безпека та ефективність препарату Симпоні у пацієнтів віком до 18 років за показаннями, відмінними від ПІА, не встановлені.
Поліартикулярний ювенільний ідіопатичний артрит
Сімпоні 50 мг, що призначається один раз на місяць, в один і той же день кожного місяця, дітям з масою тіла не менше 40 кг.
Наявні дані свідчать про те, що клінічна відповідь зазвичай досягається протягом 12-14 тижнів лікування (через 3-4 дози). Продовження терапії слід переглянути у дітей, у яких протягом цього періоду немає доказів терапевтичної користі.
Спосіб введення
Симпоні призначений для підшкірного застосування. Після адекватного навчання техніці підшкірної ін’єкції пацієнти зможуть самостійно ін’єктувати Симпоні, якщо їх лікар визначить, що вони здатні, при необхідності під відповідним наглядом лікаря. Пацієнти повинні бути проінструктовані ввести повну кількість препарату Сімпоні відповідно до повної інструкції щодо введення, зазначеної в інструкції з експлуатації.
Інструкції щодо введення див. У розділі 6.6.
04.3 Протипоказання
Підвищена чутливість до активної речовини або до будь -якої з допоміжних речовин, перерахованих у розділі 6.1.
Активний туберкульоз (ТБ) або інші серйозні інфекції, такі як сепсис та умовно -патогенні інфекції (див. Розділ 4.4).
Пацієнти з помірною або тяжкою серцевою недостатністю (NYHA Клас III / IV - Нью -Йоркська асоціація серця) (див. Розділ 4.4).
04.4 Спеціальні попередження та відповідні запобіжні заходи щодо використання
Інфекції
До, під час та після лікування препаратом Симпоні пацієнти повинні ретельно спостерігатися на наявність інфекцій, включаючи туберкульоз. Оскільки елімінація голімумабу може зайняти до 5 місяців, протягом цього періоду слід продовжувати моніторинг. Подальше лікування Симпоні не слід проводити, якщо у пацієнта розвиваються важкі інфекції або сепсис (див. Розділ 4.3).
Симпоні не можна застосовувати пацієнтам з клінічно значущою, активною інфекцією. Необхідно бути обережним при розгляді застосування Симпоні пацієнтам з хронічною інфекцією або рецидивуючими інфекціями в анамнезі. Пацієнтів слід належним чином поінформувати про необхідність уникати впливу потенційних факторів ризику інфекцій.
Пацієнти, які приймають ліки, що блокують ФНП, більш схильні до важких інфекцій.
У пацієнтів, які лікувались препаратом Симпоні, повідомлялося про бактеріальні інфекції (включаючи сепсис та пневмонію), мікобактеріальні (включаючи туберкульоз), інвазивні грибкові інфекції та умовно -патогенні інфекції, включаючи летальні наслідки. Деякі з цих серйозних інфекцій розвинулися у пацієнтів, які отримували супутню імуносупресивну терапію, що, крім основного захворювання, може схилити їх до інфекцій. Пацієнти, у яких під час лікування Симпоні розвивається нова інфекція, повинні бути ретельно контрольовані та пройти "ретельну діагностичну оцінку. Прийом препарату Симпоні слід припинити, якщо у пацієнта розвивається нова важка інфекція або сепсис та розпочато відповідну" терапію. Антимікробну або протигрибкову терапію, поки інфекція не стане Для пацієнтів, які жили або подорожували в регіони, де інвазивні грибкові інфекції, такі як гістоплазмоз, кокцидіоїдомікоз або бластомікоз, є ендемічними, переваги та ризики лікування Сімпоні слід ретельно розглянути перед початком терапії Симпоні. У пацієнтів з високим ризиком, які отримують лікування Сімпоні, інвазивну грибкову інфекцію, слід запідозрити, якщо у них розвинеться важке системне захворювання. Якщо можливо, діагноз та призначення емпіричної протигрибкової терапії у цих пацієнтів слід проводити за погодженням з лікарем, який має досвід лікування пацієнтів з інвазивними грибковими інфекціями.
Туберкульоз
Повідомлялося про випадки туберкульозу у пацієнтів, які отримували Симпоні. Слід зазначити, що в більшості цих випадків це був позалегеневий туберкульоз, локалізований та дифузний.
Перед початком лікування Симпоні всіх пацієнтів слід обстежити як на активний, так і на неактивний («латентний») туберкульоз. Ця оцінка повинна включати детальну історію хвороби, включаючи особисту історію туберкульозу або можливий попередній контакт з джерелом туберкульозної інфекції та попередню та / або супутню імуносупресивну терапію. Усім пацієнтам слід провести відповідні діагностичні тести, такі як шкірні або туберкулінові аналізи та рентген грудної клітки (можуть застосовуватися місцеві рекомендації). Рекомендується повідомляти про ці тести в картці оповіщення пацієнта. Рецепторам нагадується про ризик хибнонегативних результатів шкірного тесту на туберкулін, особливо у важкохворих або пацієнтів з ослабленим імунітетом.
Якщо діагностовано активний туберкульоз, терапію Сімпоні не слід розпочинати (див. Розділ 4.3).
При підозрі на прихований туберкульоз слід звернутися до лікаря з досвідом лікування туберкульозу. У всіх ситуаціях, описаних нижче, баланс користь / ризик терапії Симпоні повинен бути ретельно продуманий.
Якщо діагностується неактивний ("латентний") туберкульоз, антитуберкульозну терапію прихованого туберкульозу слід розпочати до початку терапії Сімпоні відповідно до місцевих рекомендацій.
У пацієнтів, які мають багато чи значні фактори ризику розвитку туберкульозу та мають негативний тест на прихований туберкульоз, перед початком застосування препарату Симпоні слід розглянути можливість протитуберкульозної терапії. пацієнти з анамнезом латентного або активного туберкульозу в анамнезі, для яких адекватний курс лікування не може бути підтверджений.
Випадки активного туберкульозу мали місце у пацієнтів, які отримували Симпоні під час та після лікування прихованого туберкульозу. Пацієнти, які проходять лікування препаратом Сімпоні, повинні бути ретельно обстежені на наявність ознак та симптомів активного туберкульозу, включаючи пацієнтів, у яких негативний тест на латентний туберкульоз, пацієнтів, які лікуються від прихованого туберкульозу, або пацієнтів, які раніше проходили лікування прихованого туберкульозу.
Всім пацієнтам слід порадити звернутися до лікаря, якщо під час або після лікування Симпоні з’являються ознаки / симптоми, що свідчать про туберкульоз (наприклад, постійний кашель, виснаження / втрата ваги, субфебрильна температура).
Реактивація вірусу гепатиту В.
Реактивація гепатиту В спостерігалася у пацієнтів, які отримували антагоніст ФНП, включаючи Симпоні, і які були хронічними носіями цього вірусу (тобто позитивно на поверхневий антиген). У деяких випадках наступали летальні наслідки.
Пацієнтів слід обстежити на наявність інфекції ВГВ перед початком лікування Симпоні.Пацієнтам, у яких позитивний тест на ВГВ, рекомендується проконсультуватися з лікарем, який має досвід лікування гепатиту В.
Носіїв вірусу гепатиту В, які потребують лікування Симпоні, слід ретельно контролювати на наявність ознак та симптомів активної інфекції вірусу гепатиту В протягом усього періоду терапії та протягом кількох місяців після закінчення терапії. терапію в поєднанні з терапією антагоністами ФНП для запобігання повторної активації вірусу гепатиту В. У пацієнтів, у яких розвивається реактивація вірусу гепатиту В, лікування Симпоні слід припинити та розпочати ефективну противірусну терапію з відповідним підтримуючим лікуванням.
Злоякісні новоутворення та лімфопроліферативні захворювання
Потенційна роль терапії інгібіторами ФНП у розвитку злоякісних пухлин невідома. На підставі наявних знань неможливо виключити можливий ризик розвитку лімфоми, лейкемії або інших злоякісних пухлин у пацієнтів, які отримують антагоніст ФНП. Слід бути обережним при розгляді терапії інгібіторами ФНП у пацієнтів із злоякісними захворюваннями в анамнезі або при розгляді продовження лікування у пацієнтів, у яких розвивається злоякісне новоутворення.
Злоякісні новоутворення у дітей
У постмаркетинговому досвіді повідомлялося про злоякісні пухлини, деякі з летальним результатом, серед дітей, підлітків та молодих людей (до 22 років), які отримували блокатори ФНО (початок терапії ≤ 18 років) Приблизно у половині випадків Інші випадки були представлені різними злоякісними утвореннями і включали рідкісні злоякісні утворення, зазвичай пов'язані з імуносупресією. Не можна виключити ризик розвитку злоякісних новоутворень у дітей та підлітків, які отримують інгібітори ФНП.
Лімфома та лейкемія
На контрольованих фазах клінічних випробувань з усіма інгібіторами ФНП, включаючи Симпоні, спостерігалося більше випадків лімфоми серед пацієнтів, які отримували лікування проти ФНП, порівняно з пацієнтами контрольної групи. Під час клінічних випробувань Фази IIb та III Симоні при РА, АП та СА частота лімфом у пацієнтів, які отримували Сімпоні, була вищою, ніж очікувалося, у загальній популяції. збільшення фонового ризику розвитку лімфоми та лейкемії у пацієнтів з ревматоїдним артритом з тривалим, високоактивним запальним захворюванням, що ускладнює оцінку ризику.
У постмаркетинговому періоді повідомлялося про поодинокі випадки гепатоспленочної Т-клітинної лімфоми (HSTCL) у пацієнтів, які отримували інші блокатори ФНП (див. Розділ 4.8). Ця рідкісна форма Т-клітинної лімфоми має надзвичайно агресивний перебіг і зазвичай летальний результат Більшість випадків траплялося у підлітків та молодих дорослих чоловіків, майже всі отримували супутнє лікування азатіоприном (AZA) або 6-меркаптопурином (6-МП) при запальних захворюваннях кишечника. Необхідно ретельно розглянути потенційний ризик комбінації АЗА або 6-МП та Симпоні. Не можна виключати ризик розвитку гепатоспленочної Т-клітинної лімфоми у пацієнтів, які отримують блокатори ФНО.
Злоякісні новоутворення, крім лімфоми
На контрольованих фазах клінічних досліджень Фази IIb та III, проведених із препаратом Симпоні при РА, АП, СА та КУ, частота злоякісних новоутворень, відмінних від лімфоми (виключаючи немеланомний рак шкіри), була подібною між групою лікування Симпоні та контрольною групою .
Дисплазія товстої кишки / карцинома
Невідомо, чи впливає лікування голімумабом на ризик розвитку дисплазії або раку товстої кишки. Усі пацієнти з виразковим колітом, які мають підвищений ризик розвитку дисплазії або раку товстої кишки (наприклад, пацієнти з тривалим виразковим колітом або первинним склерозуючим холангітом) або які мають в анамнезі дисплазію або рак товстої кишки, повинні бути обстежені на цю дисплазію при регулярні проміжки перед початком терапії та протягом хвороби. Ця оцінка повинна включати колоноскопію та біопсію відповідно до місцевих рекомендацій. У пацієнтів з вперше виявленою дисплазією, які отримують лікування препаратом Симпоні, слід ретельно продумати співвідношення користь / ризик для окремого пацієнта та чи слід продовжувати терапію.
У дослідницькому клінічному дослідженні, що оцінювало застосування препарату Сімпоні у пацієнтів з тяжкою персистуючою астмою, у пацієнтів, які отримували Симпоні, було зареєстровано більше випадків злоякісних пухлин, ніж у пацієнтів контрольної групи (див. Розділ 4.8). Значимість цих даних невідома.
У дослідницькому клінічному дослідженні, в якому оцінювалося застосування іншого препарату проти ФНП, інфліксимабу, у пацієнтів з помірним та тяжким перебігом хронічної обструктивної хвороби легенів (ХОЗЛ) було зареєстровано більше випадків злоякісних пухлин, переважно вражаючих легені або голову та шию, у інфліксимабі. -ліковані пацієнти порівняно з пацієнтами контрольної групи. Усі пацієнти тривалий час були завзятими курцями. Тому слід бути обережним при оцінці застосування антагоніста ФНП у пацієнтів із ХОЗЛ, а також у пацієнтів з більшим ризиком злоякісних пухлин як завзяті курці.
Пухлини шкіри
Повідомлялося про меланому та клітинний рак Меркеля у пацієнтів, які отримували інгібітори ФНП, включаючи Симпоні (див. Розділ 4.8). Рекомендується періодичний огляд шкіри, особливо пацієнтам з факторами ризику раку шкіри.
Застійна серцева недостатність (ХСН)
Були повідомлення про погіршення застійної серцевої недостатності (ХСН) та нові випадки ХСН з антагоністами ФНП, включаючи Симпоні. Деякі випадки мали летальний результат. У клінічному дослідженні з іншим антагоністом ФНП спостерігалося погіршення застійної серцевої недостатності та збільшення смертності через ХСН. Симпоні не вивчався у пацієнтів із ХСН. / II) Пацієнти повинні перебувати під ретельним наглядом і припинити лікування Симпоні у пацієнтів з новими або погіршеннями симптомів серцевої недостатності (див. Розділ 4.3).
Вплив на нервову систему
Застосування лікарських засобів, що блокують ФНП, включаючи Симпоні, було пов'язано з новими або загостреними випадками клінічних симптомів та / або рентгенологічних ознак демієлінізуючих розладів центральної нервової системи, включаючи розсіяний склероз та периферичні демієлінізуючі розлади. розлади, переваги та ризики лікування анти-ФНП слід ретельно розглянути перед початком терапії Симпоні.
У разі розвитку цих станів слід розглянути можливість припинення терапії Симпоні (див. Розділ 4.8).
Хірургічні втручання
Досвід щодо безпеки лікування Симпоні у пацієнтів, які перенесли операцію, включаючи ендопротезування, обмежений. При плануванні операції слід враховувати тривалий період напіввиведення. Пацієнта, який потребує операції під час лікування Симпоні, слід ретельно контролювати на предмет підвищеного ризику інфекцій та розглянути відповідні заходи.
Імуносупресія
Існує ймовірність того, що ліки проти TNF, включаючи Simponi, впливають на захист господаря від інфекцій та злоякісних пухлин, оскільки TNF опосередковує запалення та модулює клітинні імунні реакції.
Аутоімунні реакції
Відносний дефіцит TNF? спричинене анти-TNF-терапією, може призвести до початку аутоімунного процесу.Якщо у пацієнта після лікування Симпоні проявляються симптоми, що передбачають вовчакоподібний синдром, і позитивний на антитіла до дволанцюгової ДНК, лікування Симпоні слід припинити ( див. розділ 4.8).
Гематологічні реакції
Постмаркетингові випадки панцитопенії, лейкопенії, нейтропенії, апластичної анемії та тромбоцитопенії були зареєстровані у пацієнтів, які отримували препарати проти ФНП. Цитопенії, включаючи панцитопенію, у клінічних дослідженнях із препаратом Симпоні повідомлялися не часто. Всім пацієнтам слід порадити негайно звернутися за медичною допомогою, якщо у них з’являться сумісні ознаки або симптоми порушення крові (наприклад, стійка лихоманка, синці, кровотеча та блідість). Пацієнтам з підтвердженими значними гематологічними відхиленнями слід розглянути питання про припинення терапії Симпоні.
Одночасне застосування антагоністів ФНП та анакінри
Серйозні інфекції та нейтропенія мали місце у поєднанні клінічних випробувань анакінри та іншого інгібітора ФНП, етанерцепту, без додаткової клінічної користі. З огляду на характер побічних ефектів, що спостерігаються при цій комбінованій терапії, подібні токсичні реакції можуть виникати при комбінації анакінри та інших інгібіторів ФНП. Комбінація Симпоні та анакінри не рекомендується.
Одночасне застосування антагоністів ФНП та абатацепту
У клінічних дослідженнях комбіноване застосування антагоністів ФНП та абатасепту асоціювалося з підвищеним ризиком інфекцій, включаючи серйозні інфекції, порівняно з антагоністами ФНП, що застосовувалися окремо, без збільшення клінічної користі. Симпоні та абатасепт не рекомендуються.
Одночасне застосування з іншими біологічними методами лікування
Інформації про одночасне застосування Симпоні з іншими біологічними препаратами, що використовуються для лікування тих самих станів, що і Симпоні, недостатньо. Одночасне застосування Симпоні з цими біопрепаратами не рекомендується через можливість підвищеного ризику інфекції та інших потенційних лікарських взаємодій.
Заміна між біологічними DMARD
Слід бути обережним, а пацієнтів слід продовжувати контролювати при переході з одного біопрепарату на інший, оскільки перекриття біологічної активності може ще більше збільшити ризик побічних явищ, включаючи інфекцію.
Щеплення / інфекційні терапевтичні засоби
Пацієнти, які отримують Симпоні, можуть отримувати супутні щеплення, за винятком живих вакцин (див. Розділи 4.5 та 4.6). У пацієнтів, які отримують анти-TNF-терапію, є обмежені дані про відповідь на вакцинацію, за допомогою живих вакцин або про вторинну передачу інфекції при введенні живих вакцин. Використання живих вакцин може призвести до клінічних інфекцій, у тому числі до розповсюджених інфекцій .
Інше використання інфекційних терапевтичних засобів, таких як живі аттенуйовані бактерії (наприклад, внутрішньоміхурові інстиляції БЦЖ для лікування раку), може призвести до клінічних інфекцій, включаючи дисеміновані інфекції. Рекомендується не давати терапевтичні інфекційні агенти одночасно з Симпоні.
Алергічні реакції
У постмаркетинговому досвіді повідомлялося про тяжкі системні реакції гіперчутливості (включаючи анафілактичну реакцію) після введення Симпоні. Деякі з цих реакцій виникали після першого введення Симпоні. негайно припинити і розпочати відповідну терапію.
Чутливість до латексу
Ковпачок для голки на попередньо заповненій ручці або наповненому шприці виготовлений із сушеного натурального каучуку, що містить латекс, і може викликати алергічні реакції у людей, чутливих до латексу.
Особливі популяції
Літні люди (≥ 65 років)
У дослідженнях РА, AP, SA та CU фази III не спостерігалося загальних відмінностей у побічних явищах (АЕ), серйозних побічних явищах (ЕАГ) та серйозних інфекціях у пацієнтів віком від 65 років, які отримували терапію. молодшим пацієнтам. Однак при лікуванні людей похилого віку слід бути обережними, особливу увагу слід приділити виникненню інфекцій.
Порушення функції нирок та печінки
Специфічних досліджень із застосуванням Симпоні у пацієнтів з нирковою або печінковою недостатністю не проводилося. Симпоні слід з обережністю застосовувати пацієнтам з порушенням функції печінки (див. Розділ 4.2).
Педіатричне населення
Щеплення
По можливості, перед початком терапії Сімпоні рекомендується, щоб педіатричні пацієнти мали хорошу репутацію з усіма вакцинаціями відповідно до чинних вказівок щодо імунізації.
Допоміжні речовини
Симпоні містить сорбіт (Е420). Пацієнти з рідкісними спадковими проблемами непереносимості фруктози не повинні приймати Симпоні.
Можливість помилок лікування
Симпоні зареєстровано у концентраціях 50 мг та 100 мг для підшкірного введення. Важливо, щоб для введення правильної дози використовувалася правильна доза, зазначена у дозуванні (див. Розділ 4.2). Слід обережно поставити правильну дозу, щоб уникнути недоотримання або передозування пацієнтів.
04.5 Взаємодія з іншими лікарськими засобами та інші форми взаємодії
Досліджень взаємодії не проводилося.
Одночасне застосування з іншими біологічними методами лікування
Поєднання Симпоні з іншими біологічними засобами лікування, що застосовуються для лікування тих самих станів, що і Симпоні, включаючи анакінру та абатацепт, не рекомендується (див. Розділ 4.4).
Живі вакцини / інфекційні терапевтичні засоби
Живі вакцини не слід вводити одночасно з Симпоні (див. Розділи 4.4 та 4.6).
Інфекційні терапевтичні засоби не слід вводити одночасно з Симпоні (див. Розділ 4.4).
Метотрексат
Хоча одночасне застосування метотрексату (МТХ) призводить до збільшення мінімальних концентрацій симпоні у рівноважному стані у пацієнтів з РА, АП чи АС, дані не свідчать про необхідність коригування дози Сімпоні або МТХ (див. Розділ 5.2).
04.6 Вагітність та період лактації
Жінки дітородного віку
Жінки дітородного віку повинні використовувати адекватну контрацепцію для запобігання вагітності та продовжувати її застосування щонайменше 6 місяців після останнього застосування голімумабу.
Вагітність
Немає адекватних даних про застосування голімумабу у вагітних жінок. Через пригнічення ФНП застосування голімумабу під час вагітності може вплинути на нормальну імунну відповідь новонародженого. Дослідження на тваринах не вказують на прямий чи шкідливий вплив. Непрямий вплив на вагітність , ембріональний / внутрішньоутробний розвиток, пологи або постнатальний розвиток (див. розділ 5.3) .Застосування голімумабу не рекомендується вагітним жінкам; Голімумаб слід призначати вагітним жінкам лише у разі крайньої необхідності.
Голімумаб проникає через плаценту. Після лікування моноклональними антитілами, що інгібують ФНП, під час вагітності антитіло було виявлено протягом 6 місяців у сироватці крові немовлят, народжених від жінок, які отримували лікування. Отже, ці немовлята можуть мати підвищений ризик зараження.
Введення живих вакцин у немовлят, які зазнали впливу внутрішньоутробно голімумаб не рекомендується протягом 6 місяців після останньої ін’єкції голімумабу матері під час вагітності (див. розділи 4.4 та 4.5).
Грудне вигодовування
Невідомо, чи виділяється голімумаб у жіноче молоко або системно всмоктується після прийому. Було показано, що голімумаб проникає у молоко мавп, а оскільки імуноглобуліни людини виділяються з молоком, жінки не повинні годувати грудьми протягом лікування та принаймні 6 місяців після лікування голімумабом.
Родючість
Дослідження фертильності з голімумабом не проводилися на тваринах. Дослідження фертильності на мишах з використанням подібного антитіла, яке вибірково пригнічує функціональну активність мишачого ФНП, не показало відповідного впливу на фертильність (див. Розділ 5.3).
04.7 Вплив на здатність керувати автомобілем та працювати з механізмами
Симпоні може незначно погіршити здатність керувати автомобілем та працювати з механізмами. Після застосування Симпоні може виникнути запаморочення (див. Розділ 4.8).
04.8 Побічні ефекти
Короткий опис профілю безпеки
У контрольний період основних досліджень RA, AP, SA, Axial SpA nr та CU інфекція верхніх дихальних шляхів була найпоширенішою побічною лікарською реакцією (НПР), про яку повідомляли у 12,6% пацієнтів, які отримували голімумаб. Порівняно з 11,0% контролювати пацієнтів. Найбільш серйозні побічні реакції, повідомлені про голімумаб, включають важкі інфекції (включаючи сепсис, пневмонію, туберкульоз, інвазивні грибкові інфекції та опортуністичні інфекції), демієлінізуючі захворювання, реактивацію ВГВ, ХСН, аутоімунні процеси (вовчакоподібний синдром), гематологічні реакції, важку системну гіперчутливість ( включаючи анафілактичну реакцію), васкуліт, лімфому та лейкемію (див. розділ 4.4).
Таблиця зі списком побічних реакцій
Побічні реакції, що спостерігалися у клінічних випробуваннях та повідомлялися після введення у світовий маркетинг голімумабу, наведені в таблиці 1. У системі системних органів побічні реакції на лікарські засоби перераховані за частотою з використанням таких категорій: дуже поширені (≥ 1/10); поширені (≥ 1/100,
Таблиця 1
Таблиця із переліком НДР
*: Спостерігається з іншими блокаторами ФНП.
У цьому розділі середня тривалість спостереження (приблизно 4 роки) зазвичай представлена для всіх застосувань голімумабу. Якщо застосування голімумабу описується дозою, середня тривалість спостереження змінюється (приблизно 2 роки для дози 50 мг, приблизно 3 роки для дози 100 мг), оскільки пацієнти можуть переходити між прийомами.
Опис окремих побічних реакцій на лікарські засоби
Інфекції
У контрольний період основних досліджень інфекція верхніх дихальних шляхів була найпоширенішою побічною реакцією, зареєстрованою у 12,6% пацієнтів, які отримували голімумаб (частота на 100 суб’єктів-років: 60,8; 95% ДІ: 55,0, 67,1) порівняно з 11,0% контрольних пацієнтів (частота на 100 пацієнтів на рік: 54,5; 95% ДІ: 46,1, 64,0). На контрольованих та неконтрольованих етапах досліджень із середнім періодом спостереження приблизно 4 роки частота захворювань на 100 суб’єкт-років інфекцій верхніх дихальних шляхів становила 34,9 подій; 95% ДІ: 33,8, 36,0 у пацієнтів, які отримували голімумаб.
У контрольний період основних досліджень інфекції спостерігалися у 23,0% пацієнтів, які отримували голімумаб (частота на 100 суб’єктів-років: 132,0; 95% ДІ: 123,3, 141,1) порівняно з 20,2% контрольних пацієнтів (частота на 100 предметних років: 122,3; 95% ДІ: 109,5, 136,2). На контрольованих та неконтрольованих фазах досліджень із середнім періодом спостереження приблизно 4 роки частота випадків на 100 суб’єктів-років інфекцій становила 81,1 подій; 95% ДІ: 79,5, 82,8 у пацієнтів, які отримували голімумаб.
У контрольний період досліджень RA, AP, SA та Axial SpA nr серйозні інфекції спостерігалися у 1,2% пацієнтів, які отримували голімумаб, та у 1,2% контрольних пацієнтів. Частота серйозних інфекцій на 100 досліджуваних років під час спостереження у контрольному періоді досліджень РА, АП, СА та nr-осьового SpA становила 7,3; 95% ДІ: 4,6, 11, 1 для групи 100 мг голімумабу, 2,9; 95% ДІ: 1,2, 6,0 для групи 50 мг голімумабу та 3,6; 95% ДІ: 1, 5, 7,0 для групи плацебо. У контрольний період індукційних досліджень ГК голімумабу серйозні інфекції спостерігалися у 0,8 % пацієнтів, які отримували голімумаб, проти 1,5% контрольних пацієнтів. Серйозні інфекції, які спостерігалися у пацієнтів, які отримували голімумаб, включали туберкульоз, бактеріальні інфекції, включаючи сепсис та пневмонію, інвазивні грибкові інфекції та інші умовно-патогенні інфекції. Деякі з цих інфекцій мали летальний результат. У контрольованих та неконтрольованих частинах основних досліджень із середнім періодом спостереження до 3 років спостерігалася вища частота серйозних інфекцій, включаючи опортуністичні інфекції та туберкульоз, у пацієнтів, які отримували голімумаб у дозі 100 мг, у порівнянні з пацієнтами, які лікувалися голімумабом. 50 мг. Частота всіх тяжких інфекцій на 100 предметних років становила 4,1; 95% ДІ: 3,6, 4,5 для пацієнтів, які отримували голімумаб у дозі 100 мг та 2,5; 95% ДІ: 2,0, 3,1 для пацієнтів, які отримували 50 мг голімумабу.
Злоякісні новоутворення
Лімфома
Частота лімфом у пацієнтів, які отримували голімумаб, під час ключових досліджень була вищою, ніж очікувалося, у загальній популяції. У контрольованих та неконтрольованих частинах цих досліджень із середнім періодом спостереження до 3 років спостерігалася вища частота лімфом. у пацієнтів, які отримували голімумаб у дозі 100 мг порівняно з пацієнтами, які отримували голімумаб у дозі 50 мг. Лімфому діагностували у 11 пацієнтів (1 у групах лікування голімумабом у дозі 50 мг та 10 у групах лікування голімумабом у 100 мг) з частотою (95% ДІ) на 100 предметних років спостереження за подіями 0,03 та 0,13 для голімумабу 50 мг та голімумабу 100 мг відповідно та 0,00 подій для плацебо. Більшість лімфом траплялося у дослідженні GO-AFTER, в якому брали участь пацієнти, які раніше отримували анти-ФНП препарати та мали більш тривалу та рефрактерну тривалість захворювання (див. Розділ 4.4).
Злоякісні новоутворення, крім лімфоми
У контрольні періоди основних досліджень та протягом приблизно 4 років спостереження частота злоякісних пухлин, відмінних від лімфоми (виключаючи немеланомний рак шкіри), була подібною між голімумабом та контрольною групою. Приблизно 4 роки спостереження, частота нелімфомних злоякісних пухлин (за винятком немеланомного раку шкіри) була подібною до такої у загальній популяції.
У контрольовані та неконтрольовані періоди основних досліджень із середнім періодом спостереження до 3 років немеланомний рак шкіри був діагностований у 5 суб’єктів, які отримували плацебо, 10-з 50 мг голімумабу та 31-з 100 мг голімумабу з частота (95% ДІ) на 100 предметних років спостереження становить 0,36 для комбінованого голімумабу та 0,87 для плацебо.
У контрольовані та неконтрольовані періоди основних досліджень із середнім періодом спостереження до 3 років, злоякісні пухлини на додаток до меланоми, немеланомний рак шкіри та лімфома були діагностовані у 5 пацієнтів, які отримували плацебо, у 21, які отримували голімумаб 50 мг та у 34 пацієнтів, які отримували голімумаб у дозі 100 мг з частотою (95% ДІ) на 100 періодів спостереження, що становили 0,48 для комбінованого голімумабу та 0,87 для плацебо (див. розділ 4.4).
Випадки, зареєстровані в клінічних випробуваннях на наявність астми
У дослідницькому клінічному дослідженні пацієнти з тяжкою персистуючою астмою отримували навантажувальну дозу голімумабу (150% призначеної дози лікування) підшкірно на 0 -му тижні, потім - 200 мг голімумабу, 100 мг голімумабу або 50 мг голімумабу кожні 4 тижні підшкірно. тиждень 52. Повідомлялося про вісім злоякісних пухлин у групі комбінованого лікування голімумабом (n = 230) і жодного у групі плацебо (n = 79). Лімфома була зареєстрована у 1 пацієнта, немеланомний рак шкіри у 2 пацієнтів та інші злоякісні утворення у 5 пацієнтів. Специфічного об’єднання будь -якого типу злоякісного новоутворення не було.
На етапі дослідження, контрольованому плацебо, частота (95% ДІ) усіх злоякісних пухлин на 100 спостережень за пацієнтами за період спостереження становила 3,19 у групі лікування голімумабом. -збільшення у пацієнтів, які отримували голімумаб, становило 0,40 для лімфоми, 0,79 для немеланомного раку шкіри та 1,99 для інших злоякісних пухлин. Для пацієнтів, які отримували плацебо, частота (95% ДІ) цих злоякісних пухлин на 100 пацієнтів / рік спостереження становила 0,00. Значимість цих даних невідома.
Неврологічні події
У контрольовані та неконтрольовані періоди основних досліджень із середнім періодом спостереження до 3 років спостерігалася вища частота демієлінізації у пацієнтів, які отримували голімумаб у дозі 100 мг, порівняно з пацієнтами, які отримували голімумаб у дозі 50 мг (див. Розділ 4.4). .
Підвищення печінкових ферментів
У контрольні періоди основних досліджень РА та АР незначне підвищення рівня АЛТ (> 1 та 1 та
У контрольний період основних досліджень РА та АС підвищення АЛТ ≥ 5 разів вище норми верхнього рівня було рідкістю і спостерігалося у більшої кількості пацієнтів, які отримували голімумаб (від 0,4%до 0,9%) порівняно з контрольними пацієнтами (0,0%). Ця тенденція не спостерігалася у популяції AP. У контрольовані та неконтрольовані періоди основних досліджень РА, АП та СА із середнім періодом спостереження 5 років частота підвищення рівня АЛТ ≥ 5 разів вище ВГН була подібною як для голімумабу, так і для контрольних пацієнтів. Загалом, ці підвищення були безсимптомними, і аномалії зменшувалися або усувалися при продовженні або припиненні прийому голімумабу або модифікації супутніх препаратів. У контрольованих і неконтрольованих періодах дослідження Axial SpA не повідомлялося про жодні випадки (до 1 року) основних досліджень індукції ХО з голімумабом, підвищення рівнів АЛТ ≥ 5 х ГМН спостерігалося з однаковою частотою у пацієнтів, які отримували голімумаб та плацебо (від 0,3% до 1,0%).У контрольовані та неконтрольовані періоди основних досліджень UC із середнім періодом спостереження приблизно за 2 роки частка пацієнтів з підвищенням рівня АЛТ ≥ 5 x ГМН становила 0,8% у пацієнтів, які отримували голімумаб під час проведення дослідження UC.
У ключових дослідженнях RA, AP, SA та Axial SpA у пацієнта у дослідженні RA з уже наявними аномаліями печінки та препаратами, що вражають фактор, які отримували лікування голімумабом, розвинувся летальний неінфекційний гепатит з жовтяницею. Не можна виключити роль голімумабу як сприяючого чи погіршуючого чинника.
Реакції на місці ін’єкції
У контрольні періоди основних досліджень реакції в місці ін’єкції спостерігалися у 5,4% пацієнтів, які отримували голімумаб, порівняно з 2,0% контрольних пацієнтів. Наявність антитіл до голімумабу може збільшити ризик реакцій у місці ін’єкції. Більшість реакцій у місці ін’єкції були легкими та помірними, а найбільш частими проявами - еритема в місці ін’єкції. Реакції на місці ін’єкції зазвичай не вимагають припинення лікування препаратом.
У контрольованих дослідженнях фази IIb та / або III при РА, АП, СА, осьовій криві SpA, важкій персистуючій астмі та у дослідженнях UC фази II / III у жодного пацієнта, який лікувався голімумабом, не виникли анафілактичні реакції.
Аутоімунні антитіла
У контрольовані та неконтрольовані періоди основних досліджень з 1 роком спостереження 3,5% пацієнтів, які отримували голімумаб, та 2,3% контрольних пацієнтів мали нещодавно позитивну АНА (титрування 1: 160 або вище). Частота антитіл до dsDNA через 1 рік спостереження у пацієнтів з негативною до dsDNA на початку становила 1,1%.
Педіатричне населення
Поліартикулярний ювенільний ідіопатичний артрит
Безпеку голімумабу вивчали у фазі III дослідження 173 пацієнтів з pJIA у віці від 2 до 17 років. Середній період спостереження склав приблизно два роки. У цьому дослідженні тип та частота повідомлень про побічні ефекти були загалом подібними до тих, що спостерігалися у дослідженнях у дорослих з РА.
Повідомлення про підозрювані побічні реакції
Повідомлення про підозрювані побічні реакції, що виникають після реєстрації ліків, є важливими, оскільки вони дозволяють постійно контролювати співвідношення користь / ризик застосування лікарського засобу. http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Передозування
У клінічному дослідженні вводили разові дози до 10 мг / кг внутрішньовенно без будь-якої токсичності, що обмежує дозу. У разі передозування рекомендується спостереження за пацієнтом на предмет виявлення ознак та симптомів побічних явищ та негайне призначення відповідного симптоматичного лікування.
05.0 ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ
05.1 Фармакодинамічні властивості
Фармакотерапевтична група: імунодепресанти, інгібітори фактора некрозу пухлини альфа (TNF-?), Код АТС: L04AB06
Механізм дії
Голімумаб-це моноклональне антитіло людини, яке утворює стабільні комплекси з високою спорідненістю як до розчинної, так і до біоактивної трансмембранної форми TNF-? людини, запобігаючи зв'язуванню TNF-? до його рецепторів.
Фармакодинамічні ефекти
Було показано, що зв'язування голімумабу з TNF людини інгібує експресію молекулами адгезії клітинної поверхні, індукованої TNF-α, молекулами адгезії Е, молекули адгезії судинних клітин типу 1 (VCAM) та внутрішньоклітинною молекулою адгезії типу 1 (ICAM) клітинами ендотелію людини. В пробірці, Індуковану TNF секрецію інтерлейкінами (IL) -6, IL-8 та гранулоцитарними та макрофаговими колонієстимулюючими факторами (GM-CSF) клітинами ендотелію людини також інгібували голімумабом.
Порівняно з групами плацебо спостерігалося поліпшення рівня С-реактивного білка (СРБ), і лікування Симпоні призвело до значного зниження рівня сироватки крові від вихідного рівня IL-6, ICAM-1, матричної металопротеїнази.3 (ММР) та ендотелію судин. фактор росту (VEGF), порівняно з контрольною обробкою. Крім того, у пацієнтів з РА та АС рівень TNF-? зменшився, а рівень ІЛ-8 знизився у пацієнтів з АП. Ці зміни були помічені під час першого оцінювання (4 тиждень) після першого введення препарату Симпоні і, як правило, тривали протягом 24 тижня.
Клінічна ефективність
Ревматоїдний артрит
Ефективність препарату Симпоні була продемонстрована у трьох багатоцентрових, рандомізованих, подвійних сліпих, плацебо-контрольованих клінічних випробуваннях, проведених у більш ніж 1500 пацієнтів у віці ≥ 18 років з помірною та важкою активною РА, діагностованою за критеріями Американського коледжу ревматології (ACR) принаймні за 3 місяці до скринінгу. Пацієнти повинні були мати щонайменше 4 набряклі та 4 болючі суглоби. Симпоні або плацебо вводили підшкірно кожні 4 тижні.
GO-FORWARD оцінив 444 пацієнта з активним РА, незважаючи на стабільну дозу МТХ щонайменше 15 мг / тиждень, які раніше не отримували жодних препаратів проти ФНП. Пацієнти були рандомізовані на плацебо + МТХ, Сімпоні 50 мг + МТХ, Сімпоні 100 мг + МТХ або Симпоні 100 мг + плацебо. Пацієнтам, які отримували плацебо + МТКС, після 24 тижня призначили Симпоні 50 мг + МТХ. На 52 тижні пацієнти пройшли відкрите довгострокове розширене дослідження.
GO-AFTER оцінив 445 пацієнтів, які раніше лікувалися одним або кількома препаратами проти ФНО, адалімумабом, етанерцептом або інфліксимабом. Пацієнти були рандомізовані до плацебо, Симпоні 50 мг або Симпоні 100 мг. Під час дослідження пацієнти змогли продовжити супутню терапію DMARD МТХ, сульфасалазином (SSZ) та / або гідроксихлорохіном (HCQ). Причинами припинення попередньої терапії проти ФНП були недостатня ефективність (58%), непереносимість (13%) та / або інші причини, крім безпеки чи ефективності (29%, переважно з фінансових причин).
GO-BEFORE оцінив 637 пацієнтів з активним ревматоїдним артритом, не отримував МТХ та які раніше не отримували ліки проти ФНО. Пацієнти були рандомізовані для отримання плацебо + МТХ, Симпоні 50 мг + МТХ, Сімпоні 100 мг + МТХ або Симпоні 100 мг + плацебо. На 52 тижні пацієнти пройшли відкрите довгострокове розширене дослідження, в якому пацієнтів, які отримували плацебо + МТХ і мали принаймні 1 болючий або набряклий суглоб, перевели на лікування Симпоні 50 мг + МТХ.
У GO-FORWARD (спільними) первинними кінцевими точками була частка пацієнтів, які досягли відповіді ACR 20 на 14-му тижні, та покращення опитувальника оцінки стану здоров’я (HAQ) на 24-му тижні від базового рівня. Це частка пацієнтів, які досягли відповіді ACR 20 на 14-му тижні. У GO-BEFORE кінцевими кінцевими точками первинної оцінки були частка пацієнтів, які досягли відповіді ACR 50 на 24-му тижні, і зміна від вихідного рівня у модифікованому балі Шарпа за ван дер Хейде (vdH-S) на 52-му тижні. Окрім первинних кінцевих точок, були проведені додаткові оцінки впливу лікування Сімпоні на ознаки та симптоми артриту, рентгенологічну відповідь, фізичні функції та якість життя, пов’язану зі станом.
Загалом, не спостерігалося клінічно значущих відмінностей в оцінках ефективності між Симпоні 50 мг та 100 мг у поєднанні з режимами дозування МТХ до 104 тижня у GO-FORWARD та GO-BEFORE та до 24 тижня у GO-AFTER. у кожному з досліджень РА відповідно до плану дослідження пацієнти, які перебували у довгостроковому періоді, могли переходити між дозами Симпоні 50 мг та 100 мг на розсуд лікаря-дослідника.
Ознаки та симптоми
Результати ключових критеріїв ACR для дози 50 мг Симпоні на 14, 24 та 52 тижнях для GO-FORWARD, GO-AFTER та GO-BORE наведені в таблиці 2 і описані нижче. Відповіді були помічені під час першого оцінювання (4 тиждень) після першого введення препарату Симпоні.
У дослідженні GO-FORWARD із 89 пацієнтів, рандомізованих до препарату Симпоні 50 мг + МТХ, 48 все ще перебували на лікуванні на 104. тижні. Серед них 40, 33 та 24 пацієнти мали відповідь ACR 20/50/70 на 104 тижні, Відповідно. Серед пацієнтів, які залишалися в дослідженні та лікувалися Симпоні, подібні показники відповіді ACR 20/50/70 спостерігалися з 104 по 256 тиждень.
У дослідженні GO-AFTER відсоток пацієнтів, які досягли відповіді ACR 20, був вищим серед пацієнтів, які отримували Симпоні, порівняно з пацієнтами, які отримували плацебо, незалежно від повідомленої причини припинення однієї або декількох протизапальних терапій. -TNF.
Таблиця 2
Ключові результати ефективності контрольованих частин досліджень GO-FORWARD, GO-AFTER та GO-BEFORE
a n відповідає рандомізованим пацієнтам; фактична кількість пацієнтів, які можна оцінити для кожної кінцевої точки, може змінюватися залежно від часу.
* p ≤ 0,001
НС: Не застосовується
У дослідженні GO-BEFORE первинний аналіз у пацієнтів з помірним та важким ревматоїдним артритом (комбіновані групи Симпоні 50 та 100 мг + МТХ порівняно з одним МТКС для АКР 50) не був статистично значущим на 24-му тижні (р = 0,053 На 52-му тижні серед населення, частка пацієнтів у групі Симпоні 50 мг + МТХ, які досягли відповіді на АКР, була загалом вищою, але не суттєво відрізнялася у порівнянні з однією лише МТХ (див. Таблицю 2). Додаткові аналізи підгруп, репрезентативні для зазначеної популяції пацієнтів з , активний і прогресуючий РА. Загалом кращий ефект був продемонстрований при застосуванні Симпоні 50 мг + МТХ порівняно з одним МТХ у зазначеній популяції порівняно із загальною популяцією.
У дослідженнях GO-FORWARD та GO-AFTER на кожній заздалегідь визначеній стадії, на 14-му та 24-му тижнях (р ≤ 0,001), на кожній заздалегідь визначеній стадії спостерігалися статистично та клінічно значимі відповіді за шкалою активності захворювання (DAS28). Серед пацієнтів, які залишалися на лікуванні Симпоні, рандомізованими на початку дослідження, відповіді DAS28 зберігалися протягом 104. тижня. Серед пацієнтів, які залишалися на етапі дослідження та лікувалися Симпоні, відповіді DAS28 були подібними з 104 по 256 тиждень.
У дослідженні GO-BEFORE була оцінена основна клінічна відповідь, визначена як підтримка відповіді ACR 70 протягом безперервного 6-місячного періоду. На 52 -му тижні 15% пацієнтів у групі Симпоні 50 мг + МТКС досягли вищої клінічної відповіді порівняно з 7% пацієнтів у групі плацебо + МТХ (р = 0,018). З 159 суб’єктів, рандомізованих до препарату Симпоні 50 мг + МТКС, 96 все ще перебували на лікуванні на 104. тижні. Серед цих 85, 66 та 53 пацієнти мали відповідь ACR 20/50/70 на 104 тижні відповідно. Рівень відповіді ACR 20/50/70 спостерігався з 104 по 256 тиждень.
Рентгенологічна реакція:
У дослідженні GO-BEFORE для оцінки були використані зміни показників vdH-S, порівняно з вихідним показником, складової оцінки структурних пошкоджень, яка рентгенологічно вимірює кількість та розміри суглобових ерозій та ступінь зменшення суглобового простору в руках / зап’ястках та стопах. ступінь пошкодження конструкції. Ключові результати для Simponi у дозі 50 мг на 52 тижні представлені в таблиці 3.
Кількість пацієнтів без нової ерозії або зміни загального показника vdH-S від вихідного рівня ≤ 0 була значно вищою у групі Сімпоні, ніж у контрольній групі (р = 0,003). Рентгенологічні ефекти, які спостерігалися на 52 -му тижні, зберігалися до 104. тижня. Серед пацієнтів, які залишалися у дослідженні та лікувалися Симпоні, рентгенологічні ефекти були подібними з 104 по 256 тиждень.
Таблиця 3
Середнє значення (SD) рентгенографічних змін від базового рівня до 52-го тижня в загальній оцінці vdH-S у досліджуваній популяції GO-BEFORE
a n відповідає рандомізованим пацієнтам
* р = 0,015
** р = 0,044
Фізичні функції та якість життя, пов'язана зі здоров'ям
Фізичні функції та інвалідність оцінювались як окремі кінцеві точки у дослідженнях GO-FORWARD та GO-AFTER, використовуючи індекс інвалідності HAQ DI. У цих дослідженнях на 24 тижні Сімпоні показав клінічно та статистично значуще поліпшення показників HAQ DI порівняно з контрольною групою порівняно з контрольною групою. Серед пацієнтів, які залишалися на лікуванні Simponi, рандомізованим на початку дослідження, поліпшення показників HAQ DI зберігалося протягом 104 тижня Серед пацієнтів, які залишалися у дослідженні та лікувалися Симпоні, поліпшення показників HAQ DI було подібним з 104 по 256 тиждень.
Дослідження GO-FORWARD показало клінічно та статистично значуще поліпшення якості життя, пов'язане зі здоров'ям, виміряне за показником фізичної складової SF-36 у пацієнтів, які отримували Симпоні проти плацебо на 24 тижні. Серед пацієнтів, які продовжували лікування Симпоні, рандомізовано на початку дослідження поліпшення рівня SF-36 зберігалося протягом 104. тижня. Серед пацієнтів, які залишалися у дослідженні та лікувалися препаратом Симпоні, поліпшення фізичної складової SF-36 було подібним із 104-го тижня до 256. тижня. -ДОСЛІДЖЕННЯ ВПЕРЕД та GO-AFTER, за шкалою функціональної оцінки терапії хронічної хвороби-втома (FACIT-F), спостерігалося статистично значуще поліпшення втоми.
Псоріатичний артрит
Ефективність та безпеку препарату Симпоні оцінювали у багатоцентровому, рандомізованому, подвійному сліпому, плацебо-контрольованому клінічному дослідженні (GO-REVEAL), проведеному у 405 дорослих пацієнтів з активною ПА (≥ 3 набряклі суглоби та ≥ 3 суглоби болючі), незважаючи на терапію з нестероїдними протизапальними препаратами (НПЗЗ) або ДМАРД. Пацієнти в цьому дослідженні мали діагноз АП протягом щонайменше 6 місяців і принаймні легкий псоріаз. вузлики (43%), асиметричний периферичний артрит (30%), дистальний міжфаланговий суглобовий артрит (DIP) (15%), спондиліт з периферичним артритом (11%) та калічуючий артрит (1%). без попереднього лікування анти-TNF Симпоні або плацебо вводили підшкірно кожні 4 тижні. вводять 100 мг. Пацієнтам, які отримували плацебо, після 24 тижня призначили Симпоні по 50 мг. На 52 тижні пацієнти пройшли тривале відкрите відкрите дослідження.
Приблизно 48% пацієнтів продовжували приймати стабільні дози метотрексату (≤ 25 мг / тиждень). Допоміжними кінцевими точками були частка пацієнтів, які досягли відповіді ACR 20 на 14-му тижні, та зміна від вихідного рівня у зміненому загальному балі AP vdH-S на 24 тижні.
Загалом, клінічно значущих відмінностей у показниках ефективності між схемами дозування Симпоні 50 мг та 100 мг до 10-го тижня не спостерігалося. мг дози на розсуд лікаря -дослідника.
Ознаки та симптоми
Основні результати для дози 50 мг на 14 та 24 тижнях наведені в таблиці 4 і описані нижче.
Таблиця 4
Ключові результати ефективності дослідження GO-REVEAL
* стор
a n відповідає рандомізованим пацієнтам; фактична кількість пацієнтів, які можна оцінити для кожної кінцевої точки, може змінюватися залежно від часу
b Індекс площі та тяжкості псоріазу
c Виходячи з підгрупи пацієнтів із залученням площі поверхні тіла (BSA) ≥ 3%на початковому етапі, 79 пацієнтів (69,9%) у групі лікування плацебо та 109 (74,3%) у препараті Симпоні 50 мг.
Відповіді були помічені під час першого оцінювання (4 тиждень) після першого введення препарату Сімпоні. Подібні відповіді ACR 20 спостерігалися на 14 тижні у пацієнтів з поліартикулярним артритом за відсутності ревматоїдних вузликів та підтипів АП, асиметричного периферичного артриту. Кількість пацієнтів з іншими підтипами ПА була занадто мала, щоб дозволити достовірну оцінку.Відповіді, які спостерігалися у групах лікування Симпоні, були подібними у пацієнтів, які отримували супутній МТХ чи ні. З 146 пацієнтів, рандомізованих до 50 мг Симпоні, 70 все ще перебували на лікуванні на 104. тижні. Серед цих 70 пацієнтів 64, 46 та 31 пацієнт отримали відповідь ACR 20/50/70 відповідно. Серед пацієнтів, які залишалися в дослідженні та лікувалися Симпоні, подібні показники відповіді ACR 20/50/70 спостерігалися з 104 по 256 тиждень.
Статистично значущі відповіді також спостерігалися у DAS28 на 14 та 24 тижнях (стор
На 24 тижні покращення параметрів периферичної активності, характерних для псоріатичного артриту (наприклад, кількість набряклих суглобів, кількість ніжних суглобів, дактиліт та ентезит), спостерігалося у пацієнтів, які отримували Симпоні. Лікування препаратом Сімпоні призвело до значного поліпшення фізичних функцій за оцінкою HAQ DI та суттєвого поліпшення якості життя, пов'язаної зі здоров'ям, на основі підсумкових оцінок фізичних та психічних компонентів SF-36. на початку дослідження відповіді DAS28 та HAQ DI зберігалися протягом 104. тижня. Серед пацієнтів, які залишалися у дослідженні та лікувалися Симпоні, відповіді DAS28 та HAQ DI були подібними. від 104 тижня до 256.
Рентгенологічна реакція:
Структурні пошкодження кистей і стоп рентгенологічно оцінювали за зміною показника vdH-S від вихідного рівня, модифікованого для АП з додаванням дистальних міжфалангових суглобів (DIP) кисті.
Лікування Симпоні у дозі 50 мг зменшує швидкість прогресування периферичних пошкоджень суглобів порівняно з лікуванням плацебо на 24 тижні, що вимірюється як зміна від вихідного рівня у зміненому загальному показнику vdH -S (середній бал ± SD становив 0,27 ± 1, 3 у групі плацебо порівняно з - 0,16 ± 1,3 у групі Сімпоні; p = 0,011). З 146 пацієнтів, які були рандомізовані для прийому 50 мг Симпоні, дані рентгенографії на 52 тижні були доступні для 126 пацієнтів, з яких 77% не прогресували від вихідного рівня. На 104-му тижні рентгенологічні дані були доступні для 114 пацієнтів, а 77% не прогресували від вихідного рівня. Серед пацієнтів, які залишалися в дослідженні та лікувалися Симпоні, подібні частки пацієнтів не прогресували від вихідного рівня з 104 по 256 тиждень.
Осьовий спондилоартроз
Хвороба Марі-Штрюмпеля
Ефективність та безпеку препарату Симпоні оцінювали у багатоцентровому, подвійному сліпому, рандомізованому, плацебо-контрольованому клінічному дослідженні (GO-RAISE), проведеному у 356 дорослих пацієнтів з активним анкілозуючим спондилоартритом (визначеним як патологічна активність анкілозуючого спондиліту за Індексом Бана) (BASDAI ) ≥ 4 і VAS для загального болю в спині ≥ 4 за шкалою від 0 до 10 см). Пацієнти, які брали участь у цьому дослідженні, мали захворювання в активній фазі, незважаючи на поточну або попередню терапію НПЗЗ або ДМАРД, і раніше вони не отримували жодних препаратів проти ФНП. Симпоні або плацебо вводили підшкірно кожні 4 тижні. Пацієнти були рандомізовані до групи плацебо, Симпоні 50 мг або Симпоні 100 мг і змогли продовжити супутню терапію DMARD (MTX, SSZ та / або HCQ). Первинною кінцевою точкою був відсоток пацієнтів з відповіддю групи дослідження оцінки анкилозуючого спондиліту (ASAS 20) на 14-му тижні. Дані про ефективність, контрольовані плацебо, збиралися та аналізувалися протягом 24-го тижня.
Ключові результати для дози 50 мг наведені в таблиці 5 і описані нижче. Загалом, не спостерігалося клінічно значущих відмінностей у показниках ефективності між режимами дозування Симпоні 50 мг та 100 мг до 24 тижня. дози на розсуд лікаря -дослідника.
Таблиця 5
Ключові результати ефективності дослідження GO-RAISE
* p ≤ 0,001 для всіх порівнянь
a n відповідає рандомізованим пацієнтам; фактична кількість пацієнтів, які можна оцінити для кожної кінцевої точки, може змінюватися залежно від часу
Серед пацієнтів, які залишалися у дослідженні та лікувалися Симпоні, частка пацієнтів з відповіддю на АСАС 20 та АСАС 40 була подібною з 24 по 256 тиждень.
Статистично значущі відповіді також спостерігалися у BASDAI 50, 70 та 90 (p ≤ 0,017) на 14 та 24 тижнях. Покращення показників активності ключових захворювань було виявлено під час першої оцінки (тиждень 4) після першого введення Симпоні, яка зберігалася протягом тижня 24. Серед пацієнтів, які залишалися у дослідженні та лікувалися препаратом Симпоні, подібні темпи зміни у порівнянні з вихідним показником спостерігались у BASDAI з 24 по 25 тиждень. Постійна ефективність спостерігалася у пацієнтів при незалежно від застосування ДМАРД (МТХ, сульфасалазину та / або гідроксихлорохін), наявність антигену HLA-B27 або вихідні рівні СРБ на основі оцінки відповідей ASAS 20 на 14 тижні.
Лікування симпоні призвело до значних поліпшень фізичної функції, що оцінювалося за змінами функціонального індексу анкилозуючого спондиліту Ванни (BASFI) на вихідному рівні на 14 та 24 тижнях. покращилося на 14 і 24 тижнях. Серед пацієнтів, які залишалися в дослідженні та лікувалися Симпоні, поліпшення фізичної функції та якості життя, пов'язаної зі здоров'ям, були подібними з 24 по 256 тиждень.
Нерентгенографічний осьовий спондилоартроз
Безпеку та ефективність препарату Симпоні оцінювали у багатоцентровому, рандомізованому, подвійному сліпому, плацебо-контрольованому дослідженні (GO-AHEAD), проведеному у 197 дорослих пацієнтів з важким осьовим SpA nr в активній фазі (визначені як ті пацієнти, які відповідали класифікації ASAS критерії діагностики аксіального спондилоартрозу, але не відповідали зміненим критеріям Нью -Йорка для діагностики АС.) Пацієнти, які брали участь у цьому дослідженні, мали активне захворювання (визначене за BASDAI ≥ 4 та візуальною аналоговою шкалою (VAS) для загального болю в спині) ≥ 4, кожен за шкалою від 0 до 10 см), незважаючи на триваючу або попередню терапію НПЗЗ, і раніше вони не отримували жодного біологічного засобу, включаючи анти -ФНП. 16, поступили пацієнти відкритий період лікування, протягом якого всі отримували Симпоні по 50 мг підшкірно кожні 4 тижні до 48 тижня з оцінкою ефективності, проведеною протягом 52 тижня, і контролем безпеки протягом 60 тижня. Приблизно 93% пацієнтів, які отримували Симпоні на початку відкрите продовження (16 тиждень) залишалося на лікуванні до кінця дослідження (52 тиждень). Аналізи проводили як на всій популяції, що пройшла лікування (AT, N = 197), так і на популяції з об'єктивними ознаками запалення (OSI, N = 158, на що вказують високі рівні СРБ та / або "свідчення сакроілеїту на МРТ" Дані про ефективність, контрольовані плацебо, були зібрані та проаналізовані протягом 16-го тижня. Первинною кінцевою точкою була частка пацієнтів, які досягли відповіді ASAS 20 на 16-му тижні. Ключові результати наведені в таблиці 6 і описані нижче.
Таблиця 6
Ключові результати ефективності дослідження GO-AHEAD на 16 тижні
a n відповідає рандомізованим та лікуваним пацієнтам
b Показник активності хвороби Анкілозуючого спондиліту (С-реактивний білок) (АТ-плацебо, N = 90; AT-Сімпоні 50 мг, N = 88; OSI-плацебо, N = 71; OSI-Симпоні 50 мг, N = 71)
c n відповідає кількості пацієнтів з базовими даними та даними МРТ 16 тижня
d SPARCC (Дослідницький консорціум спондилоартриту Канади)
** р проти плацебо
* р проти плацебо
Статистично значущі поліпшення ознак та симптомів важкої активної фази nr осьового SpA було продемонстровано у пацієнтів, які отримували Симпоні 50 мг порівняно з плацебо на 16 тижні (Таблиця 6). Поліпшення було помічено під час першого оцінювання (4 тиждень) після першого введення препарату Симпоні. Показник МРТ SPARCC показав статистично значуще зменшення запалення в суглобі SI на 16 тижні у пацієнтів, які отримували Симпоні у дозі 50 мг порівняно з плацебо (Таблиця 6). Біль, оцінений за загальним болем у спині та нічними болями в спині та активністю захворювання, виміряною за ASDAS-C, також показав статистично значуще поліпшення від початкового рівня до 16 тижня у пацієнтів, які отримували Симпоні 50 мг порівняно з плацебо (p
Статистично значуще поліпшення рухливості хребта за оцінкою BASMI (Індекс метрології анкілозуючого спондиліту ванни) та фізичної функції за оцінкою BASFI було продемонстровано у пацієнтів, які отримували Симпоні 50 мг порівняно з пацієнтами, які отримували плацебо (p
Для всіх кінцевих точок, описаних вище, статистично значущі результати також були продемонстровані в популяції OSI на 16 тижні.
Як у популяції AT, так і в OSI поліпшення ознак та симптомів, рухливості хребта, фізичних функцій, якості життя та продуктивності, що спостерігалися на 16 тижні у пацієнтів, які отримували 50 мг Simponi, зберігалося у тих пацієнтів, які залишалися у дослідженні. На 52 тижні.
Виразковий коліт
Ефективність препарату Симпоні оцінювали у двох рандомізованих подвійних сліпих плацебо-контрольованих клінічних дослідженнях у дорослих пацієнтів.
В індукційному дослідженні (PURSUIT-Induction) оцінювалися пацієнти з помірним та тяжким активним виразковим колітом (оцінка Мейо від 6 до 12; ендоскопічний суббалл ≥ 2), які мали неадекватну відповідь або не переносили традиційну терапію або залежали від кортикостероїдів. У частині дослідження, що підтверджує дозу, 761 пацієнт був рандомізований для прийому Симпоні SC 400 мг на тижні 0 і 200 мг на тижні 2, Симпоні SC 200 мг на тижні 0 і 100 мг на тижні 2 або плацебо SC на тижнях 0 і 2. Допускалося одночасне введення стабільних доз пероральних аміносаліцилатів, кортикостероїдів та / або імуномодулюючих засобів. У цьому дослідженні оцінювали ефективність Симпоні до 6 тижня.
Результати підтримуючого дослідження (PURSUIT-Maintenance) базувалися на оцінці 456 пацієнтів, які досягли клінічної відповіді під час попередньої індукції Сімпоні. Пацієнти були рандомізовані для прийому Симпоні 50 мг, Симпоні 100 мг або плацебо підшкірно кожні 4 тижні. Допускалося одночасне введення стабільних доз пероральних аміносаліцилатів та / або імуномодулюючих засобів. Кортикостероїди слід було поступово зменшувати на початку підтримуючого дослідження.У цьому дослідженні ефективність препарату Симпоні оцінювали до 54 -го тижня. Пацієнти, які пройшли підтримуюче дослідження до 54 -го тижня, продовжували лікування в одному дослідженні. до 216 -го тижня. Оцінка ефективності у розширеному дослідженні ґрунтувалася на змінах у застосуванні кортикостероїдів, загальній оцінці лікарем (PGA) активності захворювання та поліпшенні якості життя, виміряній за допомогою Анкети запальних захворювань кишечника (IBDQ).
Таблиця 7
Основні результати ефективності досліджень PURSUIT - Induction та PURSUIT - Maintenance
N = кількість пацієнтів
** p ≤ 0,001
* p ≤ 0,01
a Визначається як зниження від базового рівня в балах Мейо на ≥ 30% та ≥ 3 бали, що супроводжується зменшенням підрекорду ректальної кровотечі ≥ 1 або підрезультату ректальної кровотечі 0 або 1.
b Визначається як оцінка Мейо ≤ 2 бали, без окремих підрахунків> 1
c Визначається як 0 або 1 в ендоскопічному підбаллоні балу Мейо.
d Індукція тільки з Simponi.
e Пацієнтів оцінювали на активність КУ за частковою оцінкою Майо кожні 4 тижні (втрата відповіді підтверджувалася ендоскопією). Тому один пацієнт, який підтримував відповідь, перебував у стані безперервної клінічної відповіді на кожній клінічній оцінці протягом 54 тижня.
f Для досягнення стійкої ремісії пацієнт повинен був перебувати у стадії ремісії на 30 та 54 тижнях (не показуючи втрати відповіді у будь -який момент часу до 54 тижня).
g У пацієнтів з масою тіла менше 80 кг більша частка пацієнтів, які отримували підтримуючу терапію 50 мг, демонструвала стійку клінічну ремісію, ніж ті, хто отримував плацебо.
Більше пацієнтів, які отримували Сімпоні, продемонстрували стійке загоєння слизової оболонки (пацієнти із загоюванням слизової на 30 та 54 тижнях) у групі 50 мг (42%, номінальний р
Серед 54% пацієнтів (247/456), які отримували супутню терапію кортикостероїдами на початку ПЕРСУІТ-Технічного обслуговування, частка пацієнтів, які підтримували клінічну відповідь протягом 54-го тижня і не отримували супутню кортикостероїдну терапію на початку ПІРСУІТ-Технічного обслуговування Тиждень 54 був більшим у групі 50 мг (38%, 30/78) та у групі 100 мг (30%, 25/82) порівняно з групою плацебо (21%, 18/87). ті, хто елімінував кортикостероїди на 54 тижні, були більшими у групі 50 мг (41%, 32/78) та у групі 100 мг (33%, 27/82) порівняно з групою плацебо (22%, 19/87). після подовження дослідження частка суб’єктів, які залишалися без кортикостероїдів, зазвичай зберігалася протягом 216 тижня.
На 6-му тижні Сімпоні значно покращив якість життя, що вимірюється зміною від базового рівня у показнику, специфічному для захворювання, IBDQ (Анкета запальної хвороби кишечника). підтримувався протягом 54 тижня.
Приблизно 63% пацієнтів, які отримували Симпоні на початку розширеного дослідження (56 тиждень), залишалися на лікуванні до кінця дослідження (останнє введення голімумабу на 212 тижні).
Імуногенність
У дослідженнях III, RA, AP та SA до 52-го тижня антитіла до голімумабу були виявлені за допомогою імуноферментного аналізу (ОВНС) у 5% (105/2062) пацієнтів, які отримували голімумаб, і майже всі були антитілами, які нейтралізували в пробірці. Подібні відсотки відзначені в ревматологічних показаннях. Одночасне застосування МТХ призвело до того, що відсоток пацієнтів з антитілами до голімумабу був нижчим, ніж пацієнтів, які отримували голімумаб без МТХ (приблизно 3% [41/1235] проти 8% [64/827] відповідно).
В осьовому SpA nr антитіла до голімумабу були виявлені у 7% (14/193) пацієнтів, які отримували голімумаб, до 52 тижня за допомогою аналізу ОВНС.
У дослідженнях УК ІІ та ІІІ фаз до 54 тижня антитіла до голімумабу були виявлені за допомогою аналізу ОВНС у 3% (26/946) пацієнтів, які отримували голімумаб. Шістдесят вісім відсотків (21/31) пацієнтів, позитивних на антитіла, мали нейтралізуючі антитіла в пробірці. Одночасне лікування імуномодуляторами (азатіоприн, 6-меркаптопурин та МТХ) призвело до того, що відсоток пацієнтів з антитілами до голімумабу був меншим, ніж у пацієнтів, які отримували голімумаб без імуномодуляторів (1% (4/308) проти 3% (22) відповідно). 638)). Серед пацієнтів, які продовжили розширене дослідження і мали оцінювані зразки протягом 228 тижня, антитіла до голімумабу були виявлені у 4% (23/604) пацієнтів, які отримували голімумаб. Вісімдесят два відсотки (18/22) пацієнтів, позитивних на антитіла, мали нейтралізуючі антитіла в пробірці.
Для виявлення антитіл проти голімумабу в дослідженні pJIA був використаний аналіз EIA на толерантність до ліків.Враховуючи підвищену чутливість та покращену толерантність до препаратів, очікується, що при проведенні аналізу ЕІА на толерантність до лікарських засобів буде виявлено більш високу частоту антитіл проти голімумабу порівняно з аналізом ОВНС. У дослідженні ІІІ фази ІІА протягом 48 тижня антитіла до голімумабу були виявлені за допомогою аналізу ЕІА на толерантність до лікарських засобів у 40% (69/172) дітей, які отримували голімумаб, більшість з яких мала титр менше 1: 1000. Вплив на концентрацію голімумабу у сироватці спостерігався при титрах> 1: 100, тоді як ніякого впливу на ефективність не спостерігалося до титрів> 1: 1000, хоча кількість дітей з титрами> 1: 1000 була низькою (N = 8). діти, у яких позитивний результат виявлення антитіл проти голімумабу, 39% (25/65) мали нейтралізуючі антитіла. ефективності та безпеки і тому не представляє ніяких нових сигналів безпеки.
Наявність антитіл до голімумабу може збільшити ризик реакцій у місці ін’єкції (див. Розділ 4.4). Невелика кількість пацієнтів з позитивними антитілами до голімумабу обмежує здатність робити чіткі висновки щодо взаємозв’язку між антитілами до голімумабу та клінічною ефективністю або заходами безпеки.
Оскільки аналізи імуногенності є специфічними для кожного продукту та аналізу, порівняння відсотків антитіл з даними інших продуктів недоцільне.
Педіатричне населення
Поліартикулярний ювенільний ідіопатичний артрит
Безпеку та ефективність препарату Симпоні оцінювали у рандомізованому подвійному сліпому плацебо-контрольованому дослідженні суспензії (GO-KIDS) у 173 дітей (віком від 2 до 17 років) з активною pJIA із щонайменше 5 активними суглобами. Та недостатньою. відповідь на МТХ. У дослідження були включені діти з поліартикулярним перебігом ЮІА (позитивний чи негативний ревматоїдний фактор, поліартрит, обширний олігоартрит, ювенільний псоріатичний артрит або системний ЮІА без постійних системних симптомів). Середня кількість активних суглобів на початку - 12 а середній показник CRP становив 0,17 мг / дл.
Частина 1 дослідження включала відкриту 16-тижневу фазу, на якій 173 зараховані діти отримували Симпоні 30 мг / м2 (максимум 50 мг) підшкірно кожні 4 тижні та МТХ. 154 дитини, які досягли відповіді ACR Ped 30 на 16 -му тижні, увійшли до частини 2 дослідження, фази рандомізованого відміни, і отримували Симпоні 30 мг / м2 (максимум 50 мг) + МТКС або плацебо + МТК кожні. 4 тижні. Після загострення захворювання діти отримували Симпоні 30 мг / м2 (максимум 50 мг) + МТХ. На 48-му тижні немовлята вступили у тривалу фазу подовження.
Діти в цьому дослідженні показали відповіді ACR Ped 30, 50, 70 та 90 ще на 4 -му тижні.
На 16 тижні 87% дітей відповідали на ACR Ped 30, а 79%, 66% і 36% дітей - на ACR Ped 50, ACR Ped 70 та ACR Ped 90 відповідно. На 16 тижні 34 % дітей мали неактивне захворювання, що визначається наявністю усього наступного: відсутність суглобів з активним артритом; відсутність лихоманки, висипу, серозиту, спленомегалії, гепатомегалії або генералізованої лімфаденопатії, що відноситься до ЮІА; відсутність активного увеїту; нормальна ШОЕ (
На 16 тижні всі компоненти ACR Ped продемонстрували клінічно значуще поліпшення порівняно з вихідним показником (див. Таблицю 8).
Таблиця 8
Поліпшення базового рівня компонентів ACR Ped на 16 тижні
на початку = 0 тиждень
b "n" відображає зарахованих пацієнтів
c VAS: Візуальна аналогова шкала
d CHAQ: Анкета оцінки стану здоров'я дитини
та ШОЕ (мм / год): швидкість осідання еритроцитів (міліметри на годину)
Первинна кінцева точка дослідження, відсоток дітей, які на 16 -му тижні реагували на ACR Ped 30 і не відчували загострення між 16 -м тижнем та 48 -м тижнем, не була досягнута. Більшість дітей не мали загострення. тиждень 16 та тиждень 48 (59% у групі Simponi + MTX та 53% у групі плацебо + MTX відповідно; p = 0,41).
Попередньо визначений підгруповий аналіз первинної кінцевої точки на основі вихідних значень CRP (≥ 1 мг / дл проти
На 48 -му тижні 53% та 55% дітей у групі Симпоні + МТХ та плацебо + МТХ відповідно відповідали на ACR Ped 30, а 40% та 28% дітей у групі Симпоні + МТХ та плацебо + МТХ, відповідно, досяг неактивного захворювання.
Європейське агентство з лікарських засобів відстрочило зобов'язання надсилати результати досліджень із застосуванням препарату Симпоні у педіатричній популяції з виразковим колітом (див. Розділ 4.2 для інформації про застосування у педіатрії).
05.2 Фармакокінетичні властивості
Поглинання
Після одноразового «підшкірного введення голімумабу здоровим пацієнтам або пацієнтам з РА середній час досягнення максимальної сироваткової концентрації (Tmax) становив від 2 до 6 днів. Підшкірна ін’єкція голімумабу у дозі 50 мг у здорових осіб призвела до досягнення середньої максимальної концентрації у сироватці крові. (Cmax) ± стандартне відхилення 3,1 ± 1,4 мкг / мл.
Після одноразової підшкірної ін’єкції 100 мг абсорбція голімумабу була подібною у руці, животі та стегні, із середньою абсолютною біодоступністю 51%.Підшкірно, абсолютна біодоступність у дозі 50 мг або 200 мг голімумабу очікується подібною.
Розповсюдження
Після одноразового внутрішньовенного введення середній об’єм розподілу становив 115 ± 19 мл / кг.
Ліквідація
Системний кліренс голімумабу оцінювався як 6,9 ± 2,0 мл / добу / кг. Оцінювалося, що кінцевий період напіввиведення становить близько 12 ± 3 днів у здорових добровольців і мав подібні значення у пацієнтів з РА, АП, СА або КУ.
Коли дозу голімумабу у дозі 50 мг вводили підшкірно пацієнтам з РА, АР чи АС кожні 4 тижні, концентрація у сироватці крові досягала стаціонарного стану до 12 тижня. При одночасному застосуванні МТХ лікування голімумабом у дозі 50 мг підшкірно кожні 4 тижні дало середнє значення (± стандартне відхилення) мінімальна сироваткова концентрація у рівноважному стані приблизно 0,6 ± 0,4 мкг / мл у пацієнтів з активним РА, незважаючи на терапію МТКС, приблизно 0,5 ± 0,4 мкг / мл у пацієнтів з активною АП та приблизно 0,8 ± 0,4 мкг / мл у Пацієнти з АС. Середні рівні мінімальної рівноважної концентрації голімумабу у пацієнтів з аксиальним SpA nr були подібними до тих, що спостерігалися у пацієнтів з АС після підшкірного введення 50 мг голімумабу кожні 4 тижні.
Пацієнти з РА, АР або СА, які не отримували одночасно МТХ, мали найнижчі концентрації голімумабу у рівноважному стані приблизно на 30% нижчі, ніж у пацієнтів, які отримували голімумаб з МТХ. У обмеженої кількості хворих на РА, які отримували голімумаб підшкірно протягом більше 6 місяців, одночасне застосування МТХ зменшило видимий кліренс голімумабу приблизно на 36%. Однак аналізи фармакокінетики населення показують, що одночасне застосування НПЗЗ, пероральних кортикостероїдів або сульфасалазину не впливало на очевидний кліренс голімумабу.
Після введення індукційних доз голімумабу 200 мг та 100 мг відповідно на 0 та 2 тижні відповідно та згодом підтримуючі дози 50 мг або 100 мг голімумабу підшкірно кожні 4 тижні у пацієнтів з УК концентрації голімумабу у сироватці досягали рівноважного стану приблизно через 14 тижнів після початку лікування Лікування голімумабом у дозі 50 мг або 100 мг підшкірно кожні 4 тижні під час підтримки призводило до середньої рівноважної мінімальної концентрації у сироватці крові приблизно на 0, 9 ± 0,5 мкг / мл та 1,8 ± 1,1 мкг / мл відповідно.
У пацієнтів з УК, які отримували 50 мг або 100 мг голімумабу підшкірно кожні 4 тижні, одночасне застосування імуномодуляторів не мало істотного впливу на мінімальні рівні голімумабу у рівноважному стані.
Пацієнти, які виробили антитіла проти голімумабу, мали в цілому низькі рівноважні мінімальні концентрації голімумабу в сироватці крові (див. Розділ 5.1).
Лінійність
У пацієнтів з РА голімумаб демонстрував приблизно пропорційні дозі фармакокінетичні параметри в діапазоні доз 0,1 - 10,0 мг / кг після одноразової внутрішньовенної дози.Після одноразової дози СК у здорових добровольців Приблизно пропорційні фармакокінетичні параметри спостерігалися також у діапазоні доз Від 50 до 400 мг.
Вплив ваги на фармакокінетику
Існує тенденція до збільшення видимого кліренсу голімумабу із збільшенням ваги (див. Розділ 4.2).
Педіатричне населення
Фармакокінетику голімумабу визначали у 173 дітей з pJIA у віці від 2 до 17 років. У дослідженні pJIA у дітей, які отримували голімумаб у дозі 30 мг / м2 (максимум 50 мг) підшкірно кожні 4 тижні, середня мінімальна концентрація голімумабу у рівноважному стані була однаковою у різних вікових групах і була також подібною або трохи вищою, ніж у дорослих РА пацієнти, які отримували 50 мг голімумабу кожні 4 тижні.
Популяційні фармакокінетичні / фармакодинамічні моделі та моделювання у дітей з pJIA підтвердили взаємозв’язок між експозицією голімумабу в сироватці крові та клінічною ефективністю та підтверджують, що дозу голімумабу у дозі 50 мг кожні 4 тижні кожні 4 тижні у дітей з вагою щонайменше 40 кг дозволяють досягати експозицій, подібних до тих, які показали свою ефективність у дорослих.
05.3 Дані доклінічної безпеки
Неклінічні дані не виявляють особливої небезпеки для людини на основі звичайних досліджень фармакології безпеки, токсичності при повторних дозах, токсичності для репродуктивної системи та розвитку.
Дослідження мутагенності, фертильності тварин або довгострокової канцерогенності не проводилися з голімумабом.
У дослідженні фертильності та загальних репродуктивних функцій мишей з використанням подібного антитіла, яке вибірково пригнічує функціональну активність мишачого TNF?, Кількість вагітних мишей була зменшена. Невідомо, чи були ці результати обумовлені ефектами. В еволюційному дослідженні токсичності, проведеному на мишах після введення того самого аналогового антитіла, і на мавпах -циномолгах, які використовували голімумаб, не було ознак токсичності для матері, ембріотоксичності чи тератогенності.
06.0 ФАРМАЦЕВТИЧНА ІНФОРМАЦІЯ
06.1 Допоміжні речовини
Сорбіт (E420)
L-гістидин
L-гістидин моногідрохлорид моногідрат
Полісорбат 80
Вода для ін'єкцій.
06.2 Несумісність
За відсутності досліджень сумісності цей лікарський засіб не можна змішувати з іншими продуктами.
06.3 Строк дії
22 місяці
06.4 Особливі умови зберігання
Зберігати в холодильнику (2 ° C - 8 ° C).
Не заморожувати.
Зберігайте попередньо заповнену ручку або наповнений шприц у зовнішній коробці для захисту від світла.
06.5 Характер безпосередньої упаковки та вміст упаковки
Симпоні 50 мг розчин для ін’єкцій у попередньо заповненій ручці
0,5 мл розчину у попередньо заповненому шприці (склянка типу 1) із фіксованою голкою (нержавіюча сталь) та ковпачком для голки (гума, що містить латекс), у попередньо заповненій ручці. ручка та мультиупаковки, що містять 3 (3 пачки по 1) попередньо заповнених ручок.
Симпоні 50 мг розчин для ін’єкцій у попередньо заповненому шприці
0,5 мл розчину у попередньо заповненому шприці (скло 1 типу) із нерухомою голкою (нержавіюча сталь) та ковпачком для голки (гума, що містить латекс). пачки 1) попередньо заповнених шприців.
Не всі розміри упаковок можна продавати.
06.6 Інструкції з використання та поводження
Simponi поставляється в одноразовому попередньо заповненому ручці під назвою SmartJect або в одноразовому попередньо заповненому шприці. Кожна упаковка Simponi поставляється з інструкцією із застосування, яка повністю описує, як користуватися ручкою або шприцом. Після того, як попередньо заповнену ручку або наповнений шприц вийняли з холодильника, слід дати їй досягти кімнатної температури, почекавши 30 хвилин, перш ніж вводити Симпоні. Ручку або шприц не слід струшувати.
Розчин прозорий до злегка опалесцентного, від безбарвного до блідо -жовтого кольору і може містити невеликі напівпрозорі або білі білкові частинки. Це не рідкість для розчинів, що містять білки.
Симпоні не можна використовувати, якщо розчин змінив колір, помутнів або містить видимі сторонні частинки.
Повні вказівки щодо приготування та застосування Симпоні у попередньо заповненій ручці або наповненому шприці наведені в інструкції з упаковки.
Невикористані ліки та відходи, отримані з цього препарату, слід утилізувати відповідно до місцевих правил.
07.0 ВЛАСНИК РОЗРОБНИЦТВА
Janssen Biologics B.V.
Ейнштейнвег 101
2333 CB Leiden
Нідерланди
08.0 НОМЕР РОЗВИТКУ З РОБОТИ
EU/1/09/546/001 1 попередньо заповнена ручка
EU/1/09/546/002 3 попередньо заповнені ручки
EU/1/09/546/003 1 попередньо заповнений шприц
EU/1/09/546/004 3 попередньо заповнені шприци
039541014
039541026
039541038
039541040
09.0 ДАТА ПЕРШОГО ДОЗВІЛЕННЯ АБО ОНОВЛЕННЯ ДОЗВІЛЛЯ
Дата першого дозволу: 1 жовтня 2009 року
Дата останнього оновлення: 19 червня 2014 року
10.0 ДАТА ПЕРЕГЛЯНУ ТЕКСТУ
02 лютого 2017 року
11.0 ДЛЯ РАДІОЛЕКЦІЙ, ПОВНІ ДАНІ ПРО ВНУТРІШНЮ РАДІАЦІЮ
12.0 ДЛЯ РАДІОЛЕКЦІЙ, ДОДАТКОВИХ ДЕТАЛЬНИХ ІНСТРУКЦІЙ З ВИКОРИСТОЇ ПІДГОТОВКИ І КОНТРОЛЮ ЯКОСТІ














.jpg)