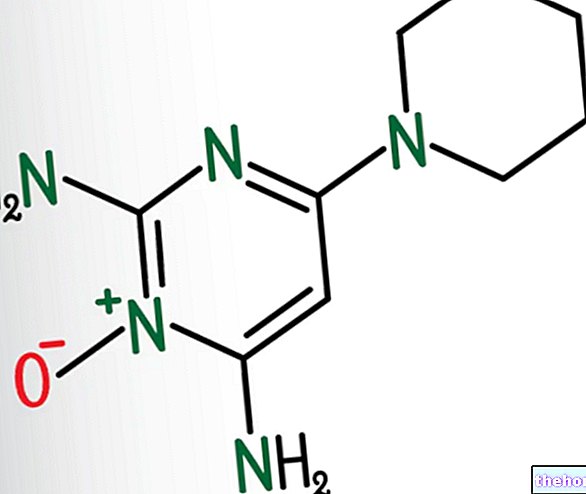
Структура та функції
Гемоглобін - це металопротеїн, що міститься в еритроцитах, який відповідає за транспортування кисню в кров. Насправді, кисень лише помірно розчинний у воді; тому кількості, розчиненої у крові (менше 2% від загальної кількості), недостатньо для задоволення метаболічних потреб тканин. Тому потреба в конкретному перевізнику очевидна.
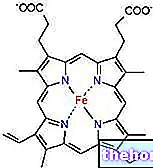
У кровоносному руслі кисень не може зв’язуватися безпосередньо і оборотно з білками, як це відбувається замість таких металів, як мідь і залізо.Не дивно, що в центрі кожної білкової субодиниці гемоглобіну, загорнутої в білкову оболонку, ми знаходимо так званий протез група EME, з металевим серцем, представленим атомом заліза в стані окислення Fe2 + (відновлений стан), який пов'язує кисень оборотним шляхом.
Аналіз крові
- Нормальні значення гемоглобіну в крові: 13-17 г / 100 мл
У жінок ці показники в середньому на 5-10% нижче, ніж у чоловіків.
Можливі причини підвищеного гемоглобіну
- Поліцитемія
- Тривале перебування на високих землях
- Хронічні захворювання легенів
- Хвороба серця
- Допінг крові (використання еритропоетину та похідних або речовин, що імітують їх дію)
Можливі причини зниження гемоглобіну
- Анемії
- Дефіцит заліза (дефіцит заліза)
- Рясна кровотеча
- Карциноми
- Вагітність
- Талассемія
- Опіки
Тому вміст кисню в крові визначається підсумовуванням невеликої кількості, розчиненої у плазмі, з часткою, пов’язаною із залізом гемоглобіну.
Більше 98% кисню, присутніх у крові, зв’язано з гемоглобіном, який, у свою чергу, циркулює у крові, що виділяється в еритроцитах.
Враховуючи центральну роль цього металу, синтез гемоглобіну вимагає адекватного надходження заліза в раціон. Приблизно 70% заліза, наявного в організмі, насправді міститься в гемових групах гемоглобіну.
Гемоглобін складається з 4 субодиниць, які за структурою дуже схожі на міоглобін *.
* Хоча гемоглобін транспортує кисень з легенів до тканин, міоглобін переносить кисень, що виділяється гемоглобіном, до різних клітинних органел, які його використовують (наприклад, мітохондрії).

Гемоглобін - це великий і складний металопротеїн, який характеризується чотирма глобулярними білковими ланцюгами, відповідно обгорнутими навколо групи гему, що містить Fe2 +.
Тому для кожної молекули гемоглобіну ми знаходимо чотири групи гему, загорнуті у відносний глобулярний білковий ланцюг. Оскільки в кожній молекулі гемоглобіну є чотири атоми заліза, кожна молекула гемоглобіну може зв’язати чотири атоми кисню з собою відповідно до оборотної реакції:
Hb + 4O2 ← → Hb (O2) 4
Як відомо більшості, завдання гемоглобіну полягає в тому, щоб взяти кисень у легені, виділити його клітинам, які цього потребують, взяти з них вуглекислий газ і випустити його в легені, де знову починається чило.
Під час проходження крові в капілярах легеневих альвеол гемоглобін зв’язує з собою кисень, який згодом виділяється в тканини периферичного кровообігу. Цей обмін відбувається тому, що зв’язки кисню з залізом групи ЕМЕ лабільні і чутливі до багатьох факторів, найважливішим з яких є натяг або парціальний тиск кисню.
Зв’язування кисню з гемоглобіном та ефект Бора
У легенях напруга кисню плазми збільшується внаслідок дифузії газу з альвеол до крові (↑ PO2); це збільшення змушує гемоглобін завзято зв’язуватися з киснем; навпаки відбувається в периферичних тканинах, де концентрація розчиненого кисню в крові зменшується (↓ PO2), а парціальний тиск вуглекислого газу збільшується (↑ CO2); це спонукає гемоглобін вивільняти кисень і заряджатися СО2. Максимально спрощуючи концепцію, чим більше вуглекислого газу в крові, тим менше кисню залишається зв’язаним з гемоглобіном.
Хоча кількість кисню, що фізично розчиняється в крові, дуже низька, вона відіграє фундаментальну роль. Насправді, ця величина сильно впливає на міцність зв’язку між киснем і гемоглобіном (а також є «важливою еталонною величиною для регулювання легеневої вентиляції).
Узагальнюючи все графіком, кількість кисню, пов'язаного з гемоглобіном, зростає по відношенню до рО2 за сигмоподібною кривою:

Той факт, що область плато настільки велика, є важливим запасом безпеки при максимальному насиченні гемоглобіну під час проходження в легені. Хоча рО2 на рівні альвеол зазвичай дорівнює 100 мм рт.ст. навіть при частковому тиску кисню, що дорівнює 70 мм рт.
У зоні максимального нахилу, коли часткова напруга кисню падає нижче 40 мм рт. Ст., Здатність гемоглобіну зв’язувати кисень раптово падає.
В умовах спокою PO2 у внутрішньоклітинних рідинах становить приблизно 40 мм рт. в цьому місці через закони газів кисень, розчинений у плазмі, дифундує у бік бідніших тканин О2, перетинаючи капілярну мембрану, отже, напруга плазми О2 падає далі, що сприяє вивільненню кисню з гемоглобіну. . З іншого боку, під час інтенсивних фізичних навантажень напруга кисню в тканинах падає до 15 мм рт.ст. або менше, внаслідок чого кров сильно виснажується киснем.
Як було сказано, в умовах спокою значна кількість кисневого гемоглобіну залишає тканини, залишаючись доступним у разі потреби (наприклад, для боротьби з раптовим збільшенням метаболізму в деяких клітинах).
Суцільна лінія, показана на зображенні вище, називається кривою дисоціації гемоглобіну; його зазвичай визначають in vitro при рН 7,4 та температурі 37 ° С.
Ефект Бора впливає як на надходження О2 на рівні легенів, так і на його вивільнення на тканинному рівні.
Там, де більше розчиненого вуглекислого газу у формі бікарбонату, гемоглобін легше виділяє кисень і заряджається вуглекислим газом (у формі бікарбонату).

Такий самий ефект досягається підкисленням крові: чим сильніше знижується рН крові і тим менше кисню залишається зв’язаним з гемоглобіном; не дивно, що в крові вуглекислий газ розчиняється переважно у формі вуглекислоти, яка дисоціює.



На честь свого першовідкривача вплив рН або вуглекислого газу на дисоціацію кисню відомий як ефект Бора.
Як і передбачалося, в кислому середовищі гемоглобін легше виділяє кисень, тоді як в основному середовищі зв’язок з киснем міцніший.

Інші фактори, здатні змінювати спорідненість гемоглобіну до кисню, включають температуру. Зокрема, спорідненість гемоглобіну до кисню знижується зі збільшенням температури тіла. Це особливо вигідно в зимові та весняні місяці, оскільки температура легеневої крові (у контакті з повітря зовнішнього середовища) нижче, ніж у тканинах, де, таким чином, полегшується вивільнення кисню.

2.3 дифосфогліцерат є проміжним продуктом гліколізу, що впливає на спорідненість гемоглобіну до кисню. Якщо його концентрація в еритроцитах зростає, спорідненість гемоглобіну до кисню зменшується, що полегшує вивільнення кисню в тканини. Не дивно, що концентрація еритроцитів 2,3 дифосфогліцерату збільшується, наприклад, при анемії, серцево-легеневій недостатності та під час перебування на великій висоті.
Загалом, вплив 2,3 бісфосфогліцерату є відносно повільним, особливо у порівнянні з швидкою реакцією на зміну рН, температури та парціального тиску вуглекислого газу.

Ефект Бора дуже важливий під час інтенсивної м’язової роботи; фактично в таких умовах у тканинах, які найбільше піддаються стресу, відбувається місцеве підвищення температури та тиску вуглекислого газу, а отже, і кислотності крові. Як пояснювалося вище, все це сприяє вивільненню кисню до тканин, зміщуючи криву дисоціації гемоглобіну вправо.